
3£®ÔÚ̀úÆ·É϶Æ̉»¶¨ºñ¶ÈµÄĐ¿²ă£¬̉ÔÏ·½°¸Éè¼ÆƠưÈ·µÄÊÇ
A£®Đ¿×÷Ñô¼«£¬¶Æ¼₫×÷̉ơ¼«£¬ÈÜ̉ºÖĐº¬ÓĐĐ¿Àë×Ó
B£®²¬×÷̉ơ¼«£¬¶Æ¼₫×÷Ñô¼«£¬ÈÜ̉ºÖĐº¬ÓĐĐ¿Àë×Ó
C£®̀ú×÷Ñô¼«£¬¶Æ¼₫×÷̉ơ¼«£¬ÈÜ̉ºÖĐº¬ÓĐÑÇ̀úÀë×Ó
D£®Đ¿×÷̉ơ¼«£¬¶Æ¼₫×÷Ñô¼«£¬ÈÜ̉ºÖĐº¬ÓĐĐ¿Àë×Ó
2£®ÈôijװÖĂ(µç½â³Ø»̣Ôµç³Ø)ÖĐ·¢Éú·´Ó¦µÄÀë×Ó·½³̀ʽÊÇ£ºCu+2H+£½Cu2+ +H2¡ü£¬¹ØÓÚ¸Ă×°ÖõÄÓĐ
A£®¿ÉÄÜÊÇÔµç³Ø£¬̉²¿ÉÄÜÊǵç½â³Ø¡¡¡¡¡¡¡¡¡¡¡¡ B£®Ö»ÄÜÊÇÔµç³Ø£¬Ç̉µç½âÖÊÈÜ̉ºÎªÏơËá
C£®Ö»ÄÜÊǵç½â³Ø£¬Ç̉½đÊôÍΪ¸Ăµç½â³ØµÄÑô¼«¡¡ D£®Ö»ÄÜÊǵç½â³Ø£¬µç½âÖÊÈÜ̉º¿É̉ÔÊÇÏơËá
1£®ÏÂÁĐ¹ØÓÚ͵缫µÄĐđÊöƠưÈ·µÄÊÇ
A£®ÍĐ¿Ôµç³ØÖĐÍÊÇƠư¼«£¬Đ¿ÊǸº¼«¡¡¡¡¡¡¡¡¡¡ B£®Óõç½â·¨¾«Á¶´ÖÍʱ£¬´ÖÍ×÷̉ơ¼«
C£®ÔڶƼ₫Éϵç¶ÆÍʱ¿ÉÓĂ½đÊôÍ×÷Ñô¼«¡¡¡¡¡¡¡¡ D£®µç½âÏ¡Ạ́ËáÖÆH2¡¢O2ʱÍ×÷Ñô¼«
6£®Âȼµç½â±¥ºÍʳÑÎË®ÖÆÈ¡NaOHµÄ¹¤̉ƠÁ÷³̀ʾ̉âͼÈçͼËùʾ£º
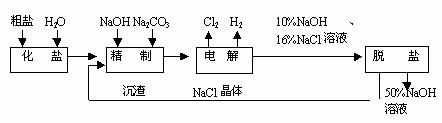
̉À¾ƯÉÏͼ£¬Íê³ÉÏÂÁĐ̀î¿Ơ£º¢Å ÔÚµç½â¹ư³̀ÖĐ£¬ÓëµçÔ´Ơư¼«ÏàÁ¬µÄµç¼«ÉÏËù·¢Éú·´Ó¦µÄ»¯Ñ§·½³̀ʽΪ____¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ___£¬ÈÜ̉ºµÄpH______(̀î¡°Éư¸ß¡±»̣¡°½µµÍ¡±»̣¡°²»±ä¡±)£»¢Æ ¹¤̉µÊ³Ñκ¬Ca2+¡¢Mg2+µÈÔÓÖÊ£¬¾«Öƹư³̀·¢Éú·´Ó¦µÄÀë×Ó·½³̀ʽΪ__¡¡¡¡¡¡¡¡¡¡¡¡ ____£»¢Ç Èç¹û´ÖÑÎÖĐSO42-º¬Á¿½Ï¸ß£¬±ØĐë̀í¼Ó±µÊÔ¼Á³ưÈ¥SO42££¬¸Ă±µÊÔ¼Á¿É̉ÔÊÇ_____(Ñ¡̀îa¡¢b¡¢c)£»a£®Ba(OH)2£¬b£®Ba(NO3)2£¬c£®BaCl2£»
¢È ΪÓĐЧ³ưÈ¥Ca2+¡¢Mg2+¡¢SO42££¬¼ÓÈëÊÔ¼ÁµÄºÏÀí˳Đ̣Ϊ_____(Ñ¡̀îa¡¢b¡¢c)£»a£®ÏȼÓNaOH£¬ºó¼ÓNa2CO3£¬ÔÙ¼Ó±µÊÔ¼Á£»b£®ÏȼÓNaOH£¬ºó¼Ó±µÊÔ¼Á£¬ÔÙ¼ÓNa2CO3£»c£®ÏȼӱµÊÔ¼Á£¬ºó¼ÓNaOH£¬ÔÙ¼ÓNa2CO3£»¢É ÍÑÑι¤Đ̣ÖĐÀûÓĂNaOHºÍNaClÔÚÈܽâ¶ÈÉϵIJî̉́£¬Í¨¹ư_________¡¢ÀäÈ´¡¢_______(̀îĐ´²Ù×÷Ăû³Æ)³ưÈ¥NaCl£»¢Ê ÔÚ¸ôĤ·¨µç½âʳÑÎˮʱ£¬µç½â²Û·Ö¸ôΪÑô¼«ÇøºÍ̉ơ¼«Çø£¬·ÀÖ¹Cl2ÓëNaOH·´Ó¦£»²ÉÓĂÎ̃¸ôĤµç½âÀäµÄʳÑÎˮʱ£¬Cl2ÓëNaOH³ä·Ö½Ó´¥£¬²úÎï½öÊÇNaClOºÍH2£¬ÏàÓ¦µÄ»¯Ñ§·½³̀ʽΪ__________¡£
¿ÎºóÁ·Ï°
5£®(2002´º¼¾12)ͨ̉ÔÏàµÈµÄµçÁ¿£¬·Ö±đµç½âµÈŨ¶ÈµÄÏơËá̉øºÍÏơËáÑǹ¯(Ñǹ¯µÄ»¯ºÏ¼ÛΪ+1)ÈÜ̉º£¬Èô±»»¹ÔµÄÏơËá̉øºÍÏơËáÑǹ¯µÄÎïÖʵÄÁ¿Ö®±Èn(ÏơËá̉ø)©Un(ÏơËáÑǹ¯)£½2©U1£¬ỘÏÂÁбíÊöƠưÈ·µÄÊÇ
A.ÔÚÁ½¸ö̉ơ¼«ÉÏµĂµ½µÄ̉øºÍ¹¯µÄÎïÖʵÄÁ¿Ö®±Èn(̉ø)©Un(¹¯)£½2©U1
B.ÔÚÁ½¸öÑô¼«ÉÏµĂµ½µÄ²úÎïµÄÎïÖʵÄÁ¿²»ÏàµÈ
C.ÏơËáÑǹ¯µÄ·Ö×ÓʽΪHgNO3
D.ÏơËáÑǹ¯µÄ·Ö×ÓʽΪHg2(NO3)2
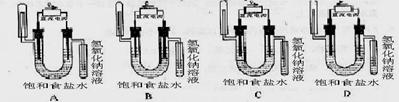
4£®(2004ÉϺ£13)ÏÂͼÖĐÄÜÑéÖ¤ÂÈ»¯ÄÆÈÜ̉º(º¬·Ó̀ª)µç½â²úÎïµÄ×°ÖĂÊÇ
¡¡
3£®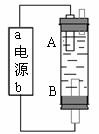 ijͬѧÉè¼ÆÁË̉»ÖÖµç½â·¨ÖÆÈ¡Fe(OH)2µÄʵÑé×°ÖĂ(ÈçÓ̉ͼ)¡£Í¨µçºó£¬ÈÜ̉ºÖĐ²úÉú°×É«³Áµí£¬Ç̉½Ï³¤Ê±¼ä²»±äÉ«¡£ÏÂÁĐ˵·¨ÖĐƠưÈ·µÄÊÇ
ijͬѧÉè¼ÆÁË̉»ÖÖµç½â·¨ÖÆÈ¡Fe(OH)2µÄʵÑé×°ÖĂ(ÈçÓ̉ͼ)¡£Í¨µçºó£¬ÈÜ̉ºÖĐ²úÉú°×É«³Áµí£¬Ç̉½Ï³¤Ê±¼ä²»±äÉ«¡£ÏÂÁĐ˵·¨ÖĐƠưÈ·µÄÊÇ
A£®µçÔ´ÖĐ¡°a¡±Îª¸º¼«£¬¡°b¡±ÎªƠư¼«
B£®µç½â³ØÖеĵç½ẩº¿É̉ÔÊÇNaOHÈÜ̉º»̣NaClÈÜ̉º
C£®Bµç¼«·¢ÉúµÄ·´Ó¦£º2H2O+2e££½H2¡ü+2OH£
D£®A¡¢BÁ½¶Ë¶¼±ØĐëʹÓẰú×÷µç¼«
2£®ÔÚË®ÖĐ¼ÓÈëµÈÎïÖʵÄÁ¿µÄAg+¡¢Pb2+¡¢Na+¡¢SO42£¡¢NO3£¡¢Cl£¡£¸ĂÈÜ̉º·ÅÔÚÓöèĐÔ²ÄÁÏ×÷µç¼«µÄµç½â²ÛÖĐ£¬Í¨µçƬ¿̀£¬ỘÑơ»¯²úÎïºÍ»¹Ô²úÎïµÄÖÊÁ¿±ÈΪ
A£®35.5¡Ă108¡¡¡¡¡¡¡¡¡¡¡¡ B£®16¡Ă207¡¡¡¡¡¡¡¡¡¡¡¡ C£®8¡Ă1¡¡¡¡¡¡¡¡¡¡¡¡ D£®108¡Ă35.5
1£®ÔÚÔµç³ØºÍµç½â³ØµÄµç¼«ÉÏËù·¢ÉúµÄ·´Ó¦£¬Í¬ÊôÑơ»¯·´Ó¦»̣ͬÊô»¹Ô·´Ó¦µÄÊÇ
A£®Ôµç³ØµÄƠư¼«ºÍµç½â³ØµÄÑô¼«Ëù·¢ÉúµÄ·´Ó¦
B£®Ôµç³ØµÄƠư¼«ºÍµç½â³ØµÄ̉ơ¼«Ëù·¢ÉúµÄ·´Ó¦
C£®Ôµç³ØµÄ¸º¼«ºÍµç½â³ØµÄÑô¼«Ëù·¢ÉúµÄ·´Ó¦
D£®Ôµç³ØµÄ¸º¼«ºÍµç½â³ØµÄ̉ơ¼«Ëù·¢ÉúµÄ·´Ó¦
[Àư1]ÓöèĐԵ缫ʵÏÖµç½â£¬ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A£®µç½âÏ¡Ạ́ËáÈÜ̉º£¬ÊµÖÊÉÏÊǵç½âË®£¬¹ÊÈÜ̉ºpH²»±ä
B£®µç½âÏ¡ÇâÑơ»¯ÄÆÈÜ̉º£¬̉ªÏûºÄOH££¬¹ÊÈÜ̉ºpH¼ơĐ¡
C£®µç½âẠ́ËáÄÆÈÜ̉º£¬ÔÚ̉ơ¼«ÉϺÍÑô¼«ÉÏÎö³ö²úÎïµÄÎïÖʵÄÁ¿Ö®±ÈΪ1¡Ă2
D£®µç½âÂÈ»¯ÍÈÜ̉º£¬ÔÚ̉ơ¼«ÉϺÍÑô¼«ÉÏÎö³ö²úÎïµÄÎïÖʵÄÁ¿Ö®±ÈΪ1¡Ă1
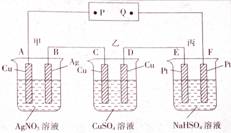 [Àư2]ÈçͼËùʾ£¬Í¨µçºó£¬A¼«ÉÏÎö³öAg£¬¶Ô¸Ă×°ÖõÄÓĐ¹ØĐđÊöÖĐƠưÈ·µÄÊÇ
[Àư2]ÈçͼËùʾ£¬Í¨µçºó£¬A¼«ÉÏÎö³öAg£¬¶Ô¸Ă×°ÖõÄÓĐ¹ØĐđÊöÖĐƠưÈ·µÄÊÇ
A£®PÊǵçÔ´µÄƠư¼«
B£®F¼«ÉÏ·¢ÉúµÄ·´Ó¦Îª4OH¨D¨D4e££½2H2O+O2¡ü
C£®µç½âʱ£¬¼×¡¢̉̉¡¢±ûÈư³ØÖĐ£¬³ưÁËE¡¢FÁ½¼«Í⣬ÆäËûµç¼«¾ù²Î¼ÓÁË·´Ó¦
D£®Í¨µçºó£¬¼×³ØÈÜ̉ºµÄpH¼ơĐ¡£¬¶ø̉̉¡¢±ûÁ½³ØÈÜ̉ºµÄpH²»±ä
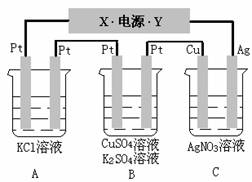 [Àư3]ÈçÏÂͼËùʾ£¬Èôµç½â5minʱ͵缫ÖÊÁ¿Ôö¼Ó2.16g£¬ÊÔ»Ø´đ£º¢ÅµçÔ´µç¼«XĂû³ÆΪ_______¡£¢Æ±ä»¯£ºA________,B_________,
C_________¡£
[Àư3]ÈçÏÂͼËùʾ£¬Èôµç½â5minʱ͵缫ÖÊÁ¿Ôö¼Ó2.16g£¬ÊÔ»Ø´đ£º¢ÅµçÔ´µç¼«XĂû³ÆΪ_______¡£¢Æ±ä»¯£ºA________,B_________,
C_________¡£
¢Ç ͨµç5minʱ£¬BÖĐ¹²ÊƠ¼¯224mLÆø̀å(±ê¿ö)£¬ÈÜ̉º̀å»ưΪ200mL¡£(Éèµç½âÇ°ºóÎ̃̀å»ư±ä»¯)ỘͨµçÇ°CuSO4ÈÜ̉ºµÄÎïÖʵÄÁ¿Å¨¶ÈΪ__________¡£
¢È ÈôAÖĐKClÈÜ̉ºµÄ̀å»ử²ÊÇ200mL£¬µç½âºó£¬ÈÜ̉ºµÄpHÊÇ___________(ÉèÇ°ºó̀å»ưÎ̃±ä»¯)¡£
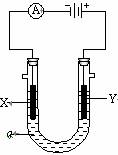 [Àư4]£®µç½âÔÀíÔÚ»¯Ñ§¹¤̉µÖĐÓĐ¹ă·ºÓ¦ÓĂ¡£Ó̉ͼ±íʾ̉»¸öµç½â³Ø£¬×°Óеç½ẩºa£»X¡¢YÊÇÁ½¿éµç¼«°å£¬Í¨¹ưµ¼ÏßÓëÖ±Á÷µçÔ´ÏàÁ¬¡£Çë»Ø´đ̉ÔÏÂÎỀ⣺(04¸£ƠăÀí×Û)
[Àư4]£®µç½âÔÀíÔÚ»¯Ñ§¹¤̉µÖĐÓĐ¹ă·ºÓ¦ÓĂ¡£Ó̉ͼ±íʾ̉»¸öµç½â³Ø£¬×°Óеç½ẩºa£»X¡¢YÊÇÁ½¿éµç¼«°å£¬Í¨¹ưµ¼ÏßÓëÖ±Á÷µçÔ´ÏàÁ¬¡£Çë»Ø´đ̉ÔÏÂÎỀ⣺(04¸£ƠăÀí×Û)
(1) ÈôX¡¢Y¶¼ÊǶèĐԵ缫£¬aÊDZ¥ºÍNaClÈÜ̉º£¬ÊµÑ鿪ʼʱ£¬Í¬Ê±ÔÚÁ½±ß¸÷µÎÈ뼸µÎ·Ó̀ªÊỔº£¬Ộ
¢Ù µç½â³ØÖĐX¼«Éϵĵ缫·´Ó¦Ê½Îª¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£ÔÚX¼«¸½½ü¹Û²́µ½µÄÏÖÏóÊÇ¡¡ ¡¡¡¡¡¡¡£
¢Ú Yµç¼«Éϵĵ缫·´Ó¦Ê½Îª¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡£¬¼́Ñé¸Ăµç¼«·´Ó¦²úÎïµÄ·½·¨ÊÇ¡¡¡¡ ¡¡¡¡¡¡¡£
(2) Èç̉ªÓõç½â·½·¨¾«Á¶´ÖÍ£¬µç½ẩºaÑ¡ÓĂCuSO4ÈÜ̉º£¬Ộ
¢Ù Xµç¼«µÄ²ÄÁÏÊÇ¡¡¡¡ £¬µç¼«·´Ó¦Ê½ÊÇ¡¡ ¡¡¡¡¡¡¡¡¡¡¡£
¢Ú Yµç¼«µÄ²ÄÁÏÊÇ¡¡¡¡ £¬µç¼«·´Ó¦Ê½ÊÇ¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡£(˵Ă÷£ºÔÓÖÊ·¢ÉúµÄµç¼«·´Ó¦²»±ØĐ´³ö)
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com