
26、(9分)将3.2gCu溶于30 mL R
mol/L过量硝酸溶液中,已知硝酸的还原产物只有NO2和NO,反应结束后,将所得溶液加水稀释至1.0 L,测得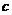 (NO
(NO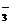 )=0.20 mol/L
)=0.20 mol/L
(1)求稀释后溶液的pH;
(2)若R的值为8,求生成气体中NO2和NO的物质的量;
(3)用NaOH溶液吸收氮的氧化物以防止污染,原理是:
NO+NO2+NaOH=2NaNO2+H2O,
2NO2+2NaOH=NaNO3+NaNO2+H2O.
若生成的混合气体能被NaOH溶液完全吸收,试讨论R的取值范围.
长河高中2010届高三第二次教学质量检测
25.(12分)
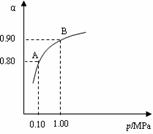 (1)某温度下,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如右图所示。将2.0 mol SO2和1.0 mol O2置于5 L密闭容器中,反应达平衡后,体系总压强为0.10 M Pa。试计算反应2SO2+O2
(1)某温度下,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如右图所示。将2.0 mol SO2和1.0 mol O2置于5 L密闭容器中,反应达平衡后,体系总压强为0.10 M Pa。试计算反应2SO2+O2 2SO3在该温度时的平衡常数(写出计算过程)。
2SO3在该温度时的平衡常数(写出计算过程)。
(2)为循环利用催化氧化所使用的催化剂钒触媒(V2O5),科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上。已知废钒催化剂中含有V2O5、VOSO4及不溶性残渣。查阅资料知:VOSO4可溶于水,V2O5难溶于水,NH4VO3难溶于水。该工艺的流程如下图。
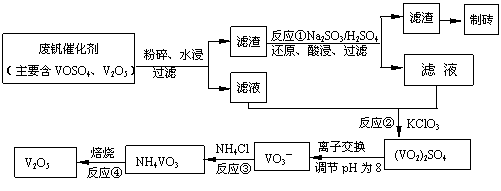
请回答下列问题:
过滤操作中需用到的玻璃仪器有 。
反应①②③④中属于氧化还原反应的是 (填数字序号)。写出其中一个反应的化学方程式,并标出电子转移的方向和数目 。
24.(11分)二氯化硫(SCl2)熔点-780C,沸点590C,密度1.638g/cm3,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2),以下是由氯气与硫反应合成二氯化硫的实验装置,其中F中装有无水CaCl2固体。

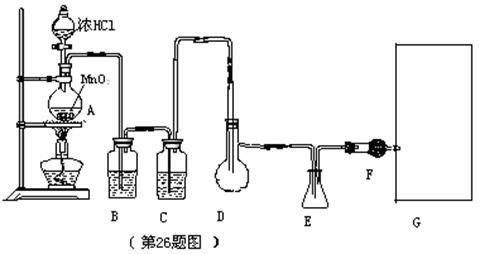
试回答下列问题:
(1)写出二氯化硫与三氧化硫作用可生成亚硫酰氯的化学方程式
(2)装置C中盛放的试剂是 ,其作用为
(3)实验开始前先排尽系统中空气,在D中放入一定量的硫粉,加热使之融化,然后摇动烧瓶使硫附着在烧瓶内壁形成一薄层膜,这样做的目的是
(4)实验时,如何防止E中液体挥发?
(5)画出虚线框内与F连接的仪器,并指出其中盛装试剂名称,以完善该实验装置。
23.(12分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

(1)试剂1是 ,试剂2是 ,加入新制氯水后溶液中发生的离子反应方程式是 , ;
(2)加入试剂2后溶液中颜色由淡黄色转变为淡红色的是因为 ;
(3)请解释加入新制氯水后颜色变深的原因
(4)该同学猜想血红色溶液变为无色溶液液的原因可能是:①溶液中的+3价铁被还原为+2价铁;② 。
22.(6分)常温下,向20 mL 氢氧化钠溶液中逐滴加入0.2 mol/L醋酸溶液,滴定曲线如下图所示:
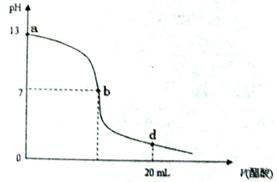
(1)该氢氧化钠溶液的物质的量浓度为 .
(2)在b点,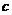 (Na
(Na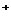 )
)
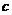 (CH3COO
(CH3COO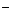 )(填”>”、“<”或“=”)
)(填”>”、“<”或“=”)
(3)氢氧化钠溶液与醋酸溶液恰好完全反应的点位于曲线的 (填选项的蝙号).
A.a点 B.b点 C.d点 D.a、b间的某点 E.b、d间的某点
21.(10分)下表给出了五种元素的相关信息,其中A、B、C、D、E为短周期元素。
|
元素 |
A |
B |
C |
D |
E |
|
相 关 信 息 |
在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料。 |
工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障。 |
植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂。 |
室温下其单质呈粉末状固体,加热易熔化。该单质在氧气中燃烧,发出明亮的蓝紫色火焰。 |
其单质不溶于冷的浓硝酸,它的氧化物是高熔点的固体,在熔融状态下可电解得到两种单质。 |
根据上述信息填空:
⑴ B在元素周期表中的位置是 ,画出D的原子结构示意图 。
⑵ 写出D的单质与烧碱水溶液加热反应的离子方程式 。
⑶ C与A形成的某一化合物能和C与B形成的另一化合物(这两种化合物分子中原子个数比皆为1:2)一起用作火箭助推剂,写出两者发生反应的化学方程式 。
⑷ E的单质可以在纯氧中燃烧,1molE的单质完全燃烧共放出a kJ的能量。试写出该反应的热化学方程式 。
⑸ E的单质不溶于冷的浓硝酸的原因是 。
20. 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g) 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
A.反应速率a>b>c
B.达到平衡时,AB3的物质的量大小为:c > b > a
C.若T2>T1,则正反应一定是放热反应
D.达到平衡时A2的转化率大小为:b>a>c
19.常温下,取物质的量浓度相等的NaOH溶液和HC1溶液,以2:1体积比相混合,所得溶液的pH等于12,则原溶液的物质的量浓度为
A.0.01mol/L B.0.02mol/L C.0.03mol/L D.0.04mol/L
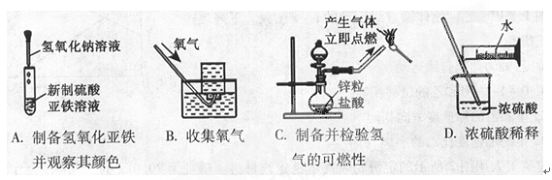
18.下列实验能达到实验目的且符合安全要求的是
17.试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是
①滴有石蕊的H2SO4溶液 ②滴有酚酞的氨水溶液
③滴有酚酞的氢氧化钠溶液 ④滴有酚酞的饱和氢氧化钙溶液
⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液
A.②⑥ B.②④ C.①③⑤ D.②④⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com