
2.正比例函数的图象经过(1,4)点,则此函数的解析式为________________
1.基本知识填空:
(1)、一般地,在求一个函数时,如果知道这个函数的一般形式,可以把所求的函数写为一般形式,其中___________________ ___,然后再根据题设条件求出这些待定系数,这种通过____________求___________来确定_____________的方法,叫待定系数法。
___,然后再根据题设条件求出这些待定系数,这种通过____________求___________来确定_____________的方法,叫待定系数法。
(2)、正比例函 数
数 的一般形式为_____________________,一次函数的一般形式为___________________________,二次函数的一般形式为__________________________.
的一般形式为_____________________,一次函数的一般形式为___________________________,二次函数的一般形式为__________________________.
2.二 次函数的解析式有哪些形式?
次函数的解析式有哪些形式?
[课前达标]
1.用待定系数法解题时,关键步骤是什么?
2.2.3 待定系数法 学案
[预习达标]
25.(10分)某化工厂以甲烷为原料合成早醇的反应为:
CH4(g) + H2O(g) → CO(g) + 3H2(g)…………………………①(反应中CH4的转化率:1)
CO(g) + 2H2(g) → CH3OH(g)………………………………②(反应中CO的转化率:2/3)
合成工艺如下(虚线框内为改进后的工艺中新增流程):


请回答下列问题(所有气体均折算成标准状况):
(1)原工艺中,当充入反应器①的甲烷和水蒸气的体积分别为672m3和1750m3时,最终反应剩余物中n(CO)=___________________,n(H2)___________________。
(2)为充分利用反应剩余物,该厂在原工艺的基础上,将下列反应运用于生产甲烷原料气:2CH4(g) + O2(g) → 2CO(g) + 4H2(g)………………③(反应中CH4的转化率:1)。若新工艺中充入反应器①的甲烷和水蒸气的体积分别为a、3a,反应剩余物中:V(H2)∶V(N2)∶V(CO)=3∶1∶1。试计算:
①充入反应器③的甲烷的体积为_______________。
②若富氧空气中除O2、N2外,其他成分忽略不计,则充入反应器③中的富氧空气的体积为________;应选择氧气的体积分数为_____________的富氧空气。
24.(10分)最近报道,在-100℃低温下合成了化合物X,元素分析仪得出其分子式为C5H4,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别没有区别,而碳的化学环境却有两种,温度升高将迅速分解,X的可能结构式是___________、_________、___________;如果分子中有三种环境不同的氢,有四种环境不同的碳,该烃可能的结构式为__________、___________;如果氢有两种环境,碳有四种环境,该烃可能的结构式为_____________、___________;如果氢有两种环境,碳有三种环境,该烃的结构简式可能为____________、______________、_______________。
23.(11分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染,这一材料是由我国某公司最新研发成功的新材料。PETG的结构简式为:


已知:Ⅰ: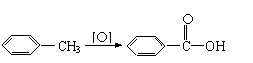

Ⅱ:RCOOR1 + R2OH → RCOOR3 + R1OH
试回答下列问题:
这种材料可采用下列合成路线:


(1) 反应②、⑥中加入的试剂X是__________________;
反应②、⑥中加入的试剂X是__________________;
(2)⑤的反应类型是________________;
(3)写出结构简式:B:___________________,I____________________________。
(4)写出化学方程式:
反应③__________________________________________________________________。
反应⑥__________________________________________________________________。
22.(8分)A、B、C、D分别代表硝酸银、偏铝酸钠、稀盐酸、浓氨水四种无色溶液中的一种。甲、乙两同学分别用两两混合的方法进行了如下图所示的实验,现象有的相同,有的不同,不同部分已标出。


(1)试写出A、B、D、C、D所代表物质的化学式:
A:______________,B______________;C________________;D______________。
(2)写出B和C按物质的量1∶3混合时反应的化学方程式:
______________________________________________________________________。
(3)写出A和D按物质的量之比为3∶1混合时反应的离子方程式:
_______________________________________________________________________。
21.(10分)1911年,Langmuir提出,电子数相同、原子数相同的分子,互称为等电子体。以后又发展成具有相同价电子(最外层电子)数和相同原子数的分子和离子也互称等电子体。X是一种新型无机材料,它与碳化硅(SiC)结构相似,物理性质相近,符合“等电子原理”。X有如下转化关系(图中部分反应的条件及部分生成物中的水已备去)。其中,C是一种能使温润的红色石蕊试纸变蓝的无色气体,D为白色胶状沉淀,E溶液的焰色反应呈黄色,M是一种常见金属,与L反应生成的Q溶液能鉴别酚类物质的存在。试回答问题:
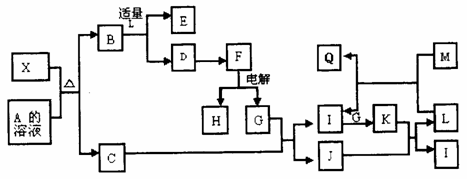
(1)M元素在周期表中的位置__________________。
(2)写出C的空间构型___________________。
(3)X属于_________晶体(填“分子”、“离子”或“离子”)
(4)①写出X与A溶液反应的离子方程式___________________________________。
⑤写出C与G反应的化学方程式________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com