
25、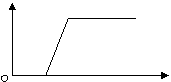 (唐店中学2009学年九年级第三次月考化学试题)
(唐店中学2009学年九年级第三次月考化学试题)
把10g铁和铜的混合物放入盛有47.3g稀硫酸的烧杯中,恰好完全反应,烧杯中物质的总质量比反应前铁和铜的混合物与稀硫酸的总质量减少了0.10g。
(1)原混合物中铜的质量?
(2)反应后所得溶液中溶质质量分数?
24. (2009年山东省枣庄市五校联考试题)下表中选项与图中所示曲线符合的是( )
|
选项 |
横坐标 |
纵坐标 |
|
A |
向一定量稀硫酸中加入锌粉的质量 |
产生氢气的体积 |
|
B |
向一定量硫酸和硫酸铜混合溶液中加入氢氧化钠溶液的质量 |
产生沉淀的质量 |
|
C |
一定量的铜粉在空气中加热的时间 |
反应后固体的总质量 |
|
D |
在一定温度下,向一定量的水中加入食盐晶体的质量 |
溶液中溶质的质量分数 |
23、(吉林省实验中学初三年级第六次月考)
请根据化学方程式计算:完全分解340g溶质质量分数为10﹪的过氧化氢溶液中的过氧化氢(H2O2),最多可生成多少克氧气?
22.(2009年山东省滨州市邹平县五校联合第一次模拟试题)(6分)张玲同学为了测定汉白玉中碳酸钙的质量分数, 称取 5.55g 研碎的汉白玉粉末,进行四次高温加热(杂质不参加反应)、冷却、称量剩余固体的重复操作。记录数据如下:
|
操作次序 |
第一次 |
第二次 |
第三次 |
第四次 |
|
剩余固体质量(g) |
4.25 |
3.95 |
3.35 |
3.35 |
请计算:
(1)完全反应后生成二氧化碳________________________g。
(2)求汉白玉中碳酸钙的质量分数。
21.(湖北省大冶市2009年中考调研考试化学试卷)(6分)鸡蛋壳的主要成分是碳酸钙。为了测定某鸡蛋壳中碳酸钙的质量分数,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10 g 放在烧杯里,然后往烧杯中加入足量的稀盐酸90 g,充分反应后,称得反应剩余物为97.14 g 。(假设其他物质不与盐酸反应)
(1)产生二氧化碳气体 g。
(2)计算该鸡蛋壳中碳酸钙的质量分数。
20.(广州十四中2008-2009学年第一学期12月月考)(3分)新研制成的一种分子结构类似足球状的物质,其化学式为C60,它的一个分子含有 个原子,属于 (填“单质”或“化合物”),相对分子质量是 。(7分)
(1)求碳酸钙中钙元素的质量分数。
(2)工业上通过煅烧石灰石来制取二氧化碳。如果制取88千克二氧化碳,至少需
 要多少碳酸钙?
要多少碳酸钙?
19. (常州市礼河实验学校调研测试试卷)(3分)消化药片所含的物质能中和胃里过多的胃酸。 某种消化药片的标记如图。医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次2片。试计算,患者按处方服用该药片一天,理论上可以中和HCl多少毫克?
(常州市礼河实验学校调研测试试卷)(3分)消化药片所含的物质能中和胃里过多的胃酸。 某种消化药片的标记如图。医生给某胃酸过多的患者开出服用此药的处方为:每日三次,每次2片。试计算,患者按处方服用该药片一天,理论上可以中和HCl多少毫克?
18.(常州市礼河实验学校调研测试试卷)(5分)某课外兴趣小组对一批铁样品(含有杂质,杂质不溶于水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中只有一位同学所取用的稀硫酸与铁样品恰好完全反应。实验数据如下表:
|
|
甲 |
乙 |
丙 |
|
烧杯+稀硫酸 |
250g |
200g |
200g |
|
加入的铁样品 |
9g |
9g |
14g |
|
充分反应后,烧杯+剩余物 |
258.7g |
208.7g |
213.7g |
请你认真分析数据,回答下列问题:(烧杯的质量为75.4g;计算结果精确到1%)
(1) 同学所取用的稀硫酸与铁样品恰好完全反应;
(2)计算样品中铁的质量分数;
(3)所用稀硫酸的溶质质量分数。
17.(2009年淄博怡中外语学校迎中考试题一)(3分) 晴晴同学为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体2.2g。试计算:
(1)该石灰石样品中碳酸钙的质量分数为多少?(写出计算过程)
(2)若要计算上述反应所消耗盐酸溶液的质量,题中还缺少的一个数据是 。
16、(2009年中考模拟测试题二)我国大约在南北朝时就能铸造铜锌合金--黄铜。某兴趣小组为了测定得到的黄铜样品中铜的含量,称取20g样品于烧杯中(烧杯质量为Bg),加入50g稀硫酸,恰好完全反应后,冷却,称得烧杯的总质量为Bg+69.8g。请计算(精确到0.1%):
⑴此黄铜中铜的质量分数;
⑵所得溶液的溶质质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com