
12.下列离子方程式正确的是 ( )
A.将氯气通入水中:Cl2+H2O=Cl-+HClO+H+
B.常温下Al与浓硝酸反应:Al+6 H++3NO- 3=Al3++3NO2↑+3 H2O
C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H++I-=Fe2++I2+3 H2O
D.次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
11.设NA为阿伏加德罗常数,下列说法正确的是 ( )
A.在含4molSi-O键的SiO2晶体中,氧原子的数目为4NA
B.标准状况下,等物质的量的NH3和SO3所含原子数都相等
C.12.5mL16mol/L浓硫酸与足量的铜反应,生成SO2的分子数约为6.02×1022
D.常温下含有NA个NO2、N2O4分子的混合气体,降温至标准状况下,其体积约为22.4L
10.废旧的电池不可以随意丢弃,某同学希望将废旧的电池回收利用,他的以下想法不正确的是 ( )
A.把锌皮取下洗净用于实验室制取氢气
B.碳棒取下洗净用作电极
C.把铜帽取下洗净回收利用
D.废电池中的黑色糊状物含有氯化铵等物质,可作化肥
9.恒温25℃时,将两铂电极插入一定量硫酸钠饱和溶液中进行电解。通电一段时间后,阳极析出了a mol气体,同时有ωg Na2SO4·10H2O晶体析出。剩余溶液中溶质的质量分数为( )
A. ×100% B.
×100% B.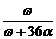 ×100% C.
×100% C. D.
D.

8.下列对实验现象的解释与结论正确的是 ( )
|
编号 |
实验操作 |
实验现象 |
解释与结论 |
|
A |
向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液 |
有白色沉淀产生 |
蛋白质发生了变性 |
|
B |
向某溶液中加入BaCl2溶液 |
有白色沉淀产生 |
生成难溶于水的BaSO4,该溶液中一定含有SO42- |
|
C |
向甲苯中滴入少量浓溴水,振荡,静置 |
溶液分层,上层呈橙红色,下层几乎无色 |
甲苯和溴水发生取代反应,使溴水褪色 |
|
D |
向蔗糖中加入浓硫酸 |
变黑,放热,体积膨胀,放出刺激性气体 |
浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
7.下列离子方程式书写不正确的是 ( )
A.NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性
2H+ + SO42- + Ba2+ + 2OHOHOHOH- = BaSO4↓+ 2H2O
B.将标准状况下112 mL氯气通入10 mL 1 mol·L-1的溴化亚铁溶液中
2Fe2+ + 4Br-+ 3Cl2 = 2Fe3+ + 6Cl- + 2Br2
C.碳酸氢铵溶液中加入足量NaOH溶液
NH4++ HCO3-+2OH- = CO32-+NH3·H2O+H2O
D.向澄清石灰水中加入过量的碳酸氢钠溶液
Ca2+ + 2OHOHOHOH- + 2HCO3-= CaCO3↓ + 2H2O + CO32-
6.下列各组离子:(1) I-、ClO-、NO3-、Cl-; (2) K+、H+、NO3-、Cl-;
(3)SO32-、S2-、Cl-、OH-; (4)Mg2+、Cu2+、SO42-、Cl-; (5)Fe3+、SCN-、K+、SO42-;
(6)K+、HPO42-、PO43-、HSO3- 。在溶液中能大量共存的组别共有 ( )
A.1组 B.2组 C.3组 D.不少于4组
5.常温下,有甲、乙两份体积均为1L,pH均为3的溶液,其中甲为醋酸,乙为盐酸。①甲用蒸馏水稀释至100倍后,溶液的pH变为a;②乙与等体积、浓度为0.01mol/L的氨水混合,在此混合液中:n(NH4+)+n(H+)-n(OH-)= bmol。则a、b正确的答案组合是 ( )
A.3~5之间;0.0005 B.3~5之间;0.001
C.5;0.0005 D.5;0.001
4.用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.32g氧气和臭氧的混合气体中含有的氧原子数为2NA
B.标准状况下,22.4LCH3CH2Br中所含分子数为NA
C.0.1molH3O+所含质子数为NA
D.0.1molFe和足量的稀硝酸充分反应,转移电子数为0.2 NA
3.下列各组离子中,加入盐酸或NaOH溶液都能大量共存的离子组是 ( )
A.Al3+、K+、HC 、
、 B. Na+、Cl-、SO42- 、
B. Na+、Cl-、SO42- 、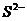
C.Na+ 、 、
、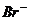 、
、 D.Na+ 、K+、Fe2+、NO3-
D.Na+ 、K+、Fe2+、NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com