
11、①K= ,②K=
,②K=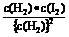 ,③K=c(CO2),④K=
,③K=c(CO2),④K=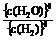
14.在一定温度下的密闭容器中存在如下反应:2SO2(g)+ O2 (g)  2SO3(g),已知
2SO3(g),已知
c始(SO2)=0.4 mol·Lˉ1,c始(O2)=1 mol·Lˉ1,经测定该反应在该温度下的平衡常数K=19。试判断:
(1)当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?
(2)达到状态时,SO2的转化率为多少?
13、在一定体积的密闭容器中,进行如下化学反应:
CO2(g) + H2(g) CO(g) + H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g) + H2O(g),其化学平衡常数K和温度t的关系如下表:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1) 能判断该反应是否达到化学平衡状态的依据是 。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(2) 某温度下,平衡浓度符合下式 : c(CO2)·c(H2)=c(CO)·c(H2O), 试判断此时的温度为 ℃。
12、高炉炼铁中发生的基本反应之一如下: FeO(s)+CO(g)  Fe(s)+CO2(g) △H<
0。
Fe(s)+CO2(g) △H<
0。
已知1100℃时平衡常数K=0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值____,平衡常数K值_____(本小题空格均备选:增大、减小或不变)
(2)1100℃时测得高炉中c(CO2)=0.025 mol·Lˉ1,c(CO)=0.1 mol·Lˉ1,在这种情况下,该反应是否处于化学平衡状态__ _(选填“是”或“否”),此时,化学反应速率是υ(正)__ _υ(逆)(选填大于、小于或等于),其原因是____ __。
11、写出下列反应的平衡常数的表达式
 ①PCl5(g) PCl3(g)+Cl2(g) ____________________________________
①PCl5(g) PCl3(g)+Cl2(g) ____________________________________
 ②2HI(g) H2(g)+I2(g)
____________________________________
②2HI(g) H2(g)+I2(g)
____________________________________
 ③CaCO3(s) CaO(s)+CO2(g) ____________________________________
③CaCO3(s) CaO(s)+CO2(g) ____________________________________
 ④Fe3O4(s)+4H2(g) 3Fe(s)+4H2O(g)
____________________________________
④Fe3O4(s)+4H2(g) 3Fe(s)+4H2O(g)
____________________________________
11.一定条件下,可逆反应X(g)+3Y(g)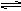 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1 mol·Lˉ1,0.3
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1 mol·Lˉ1,0.3
mol·Lˉ1,0.08 mol·Lˉ1,则下列判断不合理的是
A.c1∶c2=1∶3 B.平衡时,Y和Z的生成速率之比为3∶2
C.X、Y的转化率不相等 D.c1的取值范围为0< c1<0.14 mol·Lˉ1
10.在1 L密闭容器中,把1 mol A和1 mol B混合发生如下反应:
3A(g)+B(g) xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol·Lˉ1,下列叙述中不正确的是
xC(g)+2D(g),当反应达到平衡时,生成0.4 mol D,并测得C的平衡浓度为0.4 mol·Lˉ1,下列叙述中不正确的是
A.x的值为2 B.A的转化率为40%
C.B的平衡浓度为0.8 mol·Lˉ1 D.D的体积分数为25%
9.已知NH3·H2O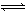 NH4+
+ OHˉ的K=1.76×10ˉ5,则0.1 mol·Lˉ1NH3·H2O溶液中OHˉ的浓度是
NH4+
+ OHˉ的K=1.76×10ˉ5,则0.1 mol·Lˉ1NH3·H2O溶液中OHˉ的浓度是
A.1.80×10ˉ6 B.1.32×10ˉ3 C.4.20×10ˉ3 D.5.00×10ˉ2
8.一定温度下将1 mol SO3 放入1L的反应器内,当反应:
2SO3(g)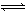 2SO2(g)+O2(g)
平衡时,容器内有0.6 molSO2,其平衡常数是
2SO2(g)+O2(g)
平衡时,容器内有0.6 molSO2,其平衡常数是
A.0.36 B.0.68 C.0.45 D.0.47
7.已知反应nA  An的平衡常数为K,则有1/2An
An的平衡常数为K,则有1/2An 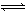 1/2nA的平衡常数是
1/2nA的平衡常数是
A.K B.K1/2 C.K2 D.Kˉ2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com