
4.(2010届广西禾池中学高三上学期第一次月考)(8分)在浓硝酸中放入铜片:
(1)若铜有剩余,则反应将要结束时的主要反应方程式是 。
(2)若反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是 。
(3)1L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.2mol/L和0.1mol/L。若向该混合液中加入9.6g铜粉,充分反应后,能产生标准状况下的气体多少L?
答案 (1)3Cu+8HNO3(稀)=3Cu(NO3)+2NO↑+4H2O 。
(2) H2SO4提供H+,NO3?继续与Cu发生反应: 3Cu+8H++2NO3?====3Cu2++2NO↑+4H2O(意思答对即可)。
(3)2.24L
3.(2010届广西禾池中学高三上学期第一次月考)(6分)已知A、B、C、D、E、F是含有同一种元素的化合物,其中A是一种日常生活中不常见的红棕色气体,F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应:
A + H2O → B + C C + F → D D + NaOH F + E + H2O
F + E + H2O
(1)写出它们的化学式:
A 、C 、F ;
(2)写出A + H2O → B + C的离子方程式,并指反应的氧化剂
,氧化剂
答案 ( 每空1分,方程式2分)
(1)A NO2 、C HNO3 、F NH3 ;
(2
3NO2+H2O=2H++2NO3-+NO ,氧化剂 NO2
2、(6分)(2010届广西禾池中学高三上学期第一次月考)氨(NH3)是重要的含氮化合物。1774年该气体由英国普里斯特里制得。为了在实验室制取干燥的氨气,甲、乙、丙三位同学分别设计了如下三套实验装置:
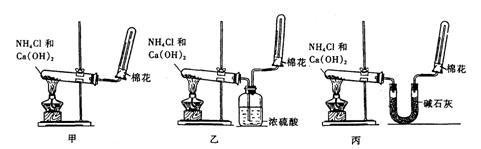
(1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) ;
(2)写出实验室制取氨气的化学方程式 ;
(3)该实验装置与实验室制备 气的装置相同;
答案 (1)实验装置和所用药品都正确的是(填“甲”、“乙”或“丙”) “丙” ;
(2)写出实验室制取氨气的化学方程式 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O ;
2NH3↑+CaCl2+2H2O ;
(3)该实验装置与实验室制备 氧 气的装置相同;
1.(贵州省大厂中学2010届高三10月月考) 工业合成氨与制备硝酸一般可连续生产,流程如下:

(1)某温度下体积为200L的氨合成塔中,测得如下数据:
 |
0 |
1 |
2 |
3 |
4 |
|
N2 |
1.500 |
1.400 |
1.200 |
C1 |
C1 |
|
H2 |
4.500 |
4.200 |
3.600 |
C2 |
C2 |
|
NH3 |
0 |
0.200 |
0.600 |
C3 |
C3 |
根
据表中数据计算0-2小时内N2的平均反应速率 mol·L-1·h-1
若起始时与平衡时的压强之比为a,则N2的转化率为 (用含a的代数式表示)
(2)希腊阿里斯多德大学的 George Marnellos
 和 Michael Stoukides,发明了一种合成氨的新
和 Michael Stoukides,发明了一种合成氨的新
方法(Science,2,Oct.1998, p98),在常压下,
把氢气和用氦气稀释的氮气分别通入一个加热到
570℃的电解池,利用能通过氢离子的多孔陶瓷固
体作电解质,氢气和氮气在电极上合成了氨,转化
率达到78%,试写出电解池阴极的电极反应
式
(3)氨气和氧气从145℃就开始反应,在不同温度
和催化剂条件下生成不同产物(如右图):
4NH3+5O2 4NO+6H2O
K1=1×1053(900℃)
4NO+6H2O
K1=1×1053(900℃)
4NH3+3O2 2N2+6H2O K2=1×1067(900℃)温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 。吸收塔中需要补充空气的原因 。
2N2+6H2O K2=1×1067(900℃)温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因 。吸收塔中需要补充空气的原因 。
(4)尾气处理时小型化工厂常用尿素作为氮氧化物的吸收剂,此法运行费用低,吸收效果好,不产生二次污染,吸收后尾气中NOx的去除率高达99.95%。其主要的反应为氮氧化物混合气与水反应生成亚硝酸,亚硝酸再与尿素反应生成CO2 和N2请写出有关反应化学方程式 , 。
答案(1)0.15 2(1-1/a) (2)N2+6e-+6H+=2NH3
(3)N2 生成NO的反应为放热反应,升高温度转化率下降
进一步与NO反应生成硝酸
(4) NO+NO2+H2O=2HNO2; CO (NH2)2+2HNO2=CO2+2N2+3H2O
14. (云南省玉溪一中2010届高三上学期期中)叠氮酸(HN3)与醋酸酸性相近,其盐稳定,但撞击时会发生爆炸生成氮气。有关叠氮酸的叙述中正确的是( )
①NaN3 的水溶液呈碱性 ② HN3 的固体属于共价化合物
③NaN3的固体属于离子化合物 ④NaN3可用于小汽车防撞保护气囊
A、①②③ B、②③④ C、①③④ D、①②③④
答案 D
13. (辽宁省东北育才中学2010届高三第二次模拟考试)已知 与足量的2mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是( )
与足量的2mol/L硫酸液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是( )
A.反应中硫酸作氧化剂
B. 中硫元素被氧化
中硫元素被氧化
C.1mol 完全反应转移0.5mol电子
完全反应转移0.5mol电子
D.刺激性气味的气体是氨气
答案 C
12. (山东师大附中高三第一次模拟考试)固体A的化学式为NH5,它的所有原子的电子层结构都跟该原子同周期的稀有气体原子一样,NH5能跟水反应,化学方程式为:NH5+H2O=NH3·H2O+H2↑。则下列说法中,不正确的是
A.1molNH5中有5NA个N-H键(NA为阿伏加德罗常数的值)
B.NH5中既有共价键,又有离子键,属于离子化合物
C.NH5跟水的反应是氧化还原反应
D.NH5跟水的反应中,H2既是氧化产物又是还原产物
答案 A
11. (河南焦作十一中2010届高三上学期期中考试)在标准状况下,由NO、NO2、O2组成的混合气体充满于一个烧瓶中,将烧瓶倒立于水槽里则水全充满,设若无气体溢出也无溶质扩散于烧瓶外的水槽里,烧瓶内溶液的物质的量浓度(C)范围正确的是
(A)0<C<1/22.4 (B)1/39.2<C<1/28
(C)1/28<C<1/22.4 (D)1/39.2<C<1/22.4
答案 B
9. (河北省冀州中学2010届高三上学期期中考试).叠氮酸钠(NaN3)是抗禽流感药物“达菲”合成过程中的中间活性物质,3mol
NaN3受撞击会生成4mol 氮气和离子化合物(Na3N)。下列有关叙述错误的是( )
A.NaN3受撞击时,既是氧化剂又是还原剂 B.NaN3跟水反应时,有NH3生成
C.Na3N中N3-半径比Na+半径大 D.NaN3中,既存在离子键又存在非极性共价键
答案 B
10 (辽宁省东北育才中学2010届高三第二次模拟考试)已知磷酸分子 中,三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能再跟D2O发生氢交换。由此可知次磷酸的分子结构为
( )
中,三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能再跟D2O发生氢交换。由此可知次磷酸的分子结构为
( )

答案 B
8. (湖北省孝感高中2010届高三上学期综合测试)如图在同温同压下,两个等体积的干燥圆底烧瓶中分别充满:①NH3 ②NO2进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度的比较关系为( )
 A.①>②
A.①>②
B.①=②
C.①<②
D.不能确定
答案 B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com