
5.下列说法正确的是 ( )
A.构成单质分子的粒子一定含共价键
B.分子中非直接相邻的原子间也可形成化学键
C.两种不同非金属元素一定形成极性键
D.非极性键只存在双原子单质分子里
4.下列性质中可以证明某化合物内一定存在离子键的是 ( )
A.可溶于水 B.具有较高的熔点
C.水溶液能导电 D.熔融状态能导电
3.若短周期元素可以形成X2Y3分子,则这两种元素的原子序数之差不可能是 ( )
A.1 B.3 C.5 D.6
2.某元素R的阴离子R2-核外共有a个电子,核内有b个中子,则表示R原子组成符号正确的是 ( )
A. R B.
R B.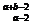 R
C.
R
C. R
D.
R
D.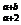 R
R
1.相对原子质量为X的原子实际质量是 ( )
A.X
B.X g
C. D.
D.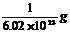
22.取5.4g由碱金属R及其氧化物R2O组成的混合物,使之与足量的水反应,蒸发反应后溶液得到8.0g无水晶体。
(1)判断该金属是哪一种碱金属?
(2)原混合物中R及R2O的质量各是多少?
21.将Na2CO3、NaHCO3的混合物1.9g,强热至无气体出现为止,恢复至原来状态,称量剩余物的质量减轻了0.31g,求原混合物中NaHCO3质量分数。
20.将a g钠溶于b g水中,a1 gNa2O溶于b1 g水中,a2 gNa2O2溶于b2 g水中,均得溶质质量分数为8%的溶液。
(1)若a1:a2=31:39,则b1:b2= 。
(2)若a为4.6,则b= 。
19.填表:
|
实验操作 |
实验现象 |
离子反应方程式 |
|
一小块钠投入FeCl3 溶液中 |
|
|
|
碳酸钠与醋酸溶液 混合 |
|
|
|
盐酸加入KHCO3 溶液中 |
|
|
|
澄清石灰水加入 NaHCO3溶液中 |
|
|
18.一定质量的Na2CO3和NaHCO3混合物共热,反应前Na2CO3在混合物中的质量分数为55.7%,当Na2CO3的含量提高到70%时,NaHCO3约分解了( )
A.20% B.36% C.42% D.50%
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com