
8.(安徽省白云中学09高三化学综合训练) 进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习方法之一。下列对有关实验事实的解释正确的是
A.溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性
B.用惰性电极电解相同浓度的Cu(NO3)2和AgNO3混合溶液,阴极首先析出的是Ag,说明Ag+的还原性比Cu2+ 强
C.常温下,将铝片放入浓硫酸中无明显现象,说明铝不和冷的浓硫酸反应
D.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
7.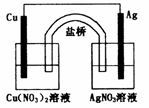 (重庆市高2009级学生学业质量调研抽理综)用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂一KNO3的U型管)构成-个原电池(如图)。以下有关该原电池的叙述正确的是
(重庆市高2009级学生学业质量调研抽理综)用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂一KNO3的U型管)构成-个原电池(如图)。以下有关该原电池的叙述正确的是
①在外电路中,电流由铜电极流向银电极
②正极反应为:Ag+ + e- = Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
A.①② D.②③ C②④ D.③④
6.(天津市2008-2009学年度第四次月考)用酸性氢氧燃料电池电解苦卤水 (含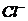 、
、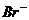 、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是
、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是
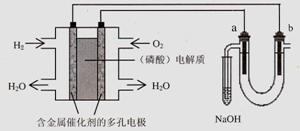
A.电池工作时,正极反应式为:O2 +2 H2O + 4e-=4 OH―
B.电解时,a 电极周围首先放电的是Br―而不是Cl―,说明当其它条件相同时前者的还原性强于后者
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗0.02g H2 时,b 极周围会产生0.02g H2
5.(天津市汉沽一中2009第五次月考化学)在25ºC时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有a mol电子转移时,溶液中析出mg Na2SO4 ·10 H2 O晶体。若温度不变,在剩余溶液中溶质的质量分数为( )
A.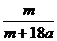 ×100%
B.
×100%
B.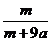 ×100%
×100%
C.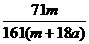 ×100%
D.
×100%
D.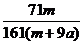 ×100%
×100%
4.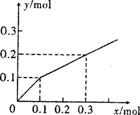 (2009届湖北省武汉市高中毕业生调研) 以Pt为电极,电解含有0.10mol M+和0.10mol N3+
(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如右图。对离子氧化能力的强弱判断正确的是(选项中H+为氢离子)
(2009届湖北省武汉市高中毕业生调研) 以Pt为电极,电解含有0.10mol M+和0.10mol N3+
(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如右图。对离子氧化能力的强弱判断正确的是(选项中H+为氢离子)
A.M+ > H+ > N3+
B.M+ >N3+ > H+
C.N3+ >H+ > M+
D.条件不足,无法确定
3. 用惰性电极电解硫酸铜溶液,当加入0.1mol Cu(OH)2使溶液恢复原来的浓度和pH时,电极上转移电子的物质的量是 ( )
A.0.1mol B.0.2mol
C.0.3mol D.0.4mol
2. 下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
下图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
A.该能量转化系统中的水也是可以循环的
B.燃料电池系统产生的能量实际上来自于水
C.水电解系统中的阳极反应:4OH--4e-=2H2O+O2↑
D.燃料电池放电时的负极反应:H2-2e-+2OH-=2H2O
例15.(09广东化学14)可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH
溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4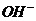
B.以NaOH溶液为电解液时,负极反应为:Al+3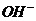 -3e-=Al(OH)3↓
-3e-=Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
[解析]电解质溶液显碱性或中性, 该燃料电极的正极发生反应为:O2+2H2O+4e-=4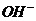 ,A对;铝作负极,负极反应应该是铝失去电子变为铝离子,在氢氧化钠的溶液中铝离子继续与过量的碱反应生成偏铝酸根,因此负极反应为:Al+4
,A对;铝作负极,负极反应应该是铝失去电子变为铝离子,在氢氧化钠的溶液中铝离子继续与过量的碱反应生成偏铝酸根,因此负极反应为:Al+4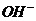 -3e=
-3e=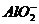 + 2H2O,B错; 该电池在碱性条件下消耗了碱,反应式为4Al+3O2+4
+ 2H2O,B错; 该电池在碱性条件下消耗了碱,反应式为4Al+3O2+4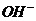 = 4
= 4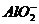 + 2H2O溶液PH降低,C错;电池工作时,电子从负极出来经过外电路流到正极,D错高
+ 2H2O溶液PH降低,C错;电池工作时,电子从负极出来经过外电路流到正极,D错高
[答案]A
例16.(09年浙江卷)市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li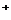 的高分子材料。这种锂离子电池的电池反应为: Li+2Li
的高分子材料。这种锂离子电池的电池反应为: Li+2Li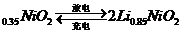
下列说法不正确的是
A.放电时,负极的电极反应式:Li-e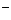 =Li
=Li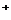
B.充电时,Li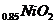 既发生氧化反应又发生还原反应
既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li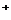 向负极移动
向负极移动
[解析]A项,Li从零价升至正价,失去电子,作为负极,正确;B项,反应逆向进行时。反应物只有一种,故化合价既有升,又有降,所以既发生氧化反应又发生还原反应,正确;C项,由于Li可以与水反应,故应为非水材料,正确;D项,原电池中阳离子应迁移至正极失电子,故错。
[答案]D
例17.(09年山东卷)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是 。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 。
[解析](1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+ 置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
[答案]
(1)Zn(或锌) 正极 (2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀
b (3)2H++2e-→H2 ,87g
[专题突破]
1.(长春市实验中学2009届高三理科综合)钢铁在潮湿的空气中会被腐蚀,发生的原电池反应:2Fe+2H2O+O2  2Fe2++4OH-。以下说法正确的是
( )
2Fe2++4OH-。以下说法正确的是
( )
A.负极发生的反应为:Fe-2e- Fe2+
Fe2+
B.正极发生的反应为:2H2O+O2+2e- 4OH-
4OH-
C.原电池是将电能转变为化学能的装置
D.钢柱在水下部分比在空气与水交界处更容易腐蚀
例13. 将两个铂电极插入500mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为
A.4×10-3mol/L B.2×10-3mol/L C.1×10-3mol/L D.1×10-7mol/L
[解析]根据电解规律可知阴极反应:Cu2++2e-=Cu,增重0.064gCu,应是Cu的质量,根据总反应方程式:
2CuSO4+2H2O 2Cu+O2↑+2H2SO4--->4H+
2Cu+O2↑+2H2SO4--->4H+
2×64g 4mol
0.064g x
x=0.002mol
[H+]=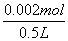 =4×10-3mol/L
=4×10-3mol/L
[答案]A
例14.(2009届福建省泉州市俊来中学高三年级月考化学)电解100mL含c(H+)=0.30mol/L
的下列溶液。当电路中通过0.04mol电子时,理论上析出金属质量最大的是
A.0.10mol/L Ag+ B.0.20mol/L Zn2+ C.0.20mol/L Cu2+ D.0.20mol/L Pb2+
[解析]电解时阴极上溶液中离子的反应顺序为Ag+ >Cu2+ >H+ >Pb2+ >Zn2+ ,
A项中Ag+ 先反应,H+后反应,可得到Ag:0.10mol/L×0.1L×108g/mol=1.08g ;H2 :0.03g 。
B项中H+先反应,Zn2+后反应,可得H2:0.03g ;Zn:(0.04mol-0.03mol)÷2×65g/mol=0.325g 。
C项中Cu2+先反应,H+后反应,可得到Cu:0.02mol/L×0.1L×64g/mol=1.28g 。D项中H+先反应,Pb 2+后反应,可得到H2:0.03g ;Pb:(0.04mol-0.03mol)÷2×207g/mol=1.05g 。
因此理论上析出金属质量最大的是C。
[答案]C
例11.银器皿日久表面逐渐变黑色,这是由于生成硫化银,有人设计用原电池原理加以除去,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银不会损失。试回答:在此原电池反应中,负极发生的反应为________;正极发生的反应为_________;反应过程中产生有臭鸡蛋气味的气体,则原电池总反应方程式为___________________________。
[解析]要善于抓住题示信息,“黑色褪去而银不会损失”,必然发生变化:Ag2S Ag,
Ag,
显然这是原电池的正极反应,Ag2S+2e-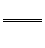 2Ag+S2-,负极反应为活泼金属发生氧化反应:Al-3e-
2Ag+S2-,负极反应为活泼金属发生氧化反应:Al-3e-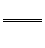 Al3+。正极生成的S2-和负极生成的Al3+在溶液中发生双水解:2Al3++3S2-+6H2O
Al3+。正极生成的S2-和负极生成的Al3+在溶液中发生双水解:2Al3++3S2-+6H2O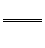 2Al(OH)3↓+3H2S↑,与题意产生臭鸡蛋气味的气体相吻合。原电池的总反应为上述三个反应的加合:3Ag2S+2Al+6H2O
2Al(OH)3↓+3H2S↑,与题意产生臭鸡蛋气味的气体相吻合。原电池的总反应为上述三个反应的加合:3Ag2S+2Al+6H2O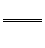 6Ag+2Al(OH)3↓+3H2S↑。
6Ag+2Al(OH)3↓+3H2S↑。
[答案]Al-3e-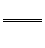 Al3+ Ag2S+2e-
Al3+ Ag2S+2e- 2Ag+S2-
2Ag+S2-
3Ag2S+2Al+6H2O 6Ag+2Al(OH)3↓+3H2S↑
6Ag+2Al(OH)3↓+3H2S↑
例12.钢铁在很弱的酸性或中性条件下发生电化学腐蚀时,正极的反应式为 ( )
A.Fe-2e- Fe2+
B.2H++2e-
Fe2+
B.2H++2e- H2↑
H2↑
C.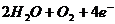
 4
4 D.Fe-3e-
D.Fe-3e- Fe3+
Fe3+
[解析]钢铁中含有多种杂质,在考虑钢铁的电化学腐蚀时,为了简化问题,主要讨论碳杂质问题。也就是以Fe为负极,C为正极的原电池反应。在中性条件或弱酸性条件下发生的是吸氧腐蚀。原电池的正极为C,发生的是还原反应,即得电子反应,故A、D选项应排除。在B、C选项中,B项是析氢腐蚀的电极反应式
[答案]C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com