
2、方程x3+2x2+3x-4=0有一个近似根在下列哪个区间内( )
A.(0,1) B.(1,2) C.(2,3) D.(3,4)
1、下列特征数一定是数据组中数据的是( )
A.众数 B.中位数 C.标准差 D.平均数
21.(6分)解:在A池中发生的反应为:
阳极(②极):4OH-- 4e-=2H2O+O2↑
阴极(①极):2Cu2++4e-=2Cu
若Cu2+完全放电后还有:4H++4e-=2H2↑ 转移电子的物质的量为:2.16÷108=0.02(mol)
由电极反应可知,每转移4mol电子,放出1molO2,所以②极上析出O2的体积为: 0.02÷4×22 .4=0.112(L)<0.224(L)
.4=0.112(L)<0.224(L)
说明A池收集到的气体中还有H2。①极上放出H2为:0.224-0.112=0.112(L),即0.005mol。
①极上析出Cu和放出H2共获得0.02mol电子。
Cu2+的物质的量为:(0.02-0.005×2)/2=0.005(mol)[Cu2+]= 0.005/0.2=0.025(mol/L) 答:通电前A池中原混合溶液Cu2+的浓度为0.025mol/L。
0.005/0.2=0.025(mol/L) 答:通电前A池中原混合溶液Cu2+的浓度为0.025mol/L。
20.(11分)
(1)锂(1分) 4Li-4e-=4Li+(2分)
(2)2SO Cl2+4e-=4Cl-+S+SO2(2分)
Cl2+4e-=4Cl-+S+SO2(2分)
(3)出现白雾,有刺激性气体生成(2分) SOCl2+H2O=SO2↑+2HCl↑(2分)
(4)锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应(2分)
19.(11分)
(1)、正极(1分),铜(1分)(2)、3.85x103 C(3分)4OH--4 e-=O2↑+2H2O(2分),4Ag++4e-=4Ag(2分),PH=1(2分)
e-=O2↑+2H2O(2分),4Ag++4e-=4Ag(2分),PH=1(2分)
18. (11分)
(1)原电池(1分) 电解池(1分)
(2)负(1分)
Fe - 2e- == Fe2+ (2分) 无色溶液变红色(2分)
(2分) 无色溶液变红色(2分)
(3)减少 5.6 (2分) 减少 0.8(2分)
16. (5分)(1)④>②>①>③(2分)
(5分)(1)④>②>①>③(2分)
(2)2N2H4(g) + 2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7kJ/mol(3分)
1 7.(11分)(1)、ΔH4= -339.2 kJ/mol(3分)
7.(11分)(1)、ΔH4= -339.2 kJ/mol(3分)
(2)、负极:Cd-2e-+2OH- =Cd(OH)2(2分)
正极:2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-(2分)
阳极:2Ni(OH)2+2OH--2e-=2NiO(OH)+2H2O(2分)
阴极:Cd(OH)2+2e- =Cd+2OH- (2分)
21.如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL,求通电前A池中原混合溶液Cu2+的浓度。

20.Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S +SO2。
请回答下列问题:
(1)电池的负极材料为 ,发生的电极反应为 ;
(2)电池正极发生的电极反应为 ;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 ;
(4)组装该电池必须在无水、无氧的条件下进行,原因是 。
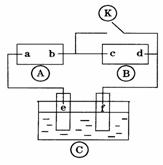
19.下图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,
 为电镀槽.断开
为电镀槽.断开 ,接通电路后发现
,接通电路后发现 上的c点显红色.为实现铁上镀铜,接通
上的c点显红色.为实现铁上镀铜,接通 后,使c、d两点短路.
后,使c、d两点短路.
(1)a极为 e极连接的电极材料为
(2)若通电一段时间后,铁上质量增加1.28g,则电源提供的电量为 库仑?( 每个
每个 电子所带电量为1.6x10-19C,保留两位小数点)
电子所带电量为1.6x10-19C,保留两位小数点)
 (3)若
(3)若 中两极为石墨电极,电解液为400ml的AgNO3溶液,则e,f两极的电极反应式分别为
,
中两极为石墨电极,电解液为400ml的AgNO3溶液,则e,f两极的电极反应式分别为
,
通过和(2)相同的电量后溶液的PH为 (假设电解后溶液体积不变,PH= -lgc(H+) )
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com