
13. 3.9g镁铝合金恰好完全溶解于120mL4mol/L的盐酸中,再加入60mL8mol/L的氢氧化钠溶液,得到沉淀10.7g,则加入盐酸时产生氢气的物质的量为(mol)
A 0.17 B 0.18 C 0.20 D 0.21 ( )
12.下列说法不正确的是( )
A.向碳酸钠溶液中通入二氧化碳可能会有晶体析出
B.一定温度下的不饱和硫酸铜溶液中加入足量的无水硫酸铜粉末,也不一定能得到饱和溶液
C.二氧化碳虽可以灭火,但镁能在其中燃烧
D.因为氢氧化铁胶体带正电荷,所以电泳实验时阴极颜色加深
11.把一定质量Na2CO3、NaHCO3、Na2CO3·xH2O的混合物等分两份,一份溶于水配成200毫升溶液时,测得溶液中C( )=1.5 mol/L.若将另一份加热到质量不在变化时的固体质量为( )
)=1.5 mol/L.若将另一份加热到质量不在变化时的固体质量为( )
A 15.9 g B 21.2 g C 88.2 g D 条件不够,无法计算
10.下列各组离子,在强碱性溶液中可以大量共存的是( )
A. 、
、 、
、 、
、 B.
B.  、
、 、
、 、
、
C.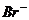 、
、
 、
、 、
、 D.
D. 、
、 、
、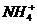 、
、
9.下列反应的化学方程式或离子方程式与反应物之间的相对量的多少无关的是
A 碳酸钠溶液与盐酸 B 氢氧化钡溶液与稀硫酸 ( )
C 碳酸氢钠溶液与澄清的石灰水 D 硝酸银溶液与氨水.
8.下列反应中,氧化剂与还原剂的物质的量之比为2 :1的是( )
A Zn + 2HCl = ZnCl2 + H2↑
B Cu +2 H2SO4(浓) = CuSO4 + SO2↑+ 2H2O
C 3S + 6NaOH = 2Na2S + Na2SO3 + 3H2O
D 2Na + Cl2 = 2NaCl
7.NA为阿伏加德罗常数,下列说法正确的是( )
A.标况下,22.4 L水中含有NA个H2O分子
B.14 g N2含有的核外电子总数为NA
C.1 mol乙烯中含2 NA个碳碳双键
D.2.3 g金属钠与足量水反应时失去的电子数是0.1NA
6.下列说法合理的是( )
A.既能与酸反应又能与碱反应的物质一定是两性物质
B.焰色反应属于元素的物理性质
C.物质的氧化性就是非金属性,是得电子的性质,物质的还原性就是金属性,是失电子的性质
D.已知铝与氢氧化钠溶液反应为: 2Al +2NaOH +2H2O = 2 NaAlO2 + 3H2↑
由化学方程式便知,铝是还原剂,水和氢氧化钠是氧化剂
5.下列说法正确的是( )
A.含氧的化合物就是氧化物
B.1 mol H2O中含有2 mol氢和1 mol氧
C.氧化剂的氧化性的相对强弱取决于得到电子数目的多少
D.等质量的铝分别与足量的盐酸和氢氧化钠溶液反应时逸出气体的量相等
4.鉴别碳酸钠、碳酸氢钠两种溶液的最合适的方法是( )
A.两种溶液各取少许,分别滴入酚酞试液,显红色的是碳酸钠溶液
B.两种溶液各取少许,分别滴加澄清的石灰水,有沉淀生成的是碳酸钠溶液
C.两种溶液各取少许,分别加热,能产生使澄清的石灰水变浑浊气体的是碳酸氢钠溶液
D.任取一种溶液少许,滴加氯化钡溶液,若有浑浊产生的是碳酸钠溶液,否则是碳酸氢钠溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com