
3ÈÛí°—૤ëöá°è¿¨ø¼àŠýÄåÖçÝòÝýºèºçáø¼ØˆÆ¯üšòúÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ (ÀÀÀÀ )
ÀÀ AÈÛÆÅâ«ÆÖ¥Æú¢ÑåÝÔ§ÛçÄú½çáÅÅí±¿ÉâÚÀÀ
ÀÀ BÈÛÇ짽êù¤¤æÍÆŠÝÔ§Ûèìò»ûþæÍçáƒÙ¥ûöá£₤§£ê¼ÀÀ
ÀÀ CÈÛò¿ÝÔ§ÛûþæÍí±à´êËò¶ÆÖøÅîŠÀÀÀÀÀÀÀÀ
ÀÀ DÈÛÅö°èêù¤¤æÍÆŠèìò»ûþæÍàÖ¤üçá¡Ô°Ý
2ÈÛØ£ö£ë˜îÏòí¥₤êùÆÅ¿ÄúÄò¥£ò¥Æú¢øÅ₤à´ÇŠòˋçáæòêüȘóðøÅý£ñ«¤üòôòççáòúÀÀÀÀ (ÀÀÀÀ )
ÀÀ AÈÛë°Ø£ÑàꢤãÈÛ£¾Ýؤë°ç¿šÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀÀÀ BÈÛë°Ø£öáæøÀÀ
ÀÀ CÈÛ¯ðý¥ë´ÅÅਿºçáúÄôèÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ DÈÛÇÇêÂë¾ö£òâüÛøó
1ÈÛòñòÕùª¥úåÄçáÀ¯ñ㧴úæóïȘØåߘóêøÉÀÝçáüøüµÇµ¿ÌáÈ°—üøÆΡûåÖÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ (ÀÀÀÀ )
ÀÀÀÀÀÀ AÈÛøÉöðë¾òÝóÖÀÀÀÀÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ BÈÛøÉâ¼ë¾òÝóÖÀÀÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ
ÀÀÀÀÀÀ CÈÛøÉÆáë¾òÝóÖÀÀÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ DÈÛøÉó§ë¾òÝóÖ
22ÈÛ¥æÀÂØØÀÂÝ«à»ë˜îÏÑåà»ñïøòê¢ý£ë˜çáî¾£₤ëÙÆŠä¢ñÜçᣚ¤üöÿîªóñAÀÂBÀÂC¡¼àÀØ£ñïȘ
¥Æú¢àà°ðñøñÇÆÎȘýãÑ´¡¼îªóñøÅî¾£₤ëÙçáê¢ÀÈ(ä¥ñÜý£àÉÆÖüÀü¾ùÃ)
ÀÀ (1)¥æàÀîªóñA¥Æú¢ààȘ躰èêꤚ訿ääͤëößè¨ößó½öÑçáó½äÍȘêꤚ訿ääÍáÉà¨àɧãÆÖüÀü¾ùÃȘ躰èçáößè¨ößó½öÑçáó½äÍÆû°öúÍò₤£ØùÛö■òíȘößó½äÍòÈÆÁȘ躰è¯æ訰êçÚ6ÈÛ00gȘå·îªóñAøÅî¾£₤ëÙçáøòê¢öˆÀÀÀÀ¢ùÀÈ
ÀÀ (2)ØØàÀîªóñB¥Æú¢ààȘ§¨ùªçûêꤚ訿ääÍøûÆÖüÀü¾ùÃøÅöÂààȘ¿ääÍëõà¨àɧãȘýºèº2ÈÛ24Ló½äÍ(Ýõ¢—)Șå·îªóñBøÅî¾£₤ëÙçáøòê¢öˆÀÀÀÀgȣඥæë˜îÏ¡áöˆé´ü¾ùÃàɧãÇùêꤚ訿ääÍȘëõà¨ñÇÆÎå·£Ã躰èÀÀÀÀL(Ýõ¢—)ó½äÍÀÈ
ÀÀ (3)Ý«àÀîªóñC¥Æú¢ààȘëõà¨ñÇÆΤµ§¨òÈÆÁ¿ääÍøûÆÖüÀü¾ùÃȘùªçûöÇàÉ¿ääÍøòê¢ÝàåÙîªóñ¥¾èìêùWgȘå·îªóñCøÅî¾£₤ëÙçáøòê¢öˆÀÀÀÀÀÀÀÀÀÈ(Æûñøò»ÝÚòƒ)
21ÈÛá°£₤îÏ¢öëãÅùàÊÅÀæÕöˆä§ƒ¢ëÙ¡ºé´ê·ùÃçáñÇÆÎúÕ¢—ȘÆûüôë¥ùªòƒæ¯øûü৽ÅÅêùÆÅ¿ÄòçîÕȤ
 ÀÀ
ÀÀ
ÀÀ (1)BòúÆûâÇòí¥₤òçîÕøÅýºèºçáó½äÍçáæ¯øûȘç¨öǧ¨ç¥¿É£Ùà¨È˜úŠøݧÆåÖåÙë¥èü¯î祿Éý¿°ðëõí«ÀÈ
ÀÀ (2)òçîÕøÅù«ûúàÀ6ÈÛ4gëÙó˜¤ë12mL18molÀÊLÈÙ1é´ê·ùÃñéåÖåýçæèíó¢øÅ¿ýààȘøÝç§ñÇÆÎëõÝüȘ柤µñÂüøèíó¢øÅ£¿ÆÅëÙó˜òÈÆÁȘ¡ûÅÀæÕîÏ躡ªƒïùªîÏçá£₤îÏøˆòÑàüöˆ£¿ÆÅأѴê¢çáê·ùÃòÈÆÁÀÈ
ÂìúŠÅÇ°—ëÙ¡ºé´ê·ùÃñÇÆÎçá£₤îÏñ§°äò§È¤ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ
ÂÖöˆòýûÇÆÅأѴê¢çáÆÁùÃç¨öÇáÉò¿ëÙó˜ëõà¨àɧãȘáÐàüöˆåÙØ·òúȤÀÀÀÀÀÀÀÀÀÀÀÀÀÀ
ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÈ
ÂÜüôêÅØˋóñøÅáÉ¿£ÆûâÇøÊû¼ñÇÆΧÃò½¤µçáèíó¢øÅàñÆÅÆÁùÃçáòúÀÀ(äŸÅÇæøá¡ÝÁ¤é)
ÀÀÀÀ AÈÛÅ¢êÈÀÀÀÀÀÀÀÀÀÀÀÀÀÀ BÈÛò₤£Øò₤ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ CÈÛNa2CO3àÉؤÀÀÀÀ DÈÛBaCl2àÉؤ
ÀÀ (3)öˆÑ´ê¢ýãÑ´ÆÁùÃçáöÿøòçáê¢é´ÑàȘ¥æÀÂØØê§îÏ躧½ÅÅêùàÓüôèÒ¥óȤ
Âì¥æîÏèºèÒ¥óñ§¯¡òúȤüàýãÑ´ëÙÆŠé´ê·ùÃñÇÆÎýºèºSO2çáê¢È˜åì¥óùÐÆÁùÃçáöÿøòçáê¢é´ÑàȘù«àüöˆýãÑ´SO2çáê¢çáñ§ñ´ÆÅÑÁøøȘúŠöòüôêÅòçîÕñ§¯¡øÅý£¢èÅÅçáòúÀÀÀÀ(äŸÅÇæøá¡ÝÁ¤é)ÀÈ
ÀÀÀÀÀÀ ÀÀÀÀ AÈÛ§¨æ¯øûAýºèºçáó½äÍ£¤£¤ë´¿»åÊüà°óꢿ»òÂÆÅ¥Ÿò₤£Øçá¡èåÿ¿ÉȘ§Ãò½ñÇÆΤµåìÇö°óê¢ÀÈ
BÈÛ§¨æ¯øûAýºèºçáó½äÍ£¤£¤ë´àŠæÐê¢çáê·ùÃùã₤çáKMnO4øÅàÉؤȘåì¥ÆàŠæÐê¢BaCl2àÉؤȘ¿»ôùÀÂüÇçÆÀ¡èåÿÀ°óꢰêçÚ
CÈÛÆûééùÛñ´ýãÑ´æ¯øûAýºèºó½äÍçáäÍ£»(ØîíÜùаèÝõæ¥æÇ¢—)
DÈÛÆûééÝˤëNaHSO3àÉؤçáñ§ñ´ýã°—æ¯øûAýºèºó½äÍçáäÍ£»(ØîíÜùа—Ýõæ¥æÇ¢—)
ÂÖØØîÏèºèÒ¥óçáñ§¯¡òúȤåÖñÇÆΤµçáàÉؤøÅ¥Æí¶êµùÛüÀòëøê1000mlȘàÀ20 mlÆÖæÑ
Åöó¢øÅȘçöàŠ¥æ£ª°àø¡òƒ¥êȘÆûÝõæ¥úãî¾£₤áóàÉؤ§½ÅÅçöÑ´(ØîøˆÈ¤Cu(OH)2¢ˆò¥°êçÚçáPHå¥öˆ5)Ș봿»ýã°—ü«¤áNaOHàÉؤçáäÍ£»âÇúµÆÁùÃçáöÿøòçáê¢çáé´ÑàÀÈ
¥ìÑ´ñÇÆÎú¯¤µèíó¢øÅàÉؤçáäÍ£»ý£ÝðȘáÐàüöˆØØîÏèºèÒ¥óçáòçîÕñ§¯¡áÉñþúµçûÆÁùÃçáöÿøòçáê¢é´ÑàÀÀÀÀ(äŸÀ¯áÉÀÝ£·À¯ñþÀÝ)ÀÈóðâÚÆèòúÀÀÀÀÀÀÀÀÀÀÀÀÀÈ
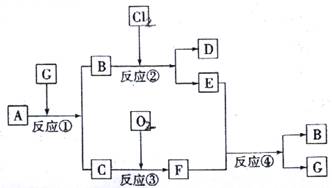
20ÈÛ¤Ö訿ääÍöÿøòAÆÅØåüô戣₤¿ÄüçȘû¢¡—ñ§¢·ÝÚòƒÆÅØ£øøñÇÆÎöÿ£·èº°èöÿ(ñÇÆÎä¾¥±¥¯èº°èçáùÛôåàË)ȘóðøÅCÀÂF°Èöôöˆößè¨ó½äÍȘDÀÂEÆÅ¿ýë˜çáî¶âŠæÆÀÈ
 ÀÀ
ÀÀ
ÀÀ (1)ÅÇ°—B¤ëFçá£₤îÏò§È¤BÀÀÀÀÀÀÀÀÀÀÀÀ ÀÀÀÀ È£FÀÀÀÀÀÀÀÀÀÀÀÈ
ÀÀ (2)ÅÇ°—CçáçÓæÆò§ÀÀÀÀÀÀÀÀÀÀÀÈ
ÀÀ (3)ÅÇ°—ñÇÆÎÂÉçáâŠæÆñ§°äò§ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÈ£ÅÇ°—ñÇÆÎÂÖçáâŠæÆñ§°äò§ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÈ
19ÈÛAÀÂBÀÂCÀÂDÀÂEöˆÑäøÉóÖåˆùÄȘåÙæÆÅ·ò»ØâÇöå—ǵÀÈóðøÅAÆŠEë˜ø¼æÍȘBçáæŸëãýÐ
çÓæÆò»òúÇöëãýÐçÓæÆò»çá2ÝÑȘCçá柡ԥÜî¾£₤öÿÑåÆÎçáùÛ£₤öÿÆŠóðúã£₤öÿñÇÆÎ躰èØ£
øøîöXÀÈAÀÂBÀÂDÀÂE¢èæÕ°è£₤¤üöÿA2D2ÀÂB2A2ÀÂE2D2Șù■ûúÑ¥¤˜ÆÅñú¥¨Åå¿ý¥Ü§ÀÀÈ
ÀÀ (1)CåˆùÄåÖøÉóÖÝÚøÅçáö£øûòúÀÀÀÀȘÅÇ°—Bçá柡ԥÜî¾£₤öÿçá§Ã¿¿ò§ÀÀÀÀÀÀÀÈ
ÀÀ (2)XçáùÛàÉؤüåÀÀÀÀÀÀ(äŸÀ¯ùÃÀÝÀÂÀ¯¥ŸÀÝ£·À¯øÅÀÝ)ÅåȘâÚÆèòú(ÆûâŠæÆñ§°äò§ÝÚòƒ)ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÈ
ÀÀ (3)AÀÂBÀÂDÀÂEùáøøåˆùÄæÕ°èçá£₤¤üöÿøÅåÙæÆ¡—ò»æŸèìçá£₤¤üöÿçá£₤îÏò§öˆ
ÀÀÀÀÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÈ
ÀÀ (4)£Þ¥»ëó§½ó¼øÅæ¯ÆÅؤä˜C2A4¤ëؤä˜çáA2D2Șù■ûúñÂ躣₤îÏñÇÆÎòÝ躰èó½ä˜CçËøò¤ëùÛí¶ó½È˜ýÂñ鰗ǵê¢ààÀÈØîøˆ0ÈÛ4moIؤä˜C2A4¤ëؤä˜çáA2D2ëõà¨ñÇÆÎòÝȘñé°—256ÈÛ6kJààê¢È˜¡ûñÇÆÎçáàà£₤îÏñ§°äò§öˆÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÈ
18ÈÛüôÝÚÆèåˆùÄøÉóÖÝÚçáú¯à»øÉóÖàË綡ÝæÍèüñ§çá¢í¯æú½Æ·¤µæÕ¤üѽ°èȘÝÚøÅÅÕüÔÇÎöˆÂ·AȘµAæÍçá꘧ÆÇÎÀÈúŠÆûüÁÆÎçá£₤îÏÆûÆÿ£ÄÇÞüôêÅöòäãȤ

ÀÀ (1)ÅÇ°—ÆèeÅö°èçáê§øøǽÆÅüÁ똤ùçÓ¤èò»Ø¾âŠæÆçáñ«¤éȤÀÀÀÀÀÀ ÀÀ ÀÀ ÀÀÀÂÀÀÀÀÀÀÀÀÀÀ ÀÀ ÀÀÀÈ ÀÀ (2)hçáçËøòáÉÆŠgåˆùÄçá柡ԥÜî¾£₤öÿÑåÆÎçáùÛ£₤öÿçáàÉؤñÇÆÎȘúŠÅÇ°—¡ûñÇÆÎçáÀÀ
âŠæÆñ§°äò§ÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ ÀÀÀÈ
ÀÀ (3)üôæµë¥òúÝÚòƒçÖà»øÉóÖ8øøåˆùÄçËøòçáàÜçÐ(ÀÌ)øªÅöë¥È˜ØîøˆøªÅöÀ¯1ÀÝǺÝÚ
ArȘå·óðøÅøªÅöÀ¯8ÀÝǺÝÚÀÀÀÀÀÀÀÀÀÀÀÀ ÀÀÀÈ(䟣₤îÏò§)

ÀÀ (4)bÀÂcÀÂdÀÂeÀÂfçáúã£₤öÿçáñÅçÐ(ÀÌ)øݧúæ½Ýõë¥(èüÆØë¥)ȘŷêÅÀ¯5ÀÝçáúã£₤öÿ
çáû«°óòúÀÀÀÀÀÀÀÀÀÀÀÀ ÀÀȘŷêÅÀ¯2ÀÝçáúã£₤öÿçá¢í¥ð¿¿ÅëöˆÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ ÀÀÀÈ
ÀÀ (5)çËøòa¤ëçËøòe¢èØåèÒ¥óöˆÅôÅëà¥êüçÓ°ÄȘçÓ§ãøòöˆKOHàÉؤȘå·çËøòaåÖ¡ûÀÀ
à¥êüçÓ°ÄçáÀÀÀÀÀÀÀÀÀÀÀÀ ÀÀ¥¨ñÂèºçÓ¥¨ñÇÆÎȘçÓ¥¨ñÇÆÎò§öˆÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ ÀÈ
17ÈÛ¡ÔäºùÃáó(£₤îÏò§öˆNa2FeO4)òúØ£øøÅôÅ냣ùÛ¥êȘ¿ÊØçèü°Èë´¿»àÓüô£₤îÏñÇÆÎøóàÀȤ
ÀÀFe2O3+3NaNO3+4NaOH====2Na2FeO4+3NaNO2+2H2OÀÈ
ÀÀ (1)ñÇÆÎøÅȘ₤¥êöˆÀÀÀÀÀÀÀÀÀÈ
ÀÀ (2)çÝ躰è4moLNa2FeO4òÝȘçÓæÆæˆØóæÉò»öˆÀÀÀÀÀÀmoLÀÈ
16ÈÛÆûæÐê¢çáCO£¿åÙ32ÈÛ0 gá°øøî¾£₤öÿȘ§¨èº°èçáó½äÍë´àŠæÐꢰöúÍò₤£ØùÛøÅȘçûç§
60g°êçÚȘ巡ûî¾£₤öÿòúÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀÀ (ÀÀÀÀ )
ÀÀAÈÛ FeOÀÀÀÀ ÀÀÀÀÀÀÀÀÀÀÀÀ BÈÛ Fe2O3ÀÀÀÀÀÀÀÀÀÀÀÀÀÀ CÈÛ CuOÀÀÀÀ ÀÀÀÀÀÀÀÀÀÀ DÈÛ Cu2O
¿º¥òîÏÅÈÆéîÀ - êñü¯ýÃêÅÝÚ - òåäãêÅÝÚ
¤±ÝÝòÀ£Ëêˆë½öËñ´¤ëý£ê¥ÅéüƒìÝ´ó§ä´ | ë½èüÆŤÎÅéüƒìÝ´æ´ú½ | çÓÅéíˋóÙƒìÝ´æ´ú½ | èÌâºòñÅÕößø¼ØÍÆŤÎÅéüƒìÝ´æ´ú½ | èÌóµúøà´ƒìÝ´æ´ú½
öËñ´¤ëý£ê¥ÅéüƒìÝ´çÓ£¯È¤027-86699610 ƒìÝ´ÆòüðȤ58377363@163.com