
17.(11分)设反应①Fe(s)+CO2(g)  FeO(s)+CO(g) △H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g) △H=Q1的平衡常数为K1,反应②Fe(s)+H2O(g)  FeO(s)+H2(g) △H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) △H=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
|
温度( T ) |
K1 |
K2 |
|
973 |
1.47 |
2.38 |
|
1173 |
2.15 |
1.67 |
(1)从上表可推断,反应①是 ▲ (填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g)  CO(g)+H2O(g) △H=Q3
CO(g)+H2O(g) △H=Q3
①根据反应①与②推导出K1、K2、K3的关系式K3= ▲ ;可推断反应③
是 ▲ (填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可
采取的措施有 ▲ 。
A.缩小容器体积 B.降低温度
C.使用合适的催化剂 D.设法减少CO的量 E.升高温度
②根据反应①与②推导出Q1、Q2、Q3的关系式Q3= ▲ ;
(3)现在恒容密闭容器中通入一定量CO2,再慢慢通入H2,使发生上述反应③,在其他条件不变时,若改变H2的起始量,容器中 CO的体积分数也随之改变,请在右图中画出CO的体积分数随n(H2)变化的示意图。

16.(10分)下图所示实验中,A、B中的电极为多孔铂电极,c、d为夹在经Na2SO4溶液浸湿的滤纸条上的铂夹,a、b为电源的两极。将A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,断开开关K1,闭合K2、K3,通以直流电。

请回答下列问题:
(1) a为直流电源 ▲ 极。
(2) 滤纸上(实验开始时中央滴有KMnO4液滴)的明显现象为 ▲ ;
(3) 写出电极反应式:A极: ▲ ;C极: ▲ 。
(4) 若经电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针是否发生偏转,说明你的理由 ▲ 。
15. (12分)核电荷数由小到大顺序排列的五种短周期元素X、Y、Z、W、Q。其中:在同周期元素中,Z的金属性最强,Q的非金属性最强;W的单质是淡黄色固体;X、Y、W在周期表中的相对位置关系如图所示:
(12分)核电荷数由小到大顺序排列的五种短周期元素X、Y、Z、W、Q。其中:在同周期元素中,Z的金属性最强,Q的非金属性最强;W的单质是淡黄色固体;X、Y、W在周期表中的相对位置关系如图所示:
(1)五种元素形成的单质,其中:固态时属于原子晶体的是 ▲ (填单质名称);
(2)这五种元素中,原子半径最大的是 ▲ (填化学式);由Z、W、Q形成的简单离子半径由大到小的顺序是 ▲ (用化学式表示);X、W、Q的最高价氧化物的水化物酸性从强到弱的顺序为 ▲ (用化学式表示);
(3)Y和Z形成的一种化合物中含有离子键和共价键,写出该化合物与水反应的化学方程式 ▲ ;
(4)写出由W所在主族元素形成的含有18e-的四原子氢化物的电子式 ▲ ;
(5)由X、Y和氢三种元素组成的化合物X6H12Y6,已知:9g该化合物燃烧生成XY2和液态H2Y时,放出140kJ的热。写出该化合物燃烧热的热化学方程式: ▲ 。
14.下列有关说法不正确的是
A.具有相同通式的有机物不一定互为同系物
B.分子组成相差一个或若干个CH2原子团的化合物一定互为同系物
C.分子式为C3H8与C6H14的两种有机物一定互为同系物
D.两个相邻同系物的相对分子质量数值一定相差14
第Ⅱ卷(共58分)
13.两个体积相同的密闭容器A和B,在A中充入SO2和O2各1g,在B中充入SO2和O2各2g,加热到相同温度,发生如下反应:2SO2(气)+O2(气)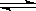 2SO3(气),对此反应的下列说法不正确的是
2SO3(气),对此反应的下列说法不正确的是
A.反应速率:B>A B.SO2的转化率B>A
C.平衡时各组分含量:B=A D.平衡时容器内压强B>A
12.镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:
 MgxMo3S4
x Mg + Mo3S4
MgxMo3S4
x Mg + Mo3S4
在镁原电池放电时,下列说法错误的是
A.Mg2+向正极迁移 B.正极反应为:Mo3S4 + 2xe- = Mo3S42x
C.Mo3S4发生氧化反应 D.负极反应为:xMg-2xe- = xMg2+
11.X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期, W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价代数和为6。下列说法正确的是
A.Y元素最高价氧化物对应的水化物化学式H2YO4
B.X与W可以形成W2X、W2X2两种化合物
C.原子半径由小到大的顺序为:W<X<Z<Y
D.Y、Z两种元素气态氢化物中,Z的气态氢化物最稳定
10.某溶液中加入铝粉产生的气体只有氢气,该溶液中肯定可以大量存在的离子组是
A.Na+、NO3-、Cl-、SO42- B.Na+、K+、Ba2+、HCO3-
C.Na+、K+、Cl-、SO42- D.Fe3+、H+、SO42-、Cl-
9.有关键能数据如表:
晶体硅在氧气中燃烧的热化学方程式为Si(s)+ O2(g)=SiO2(s); = -989.2/kJ·mol-1,则X的值为
= -989.2/kJ·mol-1,则X的值为
A.423.3 B.460 C.1165.2 D.920
8.在25℃、101kPa下,1g乙醇完全燃烧生成CO2和液态水时放热29.72kJ,下列热化学方程式正确的是
A.CH3CH2OH(l)+3O2(g)=2CO2(g)+ 3H2O(l);△H=+1367kJ/mol
B.2CH3CH2OH(l)+6O2(g)=4CO2(g)+ 6H2O(l);△H=-2734kJ/mol
C.2CH3CH2OH(l)+6O2(g)=4CO2(g)+ 6H2O(l);△H=-1367kJ/mol
D.2CH3CH2OH(l)+6O2(g)=4CO2(g)+ 6H2O(l);△H=+2734kJ/mol
|
化学键 |
Si-O |
O=O] |
Si-Si |
|
键能/kJ·mol-1 |
X |
498.8 |
176 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com