
1.(2)2:1
(3)3〈a〈1.9
(4)BC
12、(1)不可能
12、(06盐城三模)在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
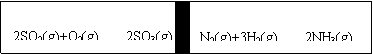
⑴若其始时左侧投入2molSO2、1molO2,右侧投入1molN2、4molH2,达到平衡后(两侧温度相同),隔板是否可能在、仍处于中央 (填“可能或不可能”)
⑵起始时投入2molSO2、1molO2;1molN2、2molH2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字)
⑶若起始时投入2molSO2、1molO2;1molN2、amolH2、0.1molNH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于中央,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围
⑷若起始时投入2molSO2、1molO2,欲用简单方法粗略测定平衡时SO2的转化率,则可将左侧的平衡混合气体中通入足量的 (填序号)
A、碳酸钠与碳酸氢钠混合溶液 B、氯化钡溶液
C、98.3%的浓硫酸 D、硝酸钡混合溶液
11、⑴任意(2分) ⑵n(D)>0.8(2分)
⑶当升高到一定温度以后,D渐渐转化为气态(2分)
Mr(A)+2Mr(B)==3Mr(C)+2Mr(D)(2分)
⑷①气体物质两边的化学计量数相等,增大压强不改变平衡状态。(1分)
②B渐渐转化为非气态,增大压强平衡向左移动。(1分)
③C渐渐转化为非气态,增大压强平衡再次向右移动。(1分)
11、(06宿迁二模)在一定温度下,向一固定容积的密闭容器中加入 1mol A和 2mol B,发生下述反应:A(g)+2B(g) 3C(g)+2D(s);ΔH<0。达到平衡时生成了1.8 mol C。
3C(g)+2D(s);ΔH<0。达到平衡时生成了1.8 mol C。
⑴在相同条件下,若向该容器中改为加入0.3mol A、0.6 mol B,要使平衡混合气体中C物质的体积分数与原平衡的相同,在D足量时,则还应加入 mol的物质C。
⑵若维持容器的体积和温度不变,反应从逆反应方向开始,按不同的配比作为起始物质,达到平衡时C仍为1.8 mol 。则D的起始物质的量n(D)应满足的条件是:n(D) mol。
当改变温度或压强时,有可能改变物质的聚集状态,对平衡产生重大影响。
⑶若升高平衡体系温度,当再次达到平衡后,测得两次平衡条件下混合气体的平均相对分子质量未发生改变,试解释形成这种结果的可能原因是:
;此时A、B、C、D四种物质相对分子质量之间的关系为 (用Mr(A)、Mr(B)、Mr(C)、Mr(D)表示)。
⑷若将容器改为容积可变的容器,在一定温度和常压下,建立上述平衡之后,A的物质的量浓度为a mol/L。现持续增大压强,当:
①当压强为原来1.5倍时,A的平衡时物质的量浓度为m mol/L,测得m=1.5a;
②当压强为原来10倍时,A的平衡时物质的量浓度为n mol/L,测得n >10 a;
③当压强为原来100倍时,A的平衡时物质的量浓度为p mol/L,测得p<100a。
试解释形成这种结果的可能的原因:
①1.5倍时: ;
②10倍时: ;
③100倍时: 。
10、(1)D
(2)降低;增大;<;增大体积使 的浓度减小,平衡向右移动,由于正反应是吸热反应,故体系的温度降低,重新达到平衡时,
的浓度减小,平衡向右移动,由于正反应是吸热反应,故体系的温度降低,重新达到平衡时, 的压强必小于850℃的平衡压强
的压强必小于850℃的平衡压强
10、反应

 在不同温度下,
在不同温度下, 的平衡压强如下表:
的平衡压强如下表:
|
温度/℃ |
550 |
650 |
750 |
850 |
897 |
|
压强/Pa |
5.32×10 |
 |
 |
 |
 |
根据上表数据,填写下列空白:
(1)若升高原 的分解平衡体系的温度,同时给反应容器加压,则原平衡_________________。
的分解平衡体系的温度,同时给反应容器加压,则原平衡_________________。
A.向逆反应方向移动 B.向正反应方向移动
C.不移动 D.无法确定平衡移动方向
(2)在一个不与外界进行热交换的密闭器中足量的 在850℃时建立分解平衡。若将该容器的容积扩大为原来的2倍,需重新达到平衡时,容器内的温度将_______________,
在850℃时建立分解平衡。若将该容器的容积扩大为原来的2倍,需重新达到平衡时,容器内的温度将_______________, 的分解率将____________________________,
的分解率将____________________________, 的平衡压强将________________
的平衡压强将________________ (填“>”、“=”、“<”),其理由是_________________________________________________________________________________。
(填“>”、“=”、“<”),其理由是_________________________________________________________________________________。
9、Ⅰ、(1)不变 ,增大(2)增大 ,增大 (3)不变 , 不变
Ⅱ、 1 < 2 < 3
Ⅲ、 x > 0.8 ,y = 1
9、在一个1L的可变容积的密闭容器中,在某温度下加入一定量的C(足量)和H2O(g)发生下列反应:
C(s)+ H2O(g)  CO(g)+H2(g)
CO(g)+H2(g)
Ⅰ、(1)若保持容器容积不变,通入一定量氖气,则达到新平衡时H2O的转化率 。保持压强不变,通入氖气使体系的容积增大一倍,则达到新平衡时H2O的转化率 。(填“增大”或“减小”或“不变”)
(2)在反应达平衡后,保持容器容积不变,通入一定量H2O(g),则达到新平衡时H2O百分含量 。保持容器容积不变,通入一定量物质的量比为1∶1的CO和H2,则达到新平衡时H2O百分含量 。(填“增大”或“减小”或“不变”)
(3)若保持压强不变,通入一定量H2O(g),则达到新平衡时H2O百分含量 。保持容器压强不变,通入一定量物质的量比未1∶1的CO和H2,则达到新平衡时H2O百分含量 。(填“增大”或“减小”或“不变”)
Ⅱ、若保持容器容积不变,开始时充入容器中的起始物质是①C(足量)、2mol H2O(g);②C(足量)、2mol H2O(g)、1molCO;③C(足量)、2mol H2O(g)、1molCO、1molH2;达到平衡时容器中H2O(g)浓度由小到大排列顺序是 。(填序号)
Ⅲ、若保持压强不变,起始时充入①C(足量)、2mol H2O(g);②C x mol、2mol H2O(g)、1molCO、y molH2时,达到平衡时,H2的浓度都相同,平衡①中H2的物质的量为1.2mol。则 x > ,y = 。
8、现有三个体积相等的密闭容器中都进行如下反应:
 CO2+H2 CO+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中甲:[H2]=[CO]=amol 乙:[CO2]=amol [H2]=2amol 丙[CO2]=[H2]=[H2O]=amol,达到平衡时,CO的浓度由大到小的顺序排列正确的是(D )
CO2+H2 CO+H2O(g),反应所处的温度相同,但反应的起始浓度不同,其中甲:[H2]=[CO]=amol 乙:[CO2]=amol [H2]=2amol 丙[CO2]=[H2]=[H2O]=amol,达到平衡时,CO的浓度由大到小的顺序排列正确的是(D )
A、丙>甲>乙 B、甲>乙>丙 C、乙>丙>甲 D、乙>甲>丙
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com