
20.(14分)某工厂用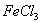 溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为:
溶液腐蚀镀有铜的绝缘板生产印刷电路,发生反应的化学方程式为: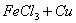 ======
======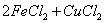 。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:
。实验小组的同学对生产印刷电路板的废液成分进行了如下探究:
①取少量废液,滴加KSCN溶液显红色。
②取10mL废液,加入足量的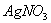 溶液,析出沉淀8.6l g。
溶液,析出沉淀8.6l g。
③另取10mL废液,加入一定质量的铜片,充分反应后,测得铜片的质量减少了0.256g
再向反应后的溶液中滴加KSCN溶液不变色。
根据探究实验得出结论:
(1)废液中含有的金属离子是 。
(2)根据有关数据计算该厂使用的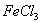 溶液中溶质的物质的量浓度(假设腐蚀电路板后溶液体积不变。写出计算过程)。
溶液中溶质的物质的量浓度(假设腐蚀电路板后溶液体积不变。写出计算过程)。
(3)10mL废液中铜离子的物质的量是 mol。
19.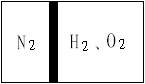 (12分)常温下,在一刚性容器内部有一个不漏气且可以滑动的 活塞,将容器分割成左右两室。左室充入N2,右室充入H2和O2,活塞正好使N2占容器体积的1/4(如图)。然后点燃H2和O2的混合气体,反应完毕后恢复至原来的温度,活塞正好停留在容器的中间。
(12分)常温下,在一刚性容器内部有一个不漏气且可以滑动的 活塞,将容器分割成左右两室。左室充入N2,右室充入H2和O2,活塞正好使N2占容器体积的1/4(如图)。然后点燃H2和O2的混合气体,反应完毕后恢复至原来的温度,活塞正好停留在容器的中间。
经检验,此时右室中气体可使带火星的木条复燃。求反应前H2和O2的物质的量之比。
18.(12分)过氧化钙是一种安全无毒的物质,带有数量不等的结晶水,通常还含有部分CaO。
(1)称取0.813g过氧化钙样品,灼热时发生如下反应:
|
(2)另取同一样品0.813g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中的Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO31.5g。
①样品中CaO的质量是 克;
②样品中CaO2·xH2O的x值为 。
17.(10分)由钾和氧组成的物质含钾的质量分数是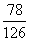 ,其阴离子只有过氧根离子(O22-)和超氧根离子(O2-)两种。求在此物质中,过氧根离子和超氧根离子的个数比
,其阴离子只有过氧根离子(O22-)和超氧根离子(O2-)两种。求在此物质中,过氧根离子和超氧根离子的个数比
16.以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到4mol Fe(OH)3沉淀,此间共消耗的水的物质的量为
A 8mol B 10mol C 11mol D 12mol
15.某试样为硫铵和磷酸氢二铵的混和物,经测定其中含百分率为21.2%,则试样中两种物质的物质的量比为:
A、1:1 B、4:1 C、1:4 D、任意比
14.将KCl和 BaCl2的混合溶液a L均匀分成两份。向其中一份中滴加稀硫酸,使Ba2+离子完全沉淀;向另一份中滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗xmol H2SO4、ymol AgNO3。下列有关推断正确的是
A.x=y
B.c(K+)=(2y-4x)/a mol·L-1
C.若a L混合溶液中c(Cl-)=1mol/L,则y=a、x=0.5a
D.若a L混合溶液中c(K+)=1mol/L,且y=0.4mol,则x=(0.2-0.5a )mol
13.在体积为VL的密闭容器中进行如下反应:mA+nB=pC+qD用A物的浓度变化表示的平均反应速率为 ,则t min时,D物增加的物质的量是
,则t min时,D物增加的物质的量是
(A) (B)
(B) (C)
(C) (D)
(D)
12.已知两个热化学方程式:
C(s)+O2(g)==CO2(g) △H= ―393.5kJ/mol
2H2(g)+O2(g)==2H2O(g) △H= ―483.6kJ/mol
现有炭粉和H2组成的悬浮气共0.2mol,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是
A.1︰1 B.1︰2
C.2︰3 D.3︰2
11.Na2O2、HCl、Al2O3 三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl―、OH―;且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为
A.3:2:1 B.2:4:1 C.2:3:1 D.4:2:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com