
37、如下有关原电池说法不正确的是:
A、原电池是将化学能转变成电能的装置
B、原电池中的化学反应是自发的氧化还原反应(高能量物质生成低能量物质的反应)
C、原电池的负极肯定是金属材料,正极不一定是金属材料但必须是导体
D、原电池在工作时,电解质溶液中的阳离子向正极移动,阴离子向负极移动
36、如下有关能量转变的说法不正确的是:
A、蜡烛的燃烧是化学能转变成光能和热能
B、火力发电是将化学能转化成热能,热能转化成机械能,机械能转化成电能
C、原电池放电时发生的反应一定是低能量物质生成高能量物质 D、吸热反应是将热能转化成化学能
35、如下有关化学变化中的能量转化的说法不正确的是:
A、化学反应中化学键的断裂需要吸收能量,化学键的形成释放出能量;
B、由高能量物质生成低能量物质,会释放出能量 C、由低能量物质生成高能量物质,会吸收能量
D、放热反应往往是总能量高的物质生成总能量低的物质
E、需要加热才发生的反应一定是吸热反应 (答案:31、F 32、F 33、H 34、D 35、E)
34、如下有关氧化性强弱的比较说法不正确的是:
A、金属性越强的金属,还原性越强 B、非金属性越强的非金属单质,氧化性越强
C、同一氧化还原反应中,氧化剂的氧化性强于氧化产物,还原剂的还原性强于还原产物
D、同种元素处于高价态下的氧化性一定强于处于低价态下的氧化性
33、如下对于氧化还原反应的说法不正确的是:
A、氧化还原反应的本质是反应中有电子的得失或偏移 B、氧化还原反应的表征是有化合价的升降
C、氧化剂在反应中得电子、化合价降低、被还原,生成还原产物
D、还原剂在反应中失电子、化合价升高、被氧化,生成氧化产物
E、氧化还原反应中的电子转移数=化合价升高的总数=化合价降低的总数
F、活泼的非金属单质常作氧化剂 G、处于中间价态的元素既有氧化性又有还原性
H、金属只能作还原剂,非金属只能做氧化剂
I、置换反应、有单质参加的化合反应、有单质生成的分解反应都属于氧化还原反应
32、如下对主族元素的说法不正确的是:
A、周期表中左下角的金属的活泼性最强,右上角的非金属元素的非金属性最强
B、同主族从上到下,原子半径递增,原子失电子能力增强,元素的金属性增强,非金属性减弱
C、同周期从左到右,原子半径递减,原子得电子能力增强,元素的金属性递减,非金属性增强
D、最外层电子数等于元素所处的族序数,电子层数等于所在的周期数
E、越活泼的金属对应的碱碱性越强,越活泼的非金属,对应的最高价氧化物的水化物的酸性越强
F、越活泼的非金属,其氢化物越不稳定
31、如下有关周期律及周期表的说法不正确的是:
A、元素周期律的实质:元素性质随原子序数的递增而呈周期性变化的规律。
B、核外电子排布、原子半径的周期性变化决定了元素的主要化合价、金属性、非金属性的周期性的变化
C、周期表有七个横行,称为七周期。分为三个短周期,四个长周期
D、周期表有十八个纵行。分为七个主族、七个副族、一个零族、一个VIII族
E、第三周期含8种元素,第五周期含18种元素
F、第三纵行是第三副族,第13纵行是第IIIA族,第十八纵行是第VIII族
30、如下有关化学键的定义,离子键、共价键的形成说法不正确的是:
A、相邻的两个或多个原子之间强烈的相互作用,通常叫化学键。
B、阴、阳离子间通过静电作用所形成的化学键,叫离子键。如NaCl中的Na+与Cl-之间。
C、通过共用电子对而形成的化学键,叫共价键。如HCl分子中的H原子与Cl原子之间。
D、氯化钠的形成: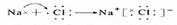 E、氯化氢的形成:
E、氯化氢的形成:
E、离子化合物中只有离子键,共价化合物中只有共价键
(答:26、D 27、F 28、C 29、B 30 、E)
29、如下说法不正确的是:
A、核外电子的运动特征:高速运动,无确定轨迹,分层排布。
B、距原子核的远近和能量的高低的关系:距核越远,能量越低。
C、核外电子层K层是离核最近的一层,M层是由里到外的第三层
D、电子先排布在能量低的层再排布到能量高的电子层;
E、各层最多容纳的电子数是2n2个;
F、最外层电子数不超过8个(K层最多为2个);
G、次外层电子数不超过18个,倒数第三层不超过32个。
28.某粒子含有6个电子、7个中子,净电荷数为0,则它的化学符号可能是 ( )
A.13Al B.13Al C.13C D.13C
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com