
16、在水平放置的已经充电的平行板电容器之间,有一带负电的油滴处于静止状态.若某时刻油滴的电荷量开始减小(质量不变),为维持该油滴原来的静止状态应: 
A.给平行板电容器继续充电,补充电荷量 B.让平行板电容器放电,减少电荷量
C.使两极板相互靠近些
D.使两极板相互远离些
15、 在地球赤道上空,沿东西方向水平放置一根通以由西向东的直线电流,则此导线:
在地球赤道上空,沿东西方向水平放置一根通以由西向东的直线电流,则此导线:
A.受到竖直向上的安培力 B.受到竖直向下的安培力
C.受到由南向北的安培力 D.受到由西向东的安培力
14、下列说法正确的是:
A.当作用力做正功时,反作用力一定做负功
B.当作用力不做功时,反作用力也不做功
C.作用力与反作用力的功,一定大小相等,正负符号相反
D.作用力做正功,反作用力也可能做正功
13.关于磁感线和电场线,下述说法正确的是: 
A.磁感线是闭和曲线,而静电场的电场线不是闭和曲线。
B.磁感线和电场线都是一些互相平行的曲线。
 C.磁感线起始于N极,终止于S极;电场线起始于正电荷,终止于负电荷。
C.磁感线起始于N极,终止于S极;电场线起始于正电荷,终止于负电荷。
D.磁感线和电场线都只能分别表示磁场和电场的方向。
12.下列各组离子:(1) I-、ClO-、NO3-、Cl-; (2) K+、H+、NO3-、Cl-;
(3)SO32-、S2-、Cl-、OH-;
(4)Mg2+、Cu2+、SO42-、Cl-; (5)Fe3+、SCN-、K+、SO42-;
(6)K+、HPO42-、PO43-、HSO3- 。在溶液中能大量共存的组别共有
A.1组
B.2组
C.3组
D.不少于4组
11.镁-H2O2酸性燃料电池采用海水作电解质(加入一定量的酸),下列结论不正确的是
A.正极发生的电极反应为:H2O2+2H++2e-=2H2O
B.电池总反应为:Mg+H2O2=Mg(OH)2
C.工作时,正极周围海水的pH增大

D.电池工作时,溶液中的H+向正极移动
10.下列反应的离子方程式书写正确的是 
A.浓烧减溶液中加入铝片:Al + 2OH-=AlO2-+H2↑ 
B.以石墨作电极电解氯化铝溶液:2Cl-+2H2O  2OH-+H2↑ +Cl2↑
2OH-+H2↑ +Cl2↑ 
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2 +2H+=2Fe3++2H2O

D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O =沸水=Fe(OH)3↓+3H+
9.右图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散。下列判断正确的是
A.滤纸上c点附近会变红色
B.Cu电极质量减小,Pt电极质量增大
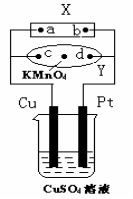 C.烧杯中溶液的pH先减小,后增大
D.烧杯中溶液中SO42-向Cu电极定向移动
C.烧杯中溶液的pH先减小,后增大
D.烧杯中溶液中SO42-向Cu电极定向移动
8.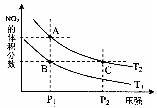 反应N2O4(g)
反应N2O4(g) 2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. A、C两点气体的平均相对分子质量:A > C
D. 由状态B到状态A,可以用加热的方法
7.设阿伏加德罗常数约为6.02×1023mol -1,下列叙述中正确的是
A.足量的锌与一定量的浓硫酸充分反应,放出2.24L气体时,转移电子数约为0.2×6.02×1023
B.常温下,4.4g CO2和N2O混合物中所含有的原子数约为0.3×6.02×1023
C.标准状况下,2.24L乙烷中含有的非极性键数约为0.7×6.02×1023
D.含1mol硅原子的SiO2晶体中Si-O键的个数约为2×6.02×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com