
要研究数列先要知道何为数列,即先要给数列下定义,为帮助同学概括出数列的定义,再给出几列数:
(幻灯片) 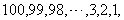 ①
①
自然数排成一列数:
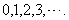 ②
②
3个1排成一列:
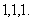 ③
③
无数个1排成一列:
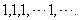 ④
④
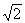 的不足近似值,分别近似到
的不足近似值,分别近似到 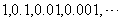 排列起来:
排列起来:
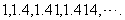 ⑤
⑤
正整数 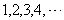 的倒数排成一列数:
的倒数排成一列数:
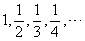 ⑥
⑥
函数 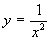 当
当
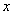 依次取
依次取
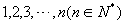 时得到一列数:
时得到一列数:
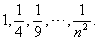 ⑦
⑦
函数 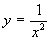 当
当
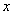 依次取
依次取
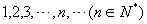 时得到一列数:
时得到一列数:
 ⑧
⑧
请学生观察8列数,说明每列数就是一个数列,数列中的每个数都有自己的特定的位置,这样数列就是按一定顺序排成的一列数.
1.(板书)数列的定义:按一定次序排成的一列数叫做数列.
为表述方便给出几个名称:项,项数,首项(以幻灯片的形式给出).以上述八个数列为例,让学生练习指出某一个数列的首项是多少,第二项是多少,指出某一个数列的一些项的项数.
由此可以看出,给定一个数列,应能够指明第一项是多少,第二项是多少,……,每一项都是确定的,即指明项数,对应的项就确定.所以数列中的每一项与其项数有着对应关系,这与我们学过的函数有密切关系.
(一)数列的概念
今天开始我们研究一个新课题.
先举一个生活中的例子:场地上堆放了一些圆钢,最底下的一层有100根,在其上一层(称作第二层)码放了99根,第三层码放了98根,依此类推,问:最多可放多少层?第57层有多少根?从第1层到第57层一共有多少根?我们不能满足于一层层的去数,而是要但求如何去研究,找出一般规律.实际上我们要研究的是这样的一列数
(板书) 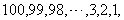 象这样排好队的数就是我们的研究对象--数列.
象这样排好队的数就是我们的研究对象--数列.
(板书)第三章 数列
24.(8分)黄铁矿主要成分是FeS2。某硫酸厂在进行黄铁矿成分测定时,取0.1000g样品在空气中充分灼烧,将生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000mol·L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL。
已知:SO2+2Fe3++2H2O═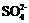 +2Fe2++4H+
+2Fe2++4H+
Cr2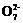 +6Fe2++14H+═2Cr3++6Fe3++7H2O
+6Fe2++14H+═2Cr3++6Fe3++7H2O
(1)样品中FeS2的质量分数是(假设杂质不参加反应) 。
(2)若灼烧6gFeS2产生的SO2全部转化为SO3气体时放出9.83kJ热量,产生的SO3与水全部化合生成H2SO4,放出13.03kJ热量,写出SO3气体转化为H2SO4的热化学方程式 。
(3)煅烧10t上述黄铁矿,理论上产生SO2的体积(标准状况)为 L,制得98%在硫酸质量为 t,SO2全部转化为H2SO4时放出的热量是 kJ。
湖北省黄冈中学2010届高三11月月考化学试题
23.(6分)实验室用50mL浓盐酸跟足量的氯酸钾固体共热制取氯气,反应的化学方程式为(未配平)KClO3+HCl--HCl+Cl2↑+H2O
(1)配平上述反应化学方程式:
KClO3+ HCl-- KCl+ Cl2↑+ H2O
(2)若产生0.1mol Cl2,则转移电子的物质的量为 mol。
(3)若反应中HCl的的利用率只有50%,当氧化产物比还原子能产物多7.1g时,求浓盐
酸的物质的量浓度。
22.(8分)有人设想合成具有以下结构的烃分子。
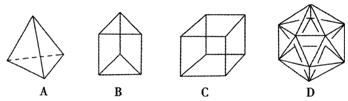
(1)结构D显然是不可能合成的,原因是 。
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构,写出金刚烷的分子式 。
(3)B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是 。
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)C的一种属于芳香烃的同分异构体是生产某塑料的单体,写出合成该塑料的化学方程式 。
21. (5分)德国和美国科学家首次制造出了由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成的(如图所示)。请回答:
(5分)德国和美国科学家首次制造出了由20个碳原子组成的空心笼状分子C20,该笼状结构是由许多正五边形构成的(如图所示)。请回答:
C20分子中共有 个正五边形,共有 条棱边。
C20晶体属于 (填晶体类型)。
20.(8分)有下列转代关系:
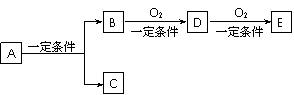
(1)若C是可用来自来水消毒的气体,D、E是氧化物,D能化为E时增加氧的质量是总质量的25.8%,则A是 (写化学式)并写出A在一定条件下生成的C的化学方程式 。
(2)若E是酸酐,且为无色易挥发的晶体,A为气态氢化物,则A与D反应生成B的化学方程式为 。
(3)若C是水,B是无氧化合物,且在同系物中是相对分子质量最小的化合物;E能使紫色石蕊试液显红色,则A的结构简式为 。A、B、D、E中易溶于水的是 。(写结构简式)
(4)写出(3)中下列反应的化学方程式,注明反应类型:
D→E 反应类型为__________。
19.(10分)下表是部分短周期元素的原子半径及主要化合价:
|
元素代号 |
W |
R |
X |
Y |
Z |
Q |
|
原子半径/nm |
0.037 |
0.186 |
0.074 |
0.075 |
0.077 |
0.110 |
|
主要化合价 |
+1 |
+1 |
-2 |
-3,+5 |
+2、+4 |
-3、+5 |
试回答下列问题:
(1)五种元素中原子半径最大的元素在周期表中位置是 。
(2)Y的氢化物比Q的氢化物沸点高的原因是 。
(3)X或与R按1∶1的原子个数比形成化合物甲,甲中存在的化学键有 ;X可与W组成含18e-的化合物乙,则乙的电子式为 ;X可与Z组成一种有恶臭味的气体丙,丙分子中各原子最外层均满足8e-结构,且含有非极性键。1 mol
丙气体可与2 mol氧气完全反应,生成一种气体,且反应前后气体的总体积不变,该生成物能使澄清石灰水变浑浊,请写出丙分子的结构式 。
18.(10分)以下是有关SO2、Cl2的性质实验。
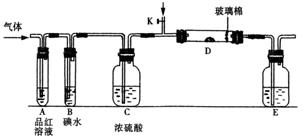 (1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
①若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若置D装的是铁粉,通入Cl2与铁粉充分反应时现象为
;若装置D中装的是五氧化二钒(催化剂)。通入SO2时,打开K通入适量O2的化学反应方程式为 。
②若装置B中装有5.0 mL 1.0×10-3mol/L在碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,该反应的化学方程式为 。
③E中盛有 溶液。
(2)某同学将足量的SO2通入一支装有氧化钡溶液的试管,未见沉淀生成,若向该试管中加入加量(填字母) ,则可以看到白色沉淀产生。
A.氨水 B.稀盐酸 C.稀硝酸 D.氯化钙
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3;当Cl2的与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com