
7. 设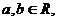 集合
集合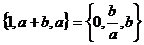 则
则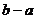 等于
(
)
等于
(
)
A 1 B. 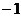 C. 2
D.
C. 2
D.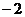
5. 已知全集I={1,2,3,4,5},A∩B={2}, ,则
,则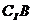 等于
(
)
等于
(
)
A.{3} B.{5} C.{1,2,4} D.{3,5}
6如果函数 对任意实数
对任意实数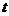 ,都有
,都有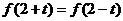 ,则 ( )
,则 ( )
A、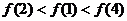 B、
B、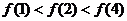
C、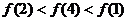 D、
D、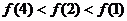
4、若函数是奇函数,当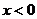 时,
时,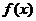 的解析式是
的解析式是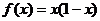 ,则当
,则当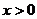 时,
时,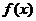 的解析式是
(
)
的解析式是
(
)
A.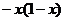 B.
B.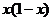 C.
C.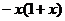 D.
D.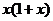
2. 复数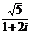 的共轭复数是 ( )
的共轭复数是 ( )
A.1+2i B.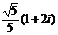 C.1-2i D.
C.1-2i D.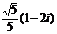
3 函数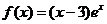 的单调递增区间是 ( )
的单调递增区间是 ( )
A. 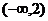 B.(0,3) C.(1,4) D.
B.(0,3) C.(1,4) D. 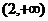
1.已知函数 ,则不等式
,则不等式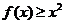 的解集是
( )
的解集是
( )
A 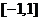 B
B 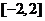 C
C 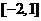 D
D 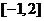
28.(10分)将a
mol的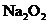 和
和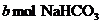 固体混合后,在密闭容器中加热到250℃,让其充分反应,假设
固体混合后,在密闭容器中加热到250℃,让其充分反应,假设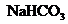 分解产生的
分解产生的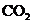 与
与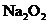 反应完后,
反应完后, 再与
再与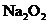 反应.
反应.
(1)当剩余固体为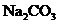 ,排出气体为
,排出气体为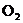 ,
, 时,
时,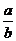 的值为________.
的值为________.
(2)当剩余固体为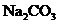 ,NaOH,排出气体为
,NaOH,排出气体为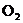 ,
, 时,
时,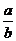 的值为________.
的值为________.
(3)当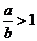 时,剩余固体为________,排出气体为________.
时,剩余固体为________,排出气体为________.
(4)当排出的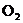 和
和 为等物质的量时,则
为等物质的量时,则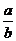 的值为________.
的值为________.
27.(12分)已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为常见的化合物,乙常温下为液体,丙的焰色反应为
黄色,右图为各种物质之间的转化关系。请回答下列问题:
(1)写出下列物质的化学式:A ,B ,D 。
(2)甲的电子式为 ,反应②中若有11.2L(标准状况下)B生成,则发生转移的电子的物质的量为 。
(3)写出反应③的离子方程式: 。

四:计算
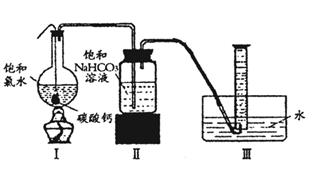 在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
请回答:
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是
。
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少Ag,总共收集到标准状况下的CO2气体BL,发现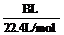 明显小于
明显小于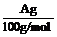 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是________ ________ 。
三:推断题
26、(16分)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M原子最外层电子数与次外层电子数之比为3∶4;N-、Z+、X+离子的半径逐渐减小;化合物XN常温下为气体。据此回答:
(1)M、N的最高价氧化物的水化物中酸性较强的是(写出化学式) 。
(2)Z与M可形成常见固体化合物C,用电子式表示C的形成过程 。
(3)已知通常状况下1g X2在Y2中完全燃烧放出a kJ的热量,请写出表示X2燃烧热的热化学方程式 。
(4)X与Y、X与M均可形成18电子分子,这两种分子在水溶液中反应有黄色沉淀生成,写出该反应的化学方程式 。
(5)化合物A、B均为由上述五种元素中的任意三种元素组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比为1∶1∶1,A溶液中水的电离程度比在纯水中小。则化合物A中的化学键类型为 ;若B为常见家用消毒剂的主要成分,则B的化学式是 。
(6)均由X、Y、Z、M四种元素组成的两种盐发生反应的离子方程式是 ;其中一种是强酸所成的酸式盐,写出Ba(OH)2溶液中逐滴加入该盐溶液至中性的离子方程式 。
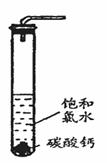 ①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性增强的原因是______ ___________ ____ ________ 。
(2)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有______ __ _ 。
12.(2008·江苏)在平面直角坐标系xOy中,设二次函数f(x)=x2+2x+b(x∈R)的图象与两个坐标轴有三个交点,经过这三点的圆记为C.
(1)求实数b的取值范围;
(2)求圆C的方程;
(3)问圆C是否经过定点(其坐标与b无关)?请证明你的结论.
[解] (1)显然b≠0,否则,二次函数f(x)=x2+2x+b的图象与两个坐标轴只有两个交点(0,0),(-2,0),这与题设不符.
由b≠0知,二次函数f(x)=x2+2x+b的图象与y轴有一个非原点的交点(0,b),
故它与x轴必有两个交点,从而方程x2+2x+b=0有两个不相等的实数根,因此方程的判别式4-4b>0,即b<1.
所以,b的取值范围是(-∞,0)∪(0,1).
(2)由方程x2+2x+b=0,得x=-1±.于是,二次函数f(x)=x2+2x+b的图象与坐标轴的交点是(-1-,0),(-1+,0),(0,b).
设圆C的方程为x2+y2+Dx+Ey+F=0.因圆C过上述三点,将它们的坐标分别代入圆C的方程,得
解上述方程组,因b≠0,得
所以,圆C的方程为x2+y2+2x-(b+1)y+b=0.
(3)圆C过定点,证明如下:
假设圆C过定点(x0,y0)(x0,y0不依赖于b),将该点的坐标代入圆C的方程,并变形为x+y+2x0-y0+b(1-y0)=0.为使x+y+2x0-y0+b(1-y0)=0对所有满足b<1(b≠0)的b都成立必须有1-y0=0,结合x+y+2x0-y0+b(1-y0)=0得x+y+2x0-y0=0.
解得或
经检验知,点(0,1),(-2,1)均在圆C上.
因此,圆C过定点.

亲爱的同学请你写上学习心得
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
___________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com