
5.下列属于配合物的是
A、NH4Cl B、Na2CO3.10H2O
C、CuSO4. 5H2O D、Co(NH3)6Cl3
4.沸腾时只需克服范德华力的液体物质是
A.水 B.酒精 C.溴 D.水银
3.分子有极性分子和非极性分子之分。下列对极性分子和非极性分子的认识正确的是
A.只含非极性键的分子一定是非极性分子
B.含有极性键的分子一定是极性分子
C.非极性分子一定含有非极性键
D.极性分子一定含有极性键
2.以极性键结合的多原子分子,分子是否有极性取决于分子的空间构型。下列分子属极性分子的是
A. H2O B. CO2 C. BCl3 D. NH3
1.下列物质的分子中,所有的原子都在同一平面上的是
A.NH3 B.C3H4 C.甲烷 D.乙烯
33.(7分)将标准状况下的224LHCl溶于635ml(ρ=1.00g/cm3)水中,得到盐酸的密度为 1.20 g/cm3,试求
(1)该盐酸的物质的量浓度
(2)标准状况下,取这种盐酸100ml与足量的NaHCO3溶液反应,放出气体的体积
32.(8分)今欲用NaOH固体配制480mL 0.2mol/L的NaOH溶液。根据题意填空:
(1)配制该溶液应选用 mL容量瓶。
(2)称量时将NaOH放在__________中,用托盘天平称取 g。
(3)若实验时遇到下列情况,将会使所配的溶液浓度发生什么变化(填“偏高”、“偏低”或“无影响”):
A.加水定容时超过刻度线 ;
B.没有将洗涤液转入容量瓶中 ;
C.容量瓶内壁沾有水滴没有烘干就进行配制 ;
D.定容时俯视 ;
31.(4分)选择下列实验方法分离物质,将分离方法的序号填在横线上
A.萃取分液 B.升华 C.蒸发结晶 D.分液 E.蒸馏 F.渗析 G.过滤
(1)______分离饱和食盐水与沙子的混合物。
(2)______从硝酸钾和氯化钠的混合液中获得硝酸钾。
(3)______分离水和汽油的混合物。
(4)______分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
30.(7分)某溶液含有Ba2+、 Cu2+、Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(写出最佳答案):
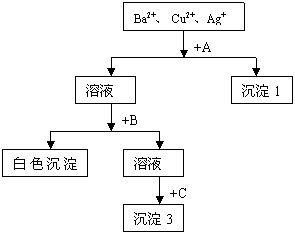
(1)所加试剂的化学式:A_________、B__________、C__________
(2)写出生成沉淀1的离子方程式_________________________;
生成沉淀3的离子方程式_____________________________
29. (6分)用双线桥法表示下列反应的电子转移方向和数目。
(6分)用双线桥法表示下列反应的电子转移方向和数目。
 (1)MnO2+4HCl
(浓) === MnCl2+Cl2↑+2H2O
(1)MnO2+4HCl
(浓) === MnCl2+Cl2↑+2H2O
(2)2KClO3 ==== 2KCl +3 O2↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com