
3.关于“电解氯化铜溶液的pH值变化”问题,化学界有以下两种不同的观点。观点一是:“理论派认为电解氯化铜溶液的pH值升高”;观点二是“实验派经过反复多次精确的试验测定,证明电解氯化铜溶液时,pH的变化如右图曲线所示关系”:
(1)电解氯化铜溶液的pH处于A点位置的原因(用离子方程式说明) ;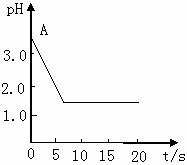
(2)理论派所持观点的理论依据是 ;
(3)实验派的实验结论是 ,他们所述的精确实验是通过 确定的;
(4)你持何种观点?你所持观点的理由是(从化学原理加以简述) 。
答案:(1)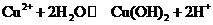
(2)随着CuCl2不断电解,Cu2+浓度减小,H+浓度减小,pH值增大
(3)随着电解,pH值减小
(4)实验派观点;电解产生了Cl2,Cl2溶于水反应生成盐酸和次氯酸,使溶液pH值减小
2.在Na2S溶液中,各微粒浓度间存在下列关系:
(1)c(Na+)+c(H+)=c(OH-)+
(2)c(OH-)=c(H+)+c(HS-)+
(3)c(Na+)=2c(S2-)+
(提示: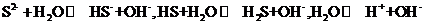 ,溶液中共存在5种带电离子:Na+、H+、S2-、HS-、OH-)
,溶液中共存在5种带电离子:Na+、H+、S2-、HS-、OH-)
答案:(1)c(Na+)+c(H+)=c(OH-)+2c(S2-)+c(HS-)
(2)c(OH-)=c(H+)+c(HS-)+2c(H2S)
(3)c(Na+)=2c(S2-)+2c(HS-)+2c(H2S)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com