
6.
 如图,在光滑水平面上放着两块长度相同、质量分别为M1、M2的木板,在两木板的左端各放一个完全一样的物块,开始时,各物块均静止,今在两物块上各作用一水平恒力F1、F2,当物块和木板分离时,两木板的速度分别为v1、v2,物块和木板间的动摩擦因数相同,下列说法正确的是
如图,在光滑水平面上放着两块长度相同、质量分别为M1、M2的木板,在两木板的左端各放一个完全一样的物块,开始时,各物块均静止,今在两物块上各作用一水平恒力F1、F2,当物块和木板分离时,两木板的速度分别为v1、v2,物块和木板间的动摩擦因数相同,下列说法正确的是
A.若F1=F2,M1>M2,则v1>v2
B.若F1=F2,M1<M2,则v1>v2
C.若F1>F2,M1=M2,则v1>v2
D.若F1<F2,M1=M2,则v1>v2
5. 一个质点正在做匀加速直线运动,用固定在地面上的照相机对该质点进行闪光照相(闪光时间间隔相等),由闪光照片得到的数据,发现质点在第一次、第二次闪光的时间间隔内移动了2m;在第三次、第四次闪光的时间间隔内移动了8m。由此可以求得
A.第一次闪光时质点的速度
B.质点运动的加速度
C.从第二次闪光到第三次闪光这段时间内质点的位移
D.质点运动的初速度
4. 如图所示,两个等大的水平力F分别作用在B和C上.A、B、C都处于静止状态。各接触面与水平地面平行.A、C间的摩擦力大小为f1,B、C间的摩擦力大小为f2,C与地面间的摩擦力大小为f3.则
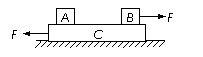 A.f1=0,f2=0,f3=0
A.f1=0,f2=0,f3=0
B.f1=0,f2=F,f3=0
C.f1=F,f2=0,f3=0
D.f1=0,f2=F,f3=F
3.
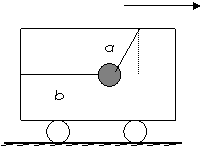 在静止的小车内,用细线a,b系住一个小球.细线a与竖直方向成θ角,拉力Ta;细线b成水平状态,拉力为Tb.现让小车从静止开始向右做匀加速直线运动,如图所示,此时小球在车内的位置仍保持不变(θ角不变).则两细线的拉力变化情况是
在静止的小车内,用细线a,b系住一个小球.细线a与竖直方向成θ角,拉力Ta;细线b成水平状态,拉力为Tb.现让小车从静止开始向右做匀加速直线运动,如图所示,此时小球在车内的位置仍保持不变(θ角不变).则两细线的拉力变化情况是
A.Ta变大,Tb不变 B.Ta变大,Tb变小
C.Ta变大,Tb变大 D.Ta不变,Tb变小
2.
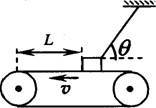 如图所示,质量为m的物体用细绳拴住放在水平粗糙传送带上,物体距传送带左端距离为L,稳定时绳与水平方向的夹角为
如图所示,质量为m的物体用细绳拴住放在水平粗糙传送带上,物体距传送带左端距离为L,稳定时绳与水平方向的夹角为 ,当传送带分别以v1、v2的速度作逆时针转动时(v1<v2),绳中的拉力分别为Fl、F2;若剪断细绳时,物体到达左端的时间分别为tl、t2,则下列说法正确的是
,当传送带分别以v1、v2的速度作逆时针转动时(v1<v2),绳中的拉力分别为Fl、F2;若剪断细绳时,物体到达左端的时间分别为tl、t2,则下列说法正确的是
A.Fl<F2 B.F1=F2
C.tl>t2 D.tl<t2
1. 如图所示,在水平力作用下,木块A、B保持静止。若木块A与B 的接触面是水平的,且F≠0。则关于木块B的受力个数可能是
A . 3个
B . 4个
C . 5 个
D . 6 个
23.(7分)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:
MnO2+4HCI(浓) 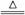 MnCl2+C12↑+2H2O
MnCl2+C12↑+2H2O
取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4L。
请回答下列问题:
(1)该反应的离子方程式为 。
(2)反应中被氧化的HCl的物质的量为 。
(3)实验室备用的浓盐酸质量分数为36.5%,密度为1.19g·cm-3, 为使用方便,请计算出该浓盐酸的物质的量浓度: 。
22.(12分)A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A、C及B、D分别是同一主族元素,B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体。
请回答下列问题:
(1)B、D在周期表中同处在_____族,B的原子结构示意图是_______,下列可以验证B与D两元素原子得电子能力强弱的实验事实是__________(填写编号);
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的原子的电子层数
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢化合的难易
(2)写出两种均含A、B、C、D四种元素的化合物相互间发生反应,且生成气体的离子方程式______________________________________________:
(3)A、B、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有l0个电子,则甲与乙反应的离子方程式为________________;
(4)D元素的气态氢化物和其低价氧化物能反应生成D的单质.该反应中氧化产物与还原产物的物质的量之比为_________________。
21.(6分)三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术创新必不可少的关键原料之一,可由氨气和氟气反应得到:4NH3+3F2 = NF3+3NH4F。则:
(1)上述反应中,氧化剂与还原剂的物质的量之比为_________;若反应中有0.5 mol NH3 被氧化,转移电子的数目为 。
(2)在潮湿的空气中,NF3 能与水蒸气发生氧化还原反应,其反应的产物有:HF、NO和HNO3 ,则在NF3、F2 、NO三种气体中,氧化性由弱到强的顺序为 。
20.(7分)今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、H+、 I-、Mg2+、Ba2+、SO42-、CO32-、NO3-,现取二份各100 mL溶液进行如下实验:
①第一份加足量NaHCO3 溶液,加热后,收集到气体0.05 mol
②第二份加足量BaCl2 溶液,充分反应后过滤干燥,得沉淀4.66 g。
根据上述实验回答
(1)溶液中一定不存在的离子是 ;
(2)溶液中无法确定是否存在的阳离子是 ;
(3)溶液中一定存在的阴离子是 ,其物质的量浓度为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com