
11.若溶液中由水电离产生的c(OH-)=1×10-12 mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
A.Al3+ Na+ NO3- Cl- B.K+ Na+ Cl- NO3-
C.K+ Na+ Cl- AlO2- D.K+ NH4+ SO42- NO3-
10.甲酸的下列性质中,不能证明它是弱电解质的是
A.1mol/L甲酸溶液的pH约为2。
B.甲酸水溶液中同时存在CH3COOH、CH3COO-、H+、OH-
C.10ml 1 mol/L甲酸恰好与10ml 1 mol/L NaOH溶液完全反应。
D.常温下,甲酸钠溶液的pH大于7。
9.用惰性电极电解某金属硫酸盐溶液时,在阴极上析出a g金属,同时在阳极上放出0.8g气体,如果该金属的相对原子质量为b,则其化合价是
A.a·b
B. C.
C. D.
D.
8.下列说法正确的是
①增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞的次数增多 ②有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使有效碰撞的次数增多 ③升高温度,能将化学反应速率增大的主要原因是增加了反应物分子中活化分子的百分数 ④催化剂能增大单位体积内活化分子的百分数,从而成千成万倍的增大反应速率
A.①②③④ B.①②③ C.③④ D.④
7.在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如
下反应:X(g)+2Y(g)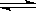 2Z(g) 此反应达到平衡的标志是
2Z(g) 此反应达到平衡的标志是
A.容器内气体密度不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为1:2:2
D.单位时间消耗0.1mol X同时生成0.2mol Z
6.下图为某化学反应速率-时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是
 A.2SO2 (g)+O2 (g)
A.2SO2 (g)+O2 (g)
 2SO3
(g) ;△H<0
2SO3
(g) ;△H<0
B.4NH3 (g)+O2 (g)  4NO(g)+6H2O (g) ;△H<0
4NO(g)+6H2O (g) ;△H<0
C.H2 (g)+I2 (g)  2HI (g) ;△H>0
2HI (g) ;△H>0
D.C (s)+H2O
(g)  CO (g)+H2 (g) ;△H>0
CO (g)+H2 (g) ;△H>0
5.下列各组分子中,都属于含极性键的非极性分子的是
A.CO2、H2S B.CCl4、CH4 C.Cl2、CCl4 D.NH3、HCl
4.已知反应A(g) + 3B(g) == 2C(g) 在某段时间内A的浓度变化的化学反应速率
为1mol/(L min),则此段时间内以C的浓度变化的化学反应速率为
A.0.5 mol/(L min) B.1 mol/(L min) C.2 mol/(L min) D.3 mol/(L min)
3.下列反应中生成物总能量高于反应物总能量的是
A.铝粉与氧化铁粉末反应 B.乙醇燃烧
C.碳酸钙受热分解 D.氧化钙溶于水
2.电解水时为了增强其导电性不应加入的电解质是
A.NaOH B.CuSO4 C.H2SO4 D.KNO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com