
12. 人民代表大会制度与西方议会制的区别是:( )
人民代表大会制度与西方议会制的区别是:( )
①人民代表大会制度实行民主集中制原则;西方议会制实行三权分立的原则
②都属于议会制
③建立的经济基础不同
④都是保证人民当家作主的政权组织形式
A.①②③ B.①③ C.②③④ D.②④
8.有学者指出,传统文化好比一捆干草,人们像驴子一样驮着它走,各人的驮法不同,聪明的人把他们化为养料轻松地走向未来,愚蠢的人把它当作祖传宝贝,永远是沉重的负担。下列选项中与作者观点不相符合的是( )
A.强调我们需要传统文化,要把它化为养料吸收
B.反对把传统文化固化,当作物件加以传承
C.启示人们在文化交流中要勇于重新打造和丰富传统文化
D.暗示在文化交流中对外来文化也要化作养料吸收
7.中国艺术有许多独到之处。以一种文字的书写方式和笔迹的律动,表现出书写者的情绪和审美的追求,从而使文字的书写升华为一种艺术方式,这就是中国书法的精髓。与书法同源的中国画,同样表现出它的独特性,所谓梅兰竹菊的气节、松石的高风,正是艺术的人生写照。这说明( )
①书法、绘画艺术是中华民族之魂 ②中华文化博大精深
③多姿多彩的中华文化展示了中华民族的生命力和创造力 ④中华文化源远流长
A.①② B.②③ C.①④ D.③④
6.《物权法》对相邻建筑物的通风、采光和日照作出明确规定,为公民维护“阳光权”提供了法律依据,这表明在我国
①公民的权利和义务是统一的 ②民主具有广泛性和真实性
③公民的合法权利受到保护 ④公民是国家的主人
A.②③ B.②④ C.①③ D.①④
5.鉴于中国以往的食品安全监管机制不健全的状况,十一届全国人大常委会七次会议通过的《食品安全法》规定:国务院设立食品安全委员会,其工作职责由国务院规定。这说明
A.国家性质决定国家机构性质
B.国家职能决定国家机构设置
C.国家性质决定国家机构设置
D.国家职能决定国家机构职责
4. 某股份有限公司中,10家国有经济的股份占53%,8家集体经济的股份占15%,5 家外资经济的股份占10%。个人股份占5%,并成立了股东代表大会、董事会、监事会等,职权分明,运转协调,该企业的特点是 ( )
A.该企业还没有建立现代企业制度
B.该企业发行的股票可上市交易
C.该企业是一家国有控股企业
D.该企业属于公有制经济
5、(2008北京理综5)据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( D )
A、正极反应式为:O2+2H2O+4e-=4OH-
B、工作一段时间后,电解液中KOH的物质的量不变
C、该燃料电池的总反应方程式为:2H2+O2=2H2O
D、用该电池电解CuCl2溶液,产生2.24 LCl2(标准状况)时,有0.1 mol电子转移
3、(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气和H2O,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:N2H4(l)+O2(g)=N2(g)+2H2O(l) △H=-624kJ·mol-1。
 (2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。肼-空气燃料电池放电时:
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。肼-空气燃料电池放电时:
正极的电极反应式是:O2+2H2O+4e-=4OH-;
负极的电极反应式是:N2H4+4OH――4e-=4H2O+N2↑。
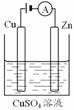
(3)如图是一个电解过程示意图。
1锌片上发生的电极反应式是:Cu2++2e-=Cu。
2假设使用肼-空气燃料电池作为本过程中的电源,铜片质量变化为128g,则肼-空气燃料电池理论上消耗标准状况下的空气112L(假设空气中氧气体积分数为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是:ClO-+2NH3=Cl-+N2H4+H2O。
[高考模拟]4、(2007山东高考)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式2Fe3++Cu=2Fe2++Cu2+。

 (2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应:Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+);
负极反应:Cu-2e-=Cu2+。
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤:①通入足量氯气将Fe2+氧化成Fe3+;②加入CuO调节溶液的pH至3.2-4.7;③过滤(除去Fe(OH)3)。
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
|
提供的药品:Cl2 浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢腐蚀。
有关反应的化学方程式:CuO+H2SO4=CuSO4+H2O、CuSO4+Fe=FeSO4+Cu;
劣质不锈钢腐蚀的实验现象:不锈钢表面有紫红色物质生成。
|
|
酸性 |
碱性 |
|
负极反应式 |
H2-2e-=2H+ |
H2+2OH――2e-=2H2O |
|
正极反应式 |
O2+4H++4e-=2H2O |
O2+2H2O+4e-=4OH- |
|
电池反应式 |
2H2+O2=2H2O |
[基础训练]1、工业上利用氢气在氯气中燃烧,所得产物溶于水的方法制得盐酸,流程复杂且造成能量浪费。有人设想利用原电池原理直接制备盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是( C )
A、两极材料都用石墨,用稀盐酸做电解质溶液
B、通入氢气的电极为原电池的负极
C、电解质溶液中的阴离子向通氯气的电极移动
D、通氯气的电极反应为Cl2+2e-=2Cl-
2、将两个铂电极用导线相连放置在KOH溶液中,然后分别向两极通入CH4和O2,即可产生电流,称为燃料电池,下列叙述正确的是( B )
1通入CH4的电极为正极;2正极的电极反应是O2+2H2O+4e-=4OH-;3通入CH4的电极反应式是CH4+2O2+4e-=CO2+2H2O;4负极的电极反应式是CH4+10OH――8e-=CO32-+7H2O;5放电时溶液中的阳离子向负极移动;6放电时溶液中的阴离子向负极移动。
A、135 B、246 C、456 D、123
(二)充电时:阴极:PbSO4+2e-=Pb+SO42-;
阳极:PbSO4+2H2O-2e-=PbO2+4H++SO42-。
总反应:2PbSO4+2H2O=Pb+PbO2+4H++2SO42-。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com