
2.下面语段中加点的词语,使用不恰当的一项是
日前,金文明先生在《咬文嚼字》上撰文指出,余秋雨在没有任何根据的情况下,强不知以为知,硬说自己将“仁者乐山”的“乐”读成lè并没有错,显然是无稽之谈。当然,余秋雨不是专攻语言的,读错一两个字,本无可非议。问题是分明错了,还要乌龟垫床脚--硬撑,并且编出一套理论来唬人,实在让人不能接受。
A.强不知以为知 B.无稽之谈 C.无可非议 D.乌龟垫床脚--硬撑
1.下列各组词语中加点的字读音完全相同的一组是
A.感喟/匮乏 吝啬/褪色 遒劲/集腋成裘
B.漂白/漂洗 角色/角斗 屏除/屏气凝神
C.祈祷/颀长 梦魇/笑靥 歆羡/万马齐喑
D.拮据/狡黠 隔阂/弹劾 洗濯/擢发难数
19.(17分)铝镁合金已成为飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。
[方案一]
[实验方案]将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。实验中发生反应的化学方程式是 。
[实验步骤]
(1)称取5.4g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中。为使其反应完全,则NaOH溶液的体积应满足关系 。
(2)过滤、洗涤、干燥、称量固体。该步骤中若在空气中微热烘干固体,冷却至室温,测得镁的质量分数将 (填“偏高”、“偏低”或“无影响”)。
[方案二]
[实验方案]将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01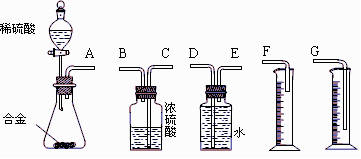 ×105Pa)的体积。
×105Pa)的体积。
[问题讨论]
(1)同学们拟选用下列实验装置完成实验:
①你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶。请你帮助分析原因 。
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 。
 A.待实验装置冷却后再读数
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
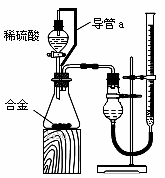
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸 滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
①装置中导管a的作用是 。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为__________mL。
18.(12分)将绿矾(FeSO4·7H2O)、硫酸铵[(NH4)2SO4]以相等物质的量混合可制得摩尔盐[FeSO4·(NH4)2SO4·6H2O]晶体。
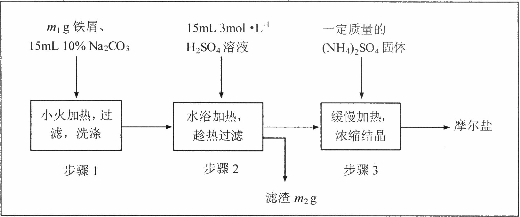
 I.根据上图回答:
I.根据上图回答:
(1)已知油污在热碱性溶液中能溶解。步骤1的目的是除去铁屑上的油污,请用离子方程式简要说明化学原理____________ 。
(2)步骤3在溶液浓缩时不能蒸发至干,为什么?
____________________________________________________________________ 。
(3)制得的晶体过滤后用无水乙醇洗涤而不用蒸馏水,理由是
________________________________________________________________________。
Ⅱ.制摩尔盐的原料之一是硫酸铵,评价硫酸铵化肥的主要指标如下:

某研究性学习小组对某硫酸铵化肥样品进行了如下实验探究:
[观察外观] 该硫酸铵化肥无可见机械杂质。
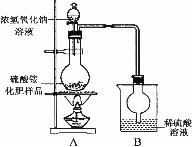
[实验探究] 按图示装置进行实验。
[交流讨论]
(1)甲同学:根据此实验测得的数据,计算的硫酸铵化肥的含氮量可能 (填偏高、偏低、或不影响),实验装置中存在一个明显缺陷是:______________________。
(2)乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液一定要足量并充分加热,原因是___________________________________ 。
[探究结论] 称取27.0g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重6.8g。则该化肥含氮量为______________,由此可判断该化肥的品质。
17.(16分)在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
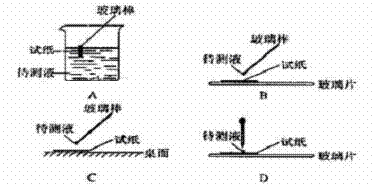
(1)请用学过的化学理论解释步骤③加入Fe粉的目的 ;
(2)写出步骤④中反应的离子方程式 ;若通入少量的氯气,则反应的离子方程式为 。
(3)上述生产流程中,可以循环利用的副产物是 ;
(4)操作⑤的名称是 ,选用的试剂是 。
(5)往操作⑤后的水溶液中再加入适量铁粉,有何现象?
;若改为加入少量现配制的亚硫酸和品红的混合液,有何现象?
,若能反应,写出反应的离子方程式
。(若不能反应,此两空可不填)
(6)往溶液丁中加入氢氧化钠溶液,现象 ,
反应的化学方程式为 。
16.(10分)某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-,取该溶液进行如下实验:
① 用蓝色石蕊试纸检测该溶液,试纸显红色;
② 取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色;
③ 取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④ 取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤ 取实验 ④ 后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:⑴在实验 ① 中,下图所示的操作中正确的是___________(填代号)
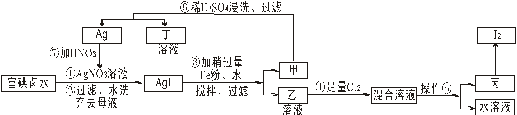
⑵根据上述实验判断原溶液中肯定存在的离子是_______,肯定不存在的离子是________。
⑶写出与②③两个实验有关的离子方程式:
②_____________________________________________________________
③_____________________________________________________________
15.在由Fe、FeO和Fe2O3组成的混合物中加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,并放出448mL气体(标况),此时溶液中无Fe3+。则下列判断正确的是
A.混合物中三种物质反应时消耗盐酸的物质的量之比为1:1:3
B.反应后所得溶液中的Fe2+和Cl-的物质的量之比为1:3
C.混合物中,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多
D.混合物中,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多
14.将质量为w1g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,共收集到标准状况下的气体V1L。向溶液中逐滴加入浓度为amol·L-1的HCl溶液,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加HCl溶液体积为V2L。将溶液蒸干灼烧得固体w2g。下列关系式中不正确的是
A.n(Na)+3n(Al)=2V1/22.4 B.23n(Na)+27n(Al)=w1
C.35.5aV2=w2-w1 D.58.5n(Na)+51n(Al)=w2
13.元素A的单质及A与B形成的化合物能按如下图所示的关系发生转化。则下列说法正确的是
A.A一定是金属元素
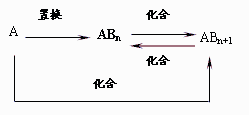 B.当n=1时,A可能是N2
B.当n=1时,A可能是N2
C.图中物质间的转化都是氧化还原反应
D.当n=3时,A可能是Fe
12.现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互关系,图中每条连 线两端的物质可以发生化学反应。下列推断不合理的是
线两端的物质可以发生化学反应。下列推断不合理的是
A.X一定为H2SO4 B.Y一定为K2CO3
C.Z可能是氯水 D.M可能为FeSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com