
12.I2在KI溶液中存在下列平衡: 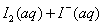

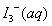 ,某I2、、KI混合溶液中,
,某I2、、KI混合溶液中, 的物质的量浓度c(
的物质的量浓度c( )与温度T的关系如图所示(曲线上任何一点都表示
)与温度T的关系如图所示(曲线上任何一点都表示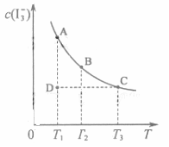 平衡状态)。下列说法正确的是
平衡状态)。下列说法正确的是
A. 反应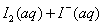

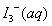 的 △H>0
的 △H>0
B.若温度为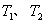 ,反应的平衡常数分别为K1、K2,则K1 < K2
,反应的平衡常数分别为K1、K2,则K1 < K2
C.若反应进行到状态D时,平衡向逆反应方向移动
D.状态B与状态C相比,状态C的c(I2)大
11.难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,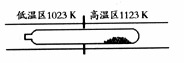 抽真空后引入适量碘并封管,置于加热炉中。反应如下:
抽真空后引入适量碘并封管,置于加热炉中。反应如下:
TaS2
(s)+2I2 (g) 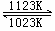 TaI4 (g)+S2 (g) ,下列说法正确的是
TaI4 (g)+S2 (g) ,下列说法正确的是
A.在不同温度区域,TaI4 的量保持不变
B. 在提纯过程中,I2 的量不断减少
C.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区
D. 该反应的平衡常数与TaI4 和S2 的浓度乘积成反比
10.在一定条件下,反应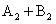
 2AB;△H = Q kJ/mol 的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a为500℃,b为300℃时的情况(其他条件不变),c则为在时刻
2AB;△H = Q kJ/mol 的反应时间与生成物AB的质量分数(AB%)的关系如图所示,其中a为500℃,b为300℃时的情况(其他条件不变),c则为在时刻 开始缩小容器容积(温度维持300℃)的情况,则
开始缩小容器容积(温度维持300℃)的情况,则

A.AB可能为气体 B.A2与B2都为气体 C.Q >0 D.Q <0
9.某探究小组利用丙酮的溴代反应:(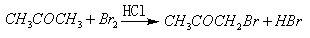 )来研究反应物浓度与反应速率的关系。反应速率
)来研究反应物浓度与反应速率的关系。反应速率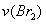 通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验
通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验 数据:
数据:

分析实验数据所得出的结论不正确的是
A. 增大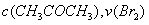 增大 B. 实验②和③的
增大 B. 实验②和③的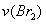 相等
相等
C. 增大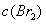 ,
,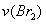 增大
D. 增大
增大
D. 增大
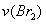 增大
增大
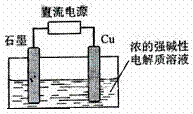
8.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,电解总反应:2Cu+H2O=Cu2O+H2 。下列说法正确的是
。下列说法正确的是
A.石墨电极上产生Cu2O
B.铜电极发生还原反应
C.铜电极接直流电源的负极
D.当有0.1mol电子转移时,有0.05 molCu2O生成。
7.下列说法正确的是 A.在原电池工作时,溶液中的阳离子向负极移动
B.在一定温度下,用惰性电极电解某溶液,若两极分别只有H-2和O2生成,电解一段时间后,该溶液的浓度一定增大
C.要使电解后的CuSO4溶液复原,可向其中加入Cu(OH)2固体
D.在铁表面镀锌时,铁作阴极
6. 右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述正确的是
右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述正确的是
 A.生铁块中的碳是原电池的负极
A.生铁块中的碳是原电池的负极
 B.红墨水柱两边的液面变为左低右高
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe-2e-=Fe2+
D.a试管中发生了析氢腐蚀,b试管中发生了吸氧腐蚀
5.下列有关电池的说法不正确的是
 A.手机上用的锂离子电池属于二次电池
A.手机上用的锂离子电池属于二次电池
 B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极
 C.甲醇燃料电池可把化学能转化为电能
C.甲醇燃料电池可把化学能转化为电能
 D.锌锰干电池中,锌电极是负极
D.锌锰干电池中,锌电极是负极
4.通常情况下,将pH分别为8和10的两种NaOH溶液等体积混合,混合溶液的C( )最接近于
)最接近于
A.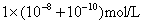 B.
B.
C.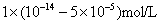 D.
D.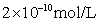
3. 下列说法正确的是
下列说法正确的是
 A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红
A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红
 B.Al3+、NO3- 、Cl-、CO32 -、Na+可大量共存于pH=2的溶液中
B.Al3+、NO3- 、Cl-、CO32 -、Na+可大量共存于pH=2的溶液中
 C.乙醇和乙酸都能溶于水,都是电解质
C.乙醇和乙酸都能溶于水,都是电解质
 D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同
D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com