
2. 用a、b两束单色光分别照射同一双缝干涉装置,在距双缝恒定距离的屏上得到如图所示的干涉图样,其中图甲是用a光照射时形成的,图乙是用b光照射时形成的.则关于a、b两束单色光,下列说法正确的是( )
用a、b两束单色光分别照射同一双缝干涉装置,在距双缝恒定距离的屏上得到如图所示的干涉图样,其中图甲是用a光照射时形成的,图乙是用b光照射时形成的.则关于a、b两束单色光,下列说法正确的是( )
A.a光光子的能量比b光的大
B.在水中,a光传播的速度比b光的大
C.水对a光的折射率比对b光的小
D.b光的波长比a光的短
解析:双缝干涉条纹的间距Δx=λ,由题图可得λa<λb.故选项A正确.
答案:A
1.光的偏振现象说明光是横波,下列现象中,不能反映光的偏振特性的是( )
A.一束自然光相继通过两个偏振片,以光束为轴旋转其中一个偏振片,透射光的强度发生变化
B.一束自然光入射到两种介质的分界面上,当反射光线与折射光线之间的夹角恰好是90°时,反射光是偏振光
C.日落时分,拍摄水面下的景物,在照相机镜头前装上偏振滤光片可以使景像更清晰
D.通过两并在一起的铅笔缝隙观察日光灯,可以看到彩色条纹
答案:D
29. (共1小题,满分8分)
质量分数不同的硫酸溶液其密度不相同,对照表如下:
|
质量分数 |
10% |
20% |
30% |
40% |
50% |
60% |
70% |
80% |
90% |
98% |
|
密度(g/mL) |
1.07 |
1.14 |
1.22 |
1.30 |
1.40 |
1.50 |
1.61 |
1.73 |
1.81 |
1.84 |
将10mL98%浓硫酸中加水稀释至100ml,取10mL该稀硫酸与足量锌反应制取氢气,请按要求完成系列问题的解答(计算结果保留一位小数):
(1)10mL98%的浓硫酸中含18 gH2SO4。
(2)列式计算消耗金属锌的质量。
解:设10mL稀硫酸与锌完全反应消耗锌的质量为x。
Zn+H2SO4=ZnSO4+H2↑
65 98
X
18.0g×
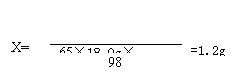
答:略
(3)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是 质量分数越大密度越大 。10mL水和10mL质量分数为b%的硫酸溶液混合,混合后溶液的质量分数应该在  % 至 b% 之间。
% 至 b% 之间。
[提出问题]氢氧化钠是否变质?若发生变质,其程度如何?
[查阅资料]碳酸钠水溶液显碱性,氯化钠、氯化钙水溶液显中性。
[进行试验]Ⅰ.取样品少许,加入稀盐酸有气泡产生;
Ⅱ. 取样品少许,加水溶解后,滴入酚酞显红色;
 Ⅲ.按下图所示过程,进一步实验:
Ⅲ.按下图所示过程,进一步实验:
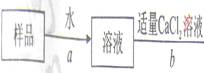
请你与小王同学一道完成下列问题的分析解答:
①氢氧化钠变质的化学反应方程式是 2NaOH+CO2=Na2CO3+H2O 。
②完成步骤a、b实验,都要使用的两件玻璃仪器是 玻璃棒、烧杯 。
③步骤b中,不能用Ca(OH)2代替CaCl2的原因是Ca(OH)2与Na2CO3反应有NaOH生成,会影响对NaOH存在的判断
④根据上述实验,若测定wg样品中氢氧化钠的质量分数,还须测定的数据是C
A.测定沉淀A 的质量
B.溶液B蒸发溶剂,测定残留固体的质量
C.溶液B与稀硫酸中和,测定消耗H2SO4的质量
13.(共2个小题,满分14分)
(1) 图Ⅰ、图Ⅱ是研究燃烧的条件的装置,
试分析后填空:
图Ⅰ实验是利用不同物质在相同温度 条
件下燃烧和不燃烧,来证实可燃物燃烧所需的条件之一:温度达到着火点。
仅用图Ⅱ所示装置就可以证实可燃物必须与氧气(或空气)接触才能燃烧,其做法是: 间歇通入氧气 。
(2)我省有着丰富的天然气资源,许多化肥厂用天然气在高温、催化剂作用下与水

蒸气反应来制备氢气和一氧化碳:CH4+H2O CO+3H2.为了证实该反应所生成的混
合气体的成分,兴趣小组的同学设计了如下图所示装置并进行实验,请你回答下列相关问题:
[实验目的]证实混合气体中含有CO和H2
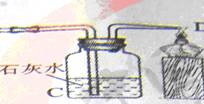

[进行实验]在装置中通入混合气体,点燃酒精灯,如上图所示进行实验
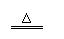 [实验分析]①若要证实混合气体中有CO,应该观察到的现象是石灰水变浑浊,A中黑色粉末变为红色,相关的化学反应方程式是 CO+CuO Cu+CO2
[实验分析]①若要证实混合气体中有CO,应该观察到的现象是石灰水变浑浊,A中黑色粉末变为红色,相关的化学反应方程式是 CO+CuO Cu+CO2
CO2+Ca(OH)2=CaCO3↓+H2O。
②若要证实混合气体中有H2,且是通过装置B验证的,应采用的方法是 称量反应前后装置B的质量并进行比较 。
③有同学认为,根据该混合气体生产的实际情况,混合气体中可能含有水分,因而还应对上述实验装置加以改进。请你提出改进的方案 在装置A前增加除水份装置 。
12.(共2个小题,满分14分)
(1) 目前,我国火力发电厂燃料主要是煤。煤燃烧会排放出SO2和NO2,这些气体不仅污染空气,而且与空气中的物质反应后,生成的物质溶于雨水,会形成“酸雨”。请按要求回答下列问题:
①二氧化硫与空气中水份反应生成亚硫酸(H2SO3),亚硫酸易与氧气反应生成硫酸。其中亚硫酸与氧气的化学方程式是 2H2SO4+O2=2H2SO4 。
②NO2是一种红棕色气体。在盛有NO2的集气瓶中放入一块活性炭,过一会儿,瓶内红棕色变淡甚至消失,活性炭具有的这种性质叫做 吸附性 。
③对于SO2和NO2,小余同学归纳出了如下一些共同点,其中正确的是 AC
A. 都是非金属氧化物 B.硫元素和氮元素化合价都为+2价
C.每个分子都由3个原子构成 D.常温常压下都是有颜色的气体
11.(共2个小题,满分14分)
(1)小李在学校实验室里,发现两瓶失去标签的溶液(标记为A、B),经询问实验员得知是稀硫酸和小苏打溶液。为了区分它们,小李进行了如下实验,请你协助他完成相关问题的解答:
①向A、B两溶液中分别加入适量纯碱,观察到A中有大量气泡,B中没有明显变化现象。A溶液中发生反应的化学方程式是
H2SO4+Na2CO3=Na2SO4+CO2↑+H2O 。
②向A、B两溶液中分别投入生锈的铁钉,观察的到A溶液逐渐变为黄色,铁钉表面有气泡产生,B中没有明显变化现象。则A中所发生化学反应的类型有 复分解反应、置换反应
③向A、B两溶液中分别加入盐酸, A中没有明显变化现象,B中的现象是溶液中有气泡产生
(2)A是一种常见液体,B是最清洁的燃料,它们与C、D、E、F几种物质按下图所示流程进行转化(部分反应条件略去),请按下列要求填空:
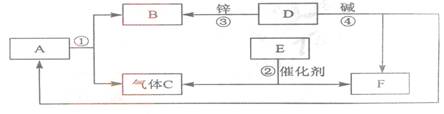
物质D的名称是 稀盐酸 ,转化④中碱的化学式是 KOH
 转化①的化学方程式是2H2O 2H2↑+O2↑,
转化①的化学方程式是2H2O 2H2↑+O2↑,

转化②的化学方程式是 2KClO3 2KCl+3O2↑ 。
10.6.4g某物质R完全燃烧生成8.8gCO2,化学反应方程式是2R+3O2 2CO2+4H2O则由此得出的下列结论,完全正确的一组是( )
2CO2+4H2O则由此得出的下列结论,完全正确的一组是( )
①R由碳、氢两种元素组成
②R中碳元素的质量分数是37.5%
③6.4gR燃烧还生成了7.2gH2O
④R的相对分子质量等于64
A.① ② B. ③④ C.①④ D. ②③
9.欲除去物质中所含少许杂质,所用的方法错误的是( )
|
序号 |
物质 |
杂质 |
除去杂质所用方法 |
|
A |
O2 |
CO2、H2O |
依次通过苛性钠溶液和浓H2SO4 |
|
B |
CO2 |
CO |
通过灼热的铜网 |
|
C |
铜粉 |
铁粉 |
加适量盐酸,反 应后再过滤 |
|
D |
火碱溶液 |
纯碱 |
加适量石灰水,滤去沉淀 |
8.请根据所学化学知识判断,下列①-④做法中正确的是( )
①用碳酸钙粉末做袋装食品的干燥剂
②用甲醛浸泡水产品使之长期不变质
③用氢氧化钠溶液和树叶做“叶脉书签”
④用高分子分离膜淡化海水
A.① ② B. ③④ C.①③ D. ②④
7.上海世博会采用了很多办法来营造“科技世博、生态世博”,以彰显“人、城市、地球”
等理念。小王对上海世博会的下列作法的认识,不正确的是( )
A.用纯电动车、氢燃料电池车、燃乙醇汽油车代替普通燃汽油车--不排放化学物质,实现了“零排放”
B.用玉米淀粉制成玉米塑料、用大豆蛋白制成大豆纤维来代替聚乙烯等塑料--使用可降解材料,能减少“白色污染”
C. 用太阳能光伏电板做成建筑材料,让建筑物的外墙屋顶成为“发电机”--可减少煤、天然气使用量,减轻空气污染
D.升级改造园区污水处理系统,将生活用水、地表雨水分类处理--可减少污染,保护水资源
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com