
3ЃЎЗжЮіЪТР§ЃКдкжаКЭЕЮЖЈВйзїЙ§ГЬжаЃЌЖдгквдЯТИїЯювђВйзїВЛЕБв§Ц№ЕФЪЕбщЮѓ
ВюЃЌгУЁАЦЋИпЁБЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБЕШЬюПеЃК
ЂХЕЮЖЈЙмгУеєСѓЫЎЯДОЛКѓЃЌЮДгУБъзМШмвКШѓЯДЃЌЪЙЕЮЖЈНсЙћ_ЁЁЁЁЁЁЁЁ _ЁЃ
ЂЦзЖаЮЦПгУеєСѓЫЎЯДОЛКѓЃЌгжгУД§ВтШмвКШѓЯДЃЌЪЙЕЮЖЈНсЙћ___ЁЁ ______ЁЃ
ЂЧБъзМвКЕЮЖЈЙмдкЕЮЖЈЧАМтзьДІгаЦјХнЃЌЕЮЖЈжеСЫЮоЦјХнЃЌНсЙћ_______ЁЃ
ЂШЕЮЖЈЧАЦНЪгЃЌЕЮЖЈжеСЫИЉЪгЃЌЪЙЕЮЖЈНсЙћ___________ЁЃ
ЂЩЕЮЖЈЧАбіЪгЃЌЕЮЖЈжеСЫЦНЪгЃЌЪЙЕЮЖЈНсЙћ____________ЁЃ
ЂЪЙ§дчЙРМЦжеЕуЃЌЪЙЕЮЖЈНсЙћ_______________ЁЃ
ЂЫЙ§ЭэЙРМЦжеЕуЃЌЪЙЕЮЖЈНсЙћ_______________ЃЌ
ЂЬгУКЌNa2OдгжЪЕФNaOHЙЬЬхРДХфжЦвбжЊХЈЖШЕФБъзМШмвКЃЌгУгкЕЮЖЈЮДжЊХЈЖШЕФбЮЫсЃЌЪЙВтЕУбЮЫсЕФХЈЖШ___________ЁЃ
ЂЭгУКЌNa2CO3дгжЪЕФNaOHЙЬЬхРДХфжЦвбжЊХЈЖШЕФБъзМШмвКЃЌгУгкЕЮЖЈЮДжЊХЈЖШЕФбЮЫсЃЌЪЙВтЕУбЮЫсЕФХЈЖШ___________ЁЃ
(10)ЯДЕгзЖаЮЦПЪБЃЌЮѓАбЯЁЪГбЮЫЎЕБзіеєСѓЫЎЃЌШЛКѓгУзЖаЮЦПзАД§ВтЕФбЮЫсЃЌгУNaOHБъзМШмвКЕЮЖЈЪБЃЌЖдВтЕУЕФНсЙћ______________ЁЃ
[Р§ЬтНтЮі]
ЁЁ[Р§1] гУ0.1mol/LNaOHШмвКЕЮЖЈ100mlЁЁ 0.1mol/LбЮЫсЪБЃЌШчЙћЕЮЖЈЮѓВюдкЁР0.1%вдФкЃЌЗДгІЭъБЯКѓЃЌШмвКЕФpHЗЖЮЇЮЊ(ЁЁЁЁ )
A.6.9-7.1ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁ B.3.3-10.7 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.4.3-9.7ЁЁЁЁ D.6-8
НтЬтЫМТЗЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
взДэЕуЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
[Р§2] гУжаКЭЕЮЖЈЕФЗНЗЈВтЖЈNaOHКЭNa2CO3ЕФЛьКЯШмвКжаNaOHЕФКЌСПЃЌПЩ
ЯШдкЛьКЯвКжаМгШыЙ§СПЕФBaCl2ШмвКЃЌЪЙNa2CO3ЭъШЋБфГЩBaCO3ГСЕэЃЌШЛКѓ
гУБъзМбЮЫсЕЮЖЈ(гУЗгЬЊзїжИЪОМС).ЪдЛиД№ЃК
(1)ЕЮЖЈЪБBaCO3ФмЗёШмНт?РэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)ШчгУМзЛљГШзіжИЪОМСЃЌдђВтЖЈЕФНсЙћЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
НтЬтЫМТЗЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
взДэЕуЃК ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
[ПМЬтдйЯж]
2.ЗжЮідРэЃКОнcБъЁЄVБъЁЄnБъ=cД§ЁЄVД§ЁЄnД§гаnД§=ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
1.ЁЁЁЁЁЁ ВњЩњЮѓВюЕФвђЫиЃК(1)БъзМШмвКВЛБъзМЁЂЂЦвЧЦїЯДЕгЮДАДвЊЧѓЁЂЂЧЕЮЖЈЙмЦјХнЮДХХОЁЁЂЂШЕЮЖЈЙмЖСЪ§ЗНЗЈВЛе§ШЗЁЂЂЩЕЮЖЈЙмТЉвКЁЂЂЪжеЕуХаЖЯВЛзМЁЂЂЫЕЮЖЈВйзїЙ§ГЬКЭЖСЪ§Й§ПьЕШ
2ЃЎЕЮЖЈЃКЂХгУЁЁЁЁЁЁ ЁЁЁЁвЦШЁвЛЖЈЬхЛ§ЕФЁЁЁЁЁЁ ЕНЁЁЁЁЁЁ жаЃЌМгЁЁЁЁЁЁЁЁ ЃЌдкЦПЕзЕцЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂЦЕЮЖЈЪБзѓЪжЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂгвЪжЁЁЁЁЁЁЁЁЁЁ ЁЂФПЙтзЂЪгЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЧжеЕуХаЖЯЃКЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂШЖСЪ§ЃКзЂвтЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЃ
ЂЩжиИДЕЮЖЈЃКЂйФПЕФЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЂкЕБЕкЖўДЮЖСЪ§гыЕквЛДЮЖСЪ§ЮѓВюКмаЁЪБЃЌЪЧЗёашвЊНјааЕкШ§ДЮЕЮЖЈЁЁЁЁЁЁЁЁЁЁ ЃЌЕБЕкЖўДЮЖСЪ§гыЕквЛДЮЖСЪ§ЮѓВюНЯДѓЪБЃЌгІИУЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ жБЕНЁЁЁЁЁЁЁЁ ЮЊжЙЃЌДЫЪБгІИУШЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ зїЮЊМЦЫуБъзМЁЃ
1ЃЎзМБИЃКЂХЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЂЦЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЂЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЂШЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЂЩЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЂЪЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
3ЃЎЪдМСЃКЂХЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЁЁЁЁЁЁ ЂЦжИЪОМСЕФбЁдёддђЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
2.вЧЦїЃК
ЂХЫсЪНЕЮЖЈЙмЃКЂйЙЙдьЬиЕуЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЂкЯДЕгвЊЧѓЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЂлВЛФмЪЂЗХЕФШмвКЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЦМюЪНЕЮЖЈЙмЃКЂйЙЙдьЬиЕуЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЂ
ЂкЯДЕгвЊЧѓЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЂ
ЂлВЛФмЪЂЗХЕФШмвКЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЧзЖаЮЦПЯДЕгвЊЧѓЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂШЦфЫќгУЕНЕФвЧЦїЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
1.ЫсМюжаКЭЕЮЖЈЃК
ЂХИХФюЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(2)дРэЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂЧЙиМќЃКЂйзМШЗВтЖЈЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂкзМШЗХаЖЯЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
18.ЂХЈC lg 0.11
ЂЦH2SO4ЕФЕквЛМЖЕчРывжжЦСЫHSO4ЃЕФЕчРы
ЂЧДѓгк
ЂШФмЁЃвђЮЊЩњГЩЕФТШЛЏЧтЦјЬхПЩвдВЛЖЯЭбРыЗДгІЬхЯЕ
ЂЩдкетСНжжЮяжЪжаЃЌCu2+ ЖМФмЫЎНтЪЙШмвКГЪЫсадЃЌЖјдкCuSO4 ШмвКжаЃЌSO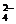 ФмЫЎНтвЛВПЗжВњЩњOHЃЃЌДгЖјЪЙCu2+ ЫЎНтВњЩњЕФЫсадгавЛВПЗжБЛЕжЯћЃЌЖјClO
ФмЫЎНтвЛВПЗжВњЩњOHЃЃЌДгЖјЪЙCu2+ ЫЎНтВњЩњЕФЫсадгавЛВПЗжБЛЕжЯћЃЌЖјClO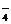 ВЛЛсЗЂЩњЫЎНт
ВЛЛсЗЂЩњЫЎНт
17.SO2ШмНтгкгъЫЎжавЛВПЗжПЊЪММДБЛбѕЛЏЮЊСђЫсЃЌвЛВПЗжШдвдбЧСђЫсДцдкЃЌгъЫЎНЕЯТКѓдкгыПеЦјГфЗжНгДЅЕФЙ§ГЬжаЃЌШѕЫс--бЧСђЫсЛЙЛсБЛбѕЛЏЮЊЧПЫс--СђЫсЃЌЫљвдPHжЕЛсБфаЁЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com