
12.室温时,若0.1mol/L的一元弱碱的电离度为1%,则下列说法正确的是( )
A.该溶液的pH=11
B.该溶液的pH=3
C.加入等体积0.1mol·L-1HCL后所得溶液的pH=7
D.加入等体积0.1mol·L-1HCl后所得溶液的pH>7
11.已知NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液pH为2。对于该溶液下列叙述中不正确的是( )
A.该温度高于25℃ B.水电离出来的c(H+)=1×10-10mol/L
C.c(H+)=c(OH-)+c(SO42-) D.该温度下加入等体积pH为12的NaOH溶液后恰好呈中性
10.pH = 2的A、B两种酸溶液各1mL, 分别加水稀释到1000mL, 其溶液的pH与溶液体积(V)的关系如右图所示,则下列说法正确的是
A.A、B两种酸溶液物质的量浓度一定相等
B.稀释后A酸溶液的酸性比B酸溶液强
C.a = 5时, A是强酸, B是弱酸
D.若A、B都是弱酸, 则5 > a > 2
9.在0.01mol/L的醋酸中加入少量硫酸后,其变化结果是( )
A.酸性增强,pH减小 B.醋酸的浓度减小
C.氢离子浓度变小 D.醋酸根离子浓度变小
8.pH=3的盐酸和pH=3的醋酸溶液,由水电离产生的c(H+) ( )
A.前者大于后者 B.前者小于后者 C.前者等于后者 D.不能确定
B.提高训练
7.pH相同的醋酸溶液和盐酸分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相同,则m、n的关系是( )
A.m=n B.m>n C.m<n D.无法判断
6.在平衡体系中,H2S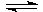 H++HS-,HS-
H++HS-,HS-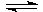 H++S2-中,增大溶液的pH,则c(S2-) ( )
H++S2-中,增大溶液的pH,则c(S2-) ( )
A 增大 B 不变 C 减小 D 可能增大可能减小
5.把0.05molNaOH固体分别加入下列100mL液体中,溶液的导电性基本不变的是 ( )
A.自来水 B. 0.5mol·L-1的盐酸 C. 0.5mol·L-1的醋酸 D. 0.5mol·L-1的氨水
4.用pH试纸测定某无色溶液的pH值时,规范的操作是 ( )
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上跟标准比色卡比较
D.在试管内放入少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
3.当一定浓度的醋酸溶液在不同温度下测其H+离子浓度,其结果是 ( )
A.缺少限制条件,无法测定 B.H+离子浓度相同
C.温度低时,H+离子浓度大 D.温度高时,H+离子浓度大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com