
1. AD 2.AC
[针对训练]
2.[解析] 设此条件下HA的电离度为x,则根据电离平衡方程式计算如下:
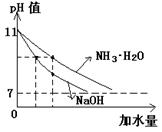
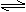 HA H+ + A-
HA H+ + A-
起始物质的量(mol): c 0 0
平衡物质的量(mol): c(1-x) cx cx
据题意有关系式:c+cx=cn 解出x,答案为C
[答案] C
[考题再现]
1.[解析]当溶液的体积和PH值均相同时,弱酸的物质的量最大,与足量金属反应时放出氢气最多,虽然硝酸与盐酸的物质的量相同,但是硝酸和任何金属反应都不放出氢气,所以答案只能选B
[答案] B
19. 用有关理论解释下列事实:甲学生在制得Mg(OH)2沉淀中加入浓氯化铵溶液,结果沉淀完全溶解,乙学生在制得的Mg(OH)2沉淀中加入浓醋酸铵溶液,结果沉淀也完全溶解。
第十章 电离平衡
第一课时 电离平衡
[例题解析]
18.现有下列两组溶液(Ⅰ)组:0.1mol/L的醋酸和盐酸,(Ⅱ)组:pH值=11
的氨水和氢氧化钠溶液。若将它们加水稀释相同的倍数,试比较(Ⅰ)组和(Ⅱ)组
溶液pH值的大小:(Ⅰ)组________,(Ⅱ)组___________。

D.奥赛一瞥
17.常温下将0.010molCH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液,判断:
①溶液中共有________种微粒(包括分子和离子);
②溶液中有两种微粒的物质的量之和一定等于0.010mol,它们是______和_______;
③溶液中n(CH3COO-)+ n(OH-)-n(H+)=_____________mol。
16.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A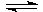 H++HA-,
H++HA-,
HA-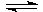 H++A2-,设有下列四种溶液:
H++A2-,设有下列四种溶液:
A. 0.01mol/L的H2A溶液
B.0.01mol/L的NaHA溶液
C.0.01mol/L的HCl与0.04mol/L的NaHA溶液等体积混合液
D.0.02mol/L的NaOH与0.O2 mol/L的NaHA溶液等体积混合液
据此,填写下列空白(填代号)
(1)c(H+)最大的是______________________,最小的是___________________.
(2)c(H2A)最大的是______________________,最小的是___________________.
(3)c(A2-)最大的是______________________,最小的是___________________.
15.用下列方法测定空气的污染物含量:将一定体积的空气通入吸收剂,并测定其电导的变化(导体电阻越小,它电导越大)。如测定H2S的含量,若用CuSO4溶液吸收,可测定很大浓度范围内的H2S,但电导变化不大,若用浓溴水吸收,仅限于低浓度范围内的H2S,但有很高的灵敏度。现要兼顾吸收容量与灵敏度,测定空气中Cl2的含量,则应选用下列吸收剂中的
A .Na2SO3 B. KI溶液 C. NaOH溶液 D. H2O
C.能力训练
14.若室温时pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为
A.10(a+b-12)% B.10(a+b-14)% C.10(12-a-b)% D.10(14-a-b)%
13.常温下,强酸溶液A和强碱溶液B的pH之和为16,当它们按一定体积比混合时,溶液的pH恰好等于7,则A与B的体积比是( )
A. 1︰10 B. 10︰1 C. 1︰100 D. 100︰1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com