
15.一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g)△H<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g)△H<0。现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
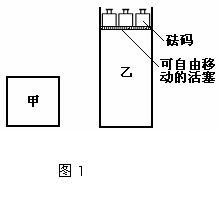
下列关于两容器中反应的说法正确的是 ( )
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成不相同,混合气体平均相对分子质量也相同
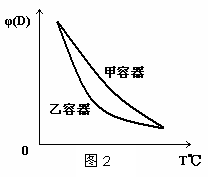
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
第Ⅱ卷(非选择题,共66分)
14.用石墨做电极电解AlCl3溶液时,下列电解液变化曲线合理的是 ( )

12.25℃时,下列各溶液中有关物质的量浓度关系正确的是 ( )
A.c(NH+4)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl)
B.Na2CO3溶液中:2c(Na+)=c(CO2-3)+c(HCO-3)+c(H2CO3)
C.NH4HSO4溶液中滴加NaOH至溶液恰好呈中性:
c(Na+)>c(SO2-4)>c(NH+4)>c(OH-)=c(H+)
D.pH相同的CH3COONa溶液、C6H5ONa、溶液Na2CO3溶液、NaOH溶液:
c(CH3COONa)<c(Na2CO3)<c(C6H5Na)<c(NaOH)
 13.某容积一定的密闭容器中,可逆反应:
13.某容积一定的密闭容器中,可逆反应:
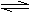 A(g)+B(g) xC(g)△H<0,符合下
A(g)+B(g) xC(g)△H<0,符合下
图所示图象(1)的关系。由此推断
对图象(2)的正确说法是( )
A.P3>P4,Y轴表示A的转化率
B.P3<P4,Y轴表示B的百分含量
C.P3>P4,Y轴表示混合气体密度
D.P3>P4,Y轴表示混合气体的平均摩尔质量
11.下列有关实验说法错误的是 ( )
A.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度
B.用10mL量筒量取5.80mL盐酸
C.做完银镜实验的试管应用稀硝酸洗涤
D.向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,以制备Fe(OH)3胶体
10.草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10mL 0.01mol·L-1NaHC2O4溶液中滴加0.01mol·L-1NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是 ( )
A.V(NaOH) = 0时,c(H+)=1×102mol·L-1
B.V(NaOH) <10mL时, 不可能存在c(Na+)=2c(C2O42 -)+c(HC2O4- )
C.V(NaOH) = 10 mL时, c(H+) = 1×10-7mol·L-1
D.V(NaOH)>10 mL时,c(Na+)>c(C2O42 -)>c(HC2O4- )
9. 我国镍氢电池居世界先进水平,国产大功率镍氢动力电池已广泛用于我海军潜艇。常见镍氢电池的某极是储氢合金LaNi5,电池的总反应为:
LaNi5H6 +
6NiO(OH)  LaNi5 + 6Ni(OH)2(LaNi5H6中各元素化合价均为零),
LaNi5 + 6Ni(OH)2(LaNi5H6中各元素化合价均为零),
下列说法正确的是 ( )
A.放电时储氢合金作正极
B.充电时储氢合金作阴极
C.放电时,电流由负极通过外电路流向正极
D.充电时阴极反应:Ni(OH)2 + OH――e-= NiO(OH)+H2O
8.25℃时,在含有大量Ba2+的某澄清透明溶液中,由水电离产生的OH-物质的量浓度为
1×10-12mol/L,则在此溶液中还可能大量共存的离子组有 ( )
A.Na+、Fe2+、NO-3 B.K+、CH3COO-、SO2-4
C.NH+4、HCO-3、SCN- D.Cu2+、Mg2+、Cl-
7.下列说法不正确的是 ( )
A.根据沸点差异可以判断两种液体混合物是否可用蒸馏方法进行分离
B.根据固体溶解度曲线可以判断物质结晶的方法
C.根据熵变可以判断所有化学反应能否自发进行
D.根据化学平衡常数可以判断化学反应进行的限度
6.11.9g金属锡跟100mL 12mol·L-1 HNO3共热一段时间。完全反应后测定溶液中c(H+)为8mol·L-1,溶液体积仍为100mL。放出的气体在标准状况下体积约为8.96L。由此推断氯化产物可能是 ( )
A.SnO2·4H2O B.Sn(NO3)4
C.Sn(NO3)2 D.Sn(NO3)2和Sn(NO3)4
5.下列反应的离子方程式正确的是 ( )
|
A.以石墨作电极电解MgCl2溶液:2Cl-+2H2O ===== H2↑+Cl2↑+2OH-
B.在强碱溶液中次氯酸钠与Fe(OH)3生成Na2FeO4:
3ClO-+2Fe(OH)3=2FeO2-4+3Cl-+H2O+4H+
C.溴化亚铁溶液中加入过量氯水:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2
D.向稀氨水中加入稀盐酸:NH3·H2O+H+=NH+4+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com