
(二)电解总反应式
1、在确保两极转移电子数目相同的条件下,将两电极反应式合并即得总反应式。
2、总反应式要注明条件:通电。若电解的H+或OH-来自于H2O,方程式中要以水分子的形式书写。
[基础训练]
1、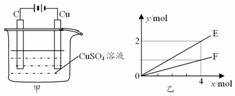 按如下图甲所示装置进行实验,若图乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是( D )
按如下图甲所示装置进行实验,若图乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是( D )
A、E表示生成铜的物质的量
B、E表示反应消耗水的物质的量
C、F表示反应生成氧气的物质的量
 D、F表示生成硫酸的物质的量
D、F表示生成硫酸的物质的量
2、食盐有广泛的用途:
 (1)写出电解饱和食盐水的离子方程式:
(1)写出电解饱和食盐水的离子方程式:
2Cl-+2H2O 2OH-+H2↑+Cl2↑。
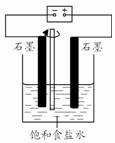
(2)用如图所示装置电解500mL2mol·L-1的食盐水可制得一种消毒液,在通电过程中不断搅拌溶液(使阳极产物全部溶解在溶液中)溶液的pH(填写字母)A。
A、逐渐增大 B、逐渐减少 C、保持不变
当阳极有氧气生成时停止通电,最终所得溶液中溶质的主要成分是NaClO;
假设电解过程中阳极产物无逸出,溶液加水至500mL,消毒液的浓度是2mol·L-1。
(3)向上述制取的消毒液中通入CO2气体,可以增强消毒效果,写出反应的离子方程式:
2ClO-+CO2+H2O=2HClO+CO32-。
3、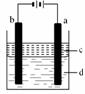 因Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,应用下图电解实验可以制得白色纯净的Fe(OH)2沉淀。两电极材料分别为石墨和铁。
因Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀,应用下图电解实验可以制得白色纯净的Fe(OH)2沉淀。两电极材料分别为石墨和铁。
(1)a电极材料应为Fe,电极反应式为Fe-2e-=Fe2+。
(2)电解液d可以是B、C(填编号)。
A、纯水 B、NaCl溶液 C、NaOH溶液 D、CuCl2溶液
(3)c为苯,其作用是:隔绝空气、防止Fe2+被空气氧化。
在加入苯之前对d应作何简单处理:将d煮沸,赶走d中溶有的氧气。
(4)若d为Na2SO4溶液,当电解一段时间看到白色Fe(OH)2沉淀后,再反接电源电解,除了电极上看到气泡外,混合物中另一明显现象为白色沉淀迅速变为灰绿色,最后变为红褐色沉淀。
[高考模拟]
4、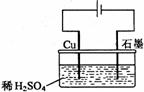 (2007江苏化学11)(多选)某同学按右图所示的装置进行电解实验。下列说法正确的是( BC )
(2007江苏化学11)(多选)某同学按右图所示的装置进行电解实验。下列说法正确的是( BC )
A、电解过程中,铜电极上有H2产生
B、电解初期,主反应方程式为:Cu+H2SO4
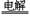 CuSO4+H2↑
CuSO4+H2↑
C、电解一定时间后,石墨电极上有铜析出
D、整个电解过程中,H+的浓度不断增大
5、(2008天津理综26)W、X、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
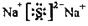 (1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O。
(2)W与Y可形成化合物W2Y,该化合物的电子式为______________。
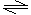 (3)X的硝酸盐水溶液显酸性,用离子方程式解释原因:Al3++3H2O Al(OH)3+3H+。
(3)X的硝酸盐水溶液显酸性,用离子方程式解释原因:Al3++3H2O Al(OH)3+3H+。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为:SO2+Cl2+2H2O=H2SO4+2HCl。
(5)比较Y、Z气态氢化物的稳定性:HCl >H2S(用分子式表示)。
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是S2->Cl->Na+>Al3+。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出Q kJ的热量。写出该反应的热化学方程式:Cl2O7(l)+H2O(l)=2HClO4(aq) ΔH=-4QkJ/mol。
(一)电极反应式
1、确定电极:与电源正极相连的为阳极,与电源负极相连的为阴极。
2、确定电极反应:阳极发生氧化反应。若是活泼金属电极,电极材料放电,若是惰性电极,溶液中阴离子放电。阴极发生还原反应,溶液中的阳离子放电。
3、写电极反应式:根据电极反应分别写出两极反应式。
(二)阴极产物的判断
直接根据阳离子放电顺序进行判断。阳离子放电顺序:Ag+>Hg2+>Fe3+>Cu2+>H+[c(H+)较大]>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+。若金属阳离子(Fe3+除外)放电则得到相应金属单质,若H+放电,则得H2。
(一)阳极产物的判断
1、首先看电极,如果是活性电极(除Au、Pt、石墨以外的金属材料作电极)则电极材料失电子,电极被溶解,溶液中阴离子不能失电子。
2、如果是惰性电极(Pt、Au、石墨)则要再看溶液中阴离子的失电子能力,此时依据阴离子放电顺序加以判断。阴离子放电顺序:S2->I->Br->Cl->OH->高价含氧酸根(SO42-、NO3-等)>F-。若S2-、I-、Br-、Cl-放电,产物是S、I2、Br2、Cl2;若OH-放电,则得H2O和O2。
30.D A.“交到有关部门,”此处的逗号应改为句号,否则句意不明确;B.“力量”,此处的逗号应改为句号或冒号;C.括号里的内容为补充说明,不是解释“详细地址”,应放在句号外。
29.B A项,去掉冒号,“预防为主,治疗为辅”加上引号;C项,括号应在逗号前;D项,“于何处”后应为问号。
28.C A项,“说”后的冒号应该为逗号;B项,从表面上看,冒号后面的内容,全是提示的范围,其实不然,这里提示的只是两句诗,应将冒号改为逗号,或将逗号改为引号内句号;D项,括号的内容是对“斑斑”的解释,应紧接在“斑斑”后,放在逗号前面。
27.C A项前一个问号改为逗号,后一个问号改为句号。因为全句为陈述语气。B项后引号里的句号去掉,因为引用部分是句子的成分。D项句末的句号应放在引号里面,因为两个引号里的话都是一个人说的,是独立引用。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com