
15.在一定条件下,将1molCO和1mol水蒸气通入某密闭容器中发生反应:
CO(g)+H2O(g) CO2 (g) +H2(g),达到平衡时生成0.7mol CO2。若条件不变,开始时加入1molCO和4mol水蒸气,则达到平衡时生成CO2的物质的量可能为
CO2 (g) +H2(g),达到平衡时生成0.7mol CO2。若条件不变,开始时加入1molCO和4mol水蒸气,则达到平衡时生成CO2的物质的量可能为
A.0.6mol B.0.9mol C.1.0mol D.1.5mol
14.在一密闭容器中进行下列反应:A(g) + B(g)  2C(?) +D(g),此反应符合下列两个图象,则下列叙述正确的是
2C(?) +D(g),此反应符合下列两个图象,则下列叙述正确的是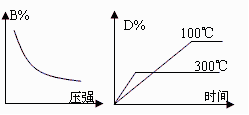
A.正反应为吸热反应,C是固体或液体
B.正反应为吸热反应,C是气体
C.正反应为放热反应,C是气体
D.正反应为放热反应,C是固体或液体
13.某温度下,在容积固定的密闭容器中发生可逆反应A(g) + 2B(g)=2C(g),达到平衡时,各物质的浓度之比为c(A):c(B):c(C)=1:1:2,保持温度不变,以1:1:2的体积比再充人A、B、C,则下列叙述正确的是
A.刚充入时反应速率v(正)减小,v(逆)增大
B.达到新的平衡时,反应混合物中C的体积分数不变
C.达到新的平衡时,c(A):c(B):c(C)仍为1:1:2
D.达到新的平衡过程中,体系压强先增大,后逐渐减小
12.下列有关氨的说法中不正确的是
A.NH3是4核10电子极性分子,三角锥型,具有还原性
B.NH3极易溶于水,可做喷泉实验,氨气易液化,液氨可用作制冷剂
C.氨气是非电解质,氨水是电解质
D.沾有浓盐酸的玻璃棒遇氨气可产生白烟
11.下列关于平衡体系的各说法中不正确的是
A.在N2+3H2 2NH3的平衡体系中,缩小体积,平衡向右移动,氨的产率增加
2NH3的平衡体系中,缩小体积,平衡向右移动,氨的产率增加
B.在CH3COOH CH3COO-+H+的平衡体系中加入CH3COONa固体,平衡向左移动
CH3COO-+H+的平衡体系中加入CH3COONa固体,平衡向左移动
C.在H2S H++HS-的平衡体系升温到100℃时,溶液中的c(H+)一定增大
H++HS-的平衡体系升温到100℃时,溶液中的c(H+)一定增大
D.在盐酸中加入KCl晶体,溶液pH不变
10.在溶液中能大量共存的一组离子或分子是
A.NH4+、OH-、NO3-、CO32- B.K+ 、Al3+、SO42- 、NH3·H2O
C.Fe2+、K+、H+、NO3- D.Na+ 、CH3COO-、CO32-、OH-
9.将0.1molN2O4置于1L密闭烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体渐渐变为红棕色:N2O4﹝g﹞ 2NO2﹝g﹞。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2﹝g﹞。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
A.烧瓶内气体的颜色不再发生变化
B.N2O4的消耗速率与NO2的生成速率之比为1︰2
C.NO2的生成速率与NO2的消耗速率相等
D.烧瓶内的压强不再随时间发生变化
8.NO和CO都是汽车尾气中的物质,它们能很缓慢地反应生成N2和CO2,对此反应有关的叙述中不正确的是
A.增大压强有利于NO和CO反应 B.使用适当催化剂可以加快化学反应速率
C.升高温度能加快化学反应速率 D.改变压强对化学反应速率没有影响
7.下列事实,不能用勒夏特列原理解释的是
A.在溴水中存在如下平衡:Br2+H2O
 HBr+HBrO,当加入NaOH溶液后颜色变浅
HBr+HBrO,当加入NaOH溶液后颜色变浅
B.对2HI H2+I2(g),平衡体系增加压强使颜色变深
H2+I2(g),平衡体系增加压强使颜色变深
C.反应CO+NO2 CO2+NO(正反应放热),升高温度使平衡向逆向移动
CO2+NO(正反应放热),升高温度使平衡向逆向移动
D.合成氨反应:N2+3H2 2NH3(正反应放热),为提高氨的产率,理论上应采取低温高压的措施
2NH3(正反应放热),为提高氨的产率,理论上应采取低温高压的措施
6.下列叙述正确的是
A.检验某稀溶液中是否含有NO3-,可先将溶液浓缩,然后加入浓H2SO4和铜片,观察有无红棕色气体产生
B.鉴别NO2和溴蒸气可用湿润的淀粉-KI试纸
C.检验溶液中是否含Cl-,可加入AgNO3溶液,观察有无白色沉淀生成
D.检验溶液中是否含NH4+,可加入足量NaOH溶液,加热,再用湿润的红色石蕊试纸伸入试管内检验是否变蓝
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com