
18.解析 由题可知
2HxA+xCaCO3=CaxA2+xCO2+xH2O
或HxA+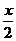 CaCO3=Ca
CaCO3=Ca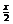 A+
A+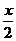 CO2+
CO2+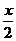 H2O
H2O
HxA与CaCO3的物质的量之比为2∶1,∴x=1
∴气态氢化物为HA型,又∴M=1.629×22.4=36.5,A的相对原子质量为35.5,应为Cl,氯元素
H-A即为H-Cl应是极性键,HA为极性分子。
17..(1)S、P、Cl、O、Se (2)稳定性:H2O>H2S>H2Se (3)SO2,极性分子 SO3非极性分子
16.
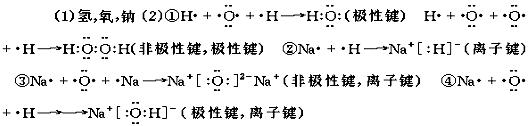
14.B
15.(1) (2)NaOH
(2)NaOH 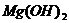 (3)均为极性分子 (4)
(3)均为极性分子 (4)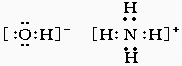
9.D 10.B 11.BC 12.BD 13.A
1.C 2.AD 3.CD 4.AD 5.B 6.BC 7.C 8.B
2.
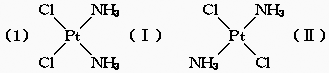
(2)Ⅱ中结构对称,分子无极性,由相似相溶原理可知
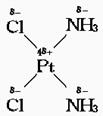 由于N-Pt、Cl-Pt键长不同,
由于N-Pt、Cl-Pt键长不同,
∴两个Cl-的负电荷重心与两个N的负电荷重心无法重合,分子有极性;而Ⅱ中两个Cl的负电荷重心落在Pt上,两个N的负电荷重心也落在Pt上,所以正负电荷重心可以重合,分子无极性。
[针对训练]
1. (1)C
Na O Cl
(2)直线型 非极性 正四面体型 非极性 (3)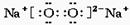 离子化合物
离子化合物
2.[解析]单质分子都是非极性键构成的非极性分子;在化合物分子中,可由极性键形成非极性分子,也可形成极性分子;铵盐是离子化合物,都可由非金属元素形成。
[答案] (1)NH3、H2O (2)O2、N2 (3)SiCl4、CO2 (4)(NH4)2SO4
[考题再现]
1.[解析]根据(CN)2分子的对称性和180度的键角这两个已知条件,即可推知其电子式,并知其为非极性分子,再据其与氯气的性质相似,可写出与碱反应的方程式。
[答案] 15.(1)(CN)2+2OH-=CN-+CNO-+H2O (2) 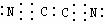
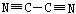 非极性 (3)14
非极性 (3)14 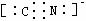
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com