
21、(10分)A、B、C、D、E是原子序数小于18的五种元素,且原子序数依次增大,其中A与B原子的最外层电子数相同,B、C、D、E位于同一周期,D原子的最外层电子数与电子层数相同,E- 与Ar原子的核外电子排布相同。
(1)E显+1价含氧酸的化学式为 。
(2)B的最高价氧化物的水化物与D的最高价氧化物的水化物相互反应的化学方程式为
。
(3)在常温下,D与E形成的化合物的水溶液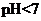 ,原因是
(用离子方程式表示)。
,原因是
(用离子方程式表示)。
(4)常温常压下, 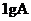 的单质在E的单质中完全燃烧,生成共价化合物,并放出
的单质在E的单质中完全燃烧,生成共价化合物,并放出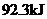 的热量,该反应的热化学方程式为
。
的热量,该反应的热化学方程式为
。
(5)将C与E组成的化合物溶于水配成溶液,用惰性电极进行电解,阴极的还原产物与阳极的氧化产物的物质的量之比为 。
20、pH=1的两种一元酸HX与HY溶液,分别取50mL加入足量的镁粉,充分反应后,收集到H2体积分别为V(HX)和V(HY)。若V(HX)>V(HY),则下列说法正确的是( )
A、HX可能是强酸
B、HX的酸性比HY的酸性弱
C、两酸的浓度大小c(HX)<c(HY)
D、将两种一元酸均稀释100倍,稀释后两溶液的pH均为3
第二卷:非选择题(共60分)
19、下列实验问题处理方法错误的是( )
① 用pH试纸测溶液pH时,将试纸用水润湿再蘸取待测液
② 实验中,点燃CO前应首先检验CO的纯度
③ 实验结束后,可将所有的废液倒入下水道排出实验室
④ 给试管中的液体加热时加入碎瓷片,以免暴沸伤人
⑤ 测定硫酸铜结晶水含量时,将晶体加热至白色,然后冷却、称重即可计算
⑥ 配制稀硫酸时,先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
A.①② B. ②④⑤ C.①③⑤ D.②④⑥
17、L-多巴是一种有机物,可用于帕金森综合症的治疗,其结构简式如下:
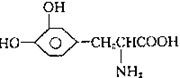
下列关于L-多巴的叙述中不正确的是 ( )
A.长期暴露在空气中易变质 B.既有酸性,又有碱性
C.一定条件下能发生聚合反应 D.分子中最多只有6个碳原子共平面
18、广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述信息,下列说法不正确的是( )
A、CaO2的水解产物是Ca(OH)2和H2O2 B、PCl3的水解产物是HClO和PH3
C、NaClO的水解产物之一是HClO D、Mg3N2的水解产物是两种碱性物质
16、工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)===Si(s)+4HCl(g);△H=+QkJ·mol-1(Q>0)
某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.反应至4min时,若HCl的浓度为0.12mol·L-1,则H2的反应速率为0.03mol/(L·min)
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH恰好反应
15、进行化学实验或探究活动,都必须注意实验安全。下列实验操作合理的是( )
A.为防止试管破裂,加热固体高锰酸钾制氧气时,试管口应向下倾斜
B.进行SO2性质探究实验时,多余的SO2应排到实验室外
C.为防止药品污染,实验结束后,用剩的白磷可溶解于CS2后倒入垃圾箱
D.配制H2SO4溶液时,先在量筒中加一定体积的水,再在搅拌下慢慢加入浓H2SO4
14、对胶体稳定不起作用的是( )
A、胶体微粒直径介于溶液与浊液之间 B、胶体微粒具有吸附作用
C、丁达尔现象 D、布朗运动
13、下列离子反应方程式书写正确的是( )
A、在Ba(OH)2溶液中加入少量的硫酸氢钠溶液:
Ba2++2OH-+2H++SO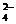 =BaSO4↓+2H2O
=BaSO4↓+2H2O
B、向次氯酸钙溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
C、标准状况下,将112mLCl2缓慢注入10mL 1mol·L-1的FeBr2溶液中:
2Fe2++4Br-+3Cl2 =2Fe3++6Cl-+2Br2
D、向苯酚钠溶液中通入少量CO2气体:
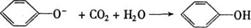 + HCO
+ HCO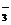
12、下列反应的ΔH表示的是中和热的是:( )
A、H2SO4(aq) + Ba(OH)2(aq) == BaSO4(s) + 2H2O(l ) ; ΔH1
B、H2SO4(浓aq) + NaOH(aq) == Na2SO4(aq) + H2O(l); ΔH2
C、HCl(aq) + NaOH(aq) == NaCl(aq) + H2O(l); ΔH3
D、HAc(aq) + NaOH(aq) == NaAc(aq) + H2O(l); ΔH4
11、某无色澄清溶液与NH4HCO3在一定条件下作用能产生气体,则在此溶液中肯定能大量共存的离子组是( )
A. MnO4-、Mg2+、Cl-、SO42-
B.Na+、Ba2+、NO3-、SO42-
C.Cl-、Na+、K+、SO42-
D.K+、NO3-、SO42-、Al3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com