
7、以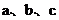 依次表示方程
依次表示方程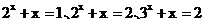 的根,则
的根,则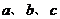 的大小顺序为
的大小顺序为
A.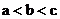 B.
B. C.
C. D.
D.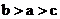
6、各项都是正数的等比数列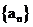 的公比
的公比 ,且
,且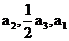 成等差数列,则
成等差数列,则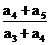 的值为
的值为
A.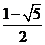 B.
B.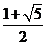 C.
C.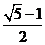 D.
D.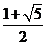 或
或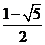
5、在坐标平面上,不等式组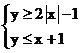 所表示的平面区域的面积为
所表示的平面区域的面积为
A.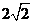 B.
B. 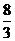 C.
C. D.
D.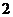
4、若抛物线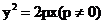 的焦点与椭圆
的焦点与椭圆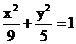 的左焦点重合,则p的值为
的左焦点重合,则p的值为
A.-2 B.2 C.-4 D.4
3、已知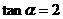 ,则
,则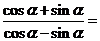
A.-3 B.3 C.2 D.-2
2、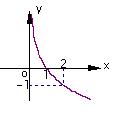 已知函数
已知函数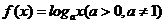 的图象如右图示,函数
的图象如右图示,函数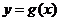 的图象与
的图象与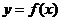 的图象关于直线
的图象关于直线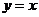 对称,则函数
对称,则函数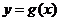 的解析式为
的解析式为
A. B.
B. 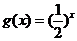
C. 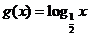 D.
D.
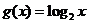
1、若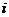 是虚数单位,且复数
是虚数单位,且复数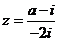 为实数,则实数
为实数,则实数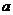 等于
等于
A.1 B.-1 C.0 D.2
25、(14分)已知反应:
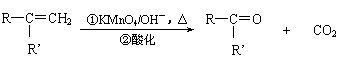
(R、R’可表示烃基或官能团)
A可进行如下反应(方框内物质均为有机物,部分无机产物已略去)。
|
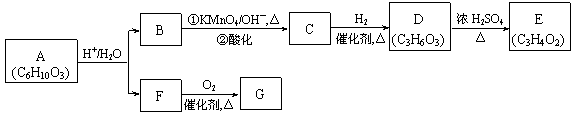

请回答:
(1)F的蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1 mol F与足量金属钠作用产生H2 22.4 L(标准状况),则F的分子式是 ,名称是 。
(2)G与F的相对分子质量之差为4,则G具有的性质是 (填序号)
a.可与银氨溶液反应
b.可与乙酸发生酯化反应
c.可与氢气发生加成反应
d.1 mol G最多可与2 mol 新制Cu(OH)2发生反应
(3)D能与NaHCO3溶液发生反应,又知两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是:
,该反应类型是 反应。
(4)H与B互为同分异构体,且所含官能团与B相同,则H的结构简式可能是:
、 。
(5)A转化为B和F的化学方程式是:
。
昆一中2010届高三年级第三次月考(11月)
23、(14分)我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:
NH3+CO2+H2O
NH4HCO3 NH4HCO3+NaCl NaHCO3↓+NH4Cl ;
 2NaHCO3 Na2CO3+CO2↑+H2O
2NaHCO3 Na2CO3+CO2↑+H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是 (填字母标号)。
a.碳酸氢钠难溶于水 b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某课外活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
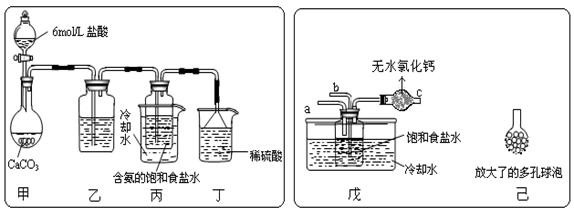
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是 ,该试剂的作用是 ;
(Ⅱ)丁装置中稀硫酸的作用是 ;
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是 (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从 管通入 气体,再从 管中通入 气体。
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是
;
(3)请你再设计出一种实验室制取少量碳酸氢钠的方法:(用文字简要说明)
。
22、(12分)下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料。
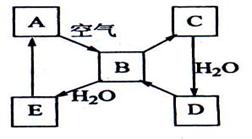
(1)写出A在加热条件下与H2反应的化学方程式
____________________________________________________________
(2)写出E与A的氢化物反应生成A的化学方程式___________________________
(3)写出一个由D生成B的化学方程式____________________________________;
(4)将5mL0.10mol·L-1的E溶液与10mL0.10 mol·L-1的NaOH溶液混合。
①写出反应的离子方程式__________________________________________;
②反应后溶液的pH ______7(填“大于”、“小于”或“等于”),理由是________;
③加热反应后的溶液,其pH________(填“增大”、“不变”或“减小”),理由是________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com