
9.[标准答案]D
[试题分析]A项苯酚与ClCH2COOH反应生成的苯氧乙酸不含有酚羟基,故残留物中若含有苯酚可以与FeCl3显紫色;B项苯酚可以被O2所氧化而呈粉红色,当然也可以被KMnO4所氧化,菠萝酯含有碳碳双键,故也可被KMnO4氧化;苯氧乙酸中含有羧酸可与碱反生中和反应,菠萝酯属于酯可以在碱性条件下发生水解;由于菠萝酯含有碳碳双键也可以使溴水褪色,故不能用来检验残留的烯丙醇。
[高考考点]有机物中官能团的性质检验
[易错提醒]理不清在多重官能团时检验的相互干扰。
[备考提示]学习有机,官能团的性质能重要。
8.(1) ;Ag++Br-=AgBr↓
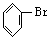 (2)导气,冷凝回流 (3) 、Br2,稀NaOH溶液,蒸馏水。分液漏斗。取少量最后一次洗液,加入稀HNO3,再加入AgNO3溶液,溶液不浑浊说明产品已洗净。(4)该反应是放热反应,反应物和白粉加入的量不适当,会使液溴挥发。挥发的液溴溶于水,生成HBr,与AgNO3反应生成AgBr沉淀,因而无法确定HBr是否是苯与Br2取代反应的产物。Br2+H2O=HBr+HBrO
HBr+AgNO3=AgBr↓+HNO3 (5)a是安全瓶,防止倒吸,b中度剂是苯或四氯化碳。装置Ⅱ的优点①控制反应进行 ②防止倒吸 ③排除液溴的干扰 ④防止有害气体污染环境。
(2)导气,冷凝回流 (3) 、Br2,稀NaOH溶液,蒸馏水。分液漏斗。取少量最后一次洗液,加入稀HNO3,再加入AgNO3溶液,溶液不浑浊说明产品已洗净。(4)该反应是放热反应,反应物和白粉加入的量不适当,会使液溴挥发。挥发的液溴溶于水,生成HBr,与AgNO3反应生成AgBr沉淀,因而无法确定HBr是否是苯与Br2取代反应的产物。Br2+H2O=HBr+HBrO
HBr+AgNO3=AgBr↓+HNO3 (5)a是安全瓶,防止倒吸,b中度剂是苯或四氯化碳。装置Ⅱ的优点①控制反应进行 ②防止倒吸 ③排除液溴的干扰 ④防止有害气体污染环境。
7.(A) D
(B)加少量液溴看颜色是否褪去
(C)消耗②步中加入的溴
(D)C10H8Br4
(E)四氢化萘和水的质量比约是1: 1.3
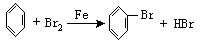
6.
|
官能团 |
鉴别方法及实验现象 |
有关反应的化学方程式 |
反应类别 |
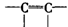 (碳碳双键) |
加溴水
溴水褪色 |
CH3(CH2)5CH=CH(CH2)9CHO +Br2→CH3(CH2)5CH-CHBr(CH2)9CHO |
加成反应 |
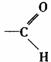 (醛基) |
加银氨溶液
生成银镜 |
CH3(CH2)5CH=CH(CH2)9CHO+ 2[Ag(NH2)2]++2OH- →CH3(CH2)5CH=CH(CH2)9COO- +NH4++2Ag++3NH3+H2O |
氧化反应 |
5.(A)先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却。
(B)将反应器放在55-60℃(或回答60℃)的水浴中加热。
(C)分液漏斗
(D)除去粗产品中残留的酸(或回答除去残留的硝酸,硫酸)
(E)大 苦杏仁
1.C 2.A 3. B 4.将试剂瓶放入水浴中加热,待晶体熔化后,再从瓶口中倒出。
2.(1)防止卤代烷挥发(或答冷疑)(2)Ag+,Na+和
(3)氯;得到的卤化银沉淀是白色的
(4)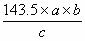 (5)A
(5)A
[针对训练]
1.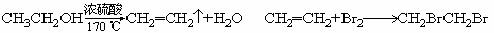 (1)
(1)
(2)b中水面会下降,玻璃管中的水面会上升,甚至溢出。
(3)除去乙烯中带出的酸性气体或答二氧化碳、二氧化硫。
(4)①乙烯发生(或通过液溴)速度过快 ②实验过程中,乙烯和浓硫酸的混合液没有迅速达到170℃(或写“控温不当”也可以)。
2. [解析]根据温度计的使用方法即可解题。制乙烯时测定的是反应混合物的温度,故应用A装置。分离苯和硝基苯的混合物和石油分馏均为分馏实验,测定的是蒸汽的温度,故应用B装置。测定硝酸钾在水中的溶解度是测定溶液的温度,故应选用C装置。
[答案](1)A① B③⑤ C ⑦(2)减少苯的挥发(或答起冷凝器作用)
[考题再现]
1. [解析]本题是一道实验探究题,并对书中的制取乙酸乙酯的实验进行了改进。此类考题是以后考试的方向,应重视。该类考题特点是形变但原理不变,应用反应原理即可解题。
[答案](1)实验中硫酸的主要作用是催化作用和吸水作用;
(2)用过量乙醇的主要目的是使酯化反应向生成乙酸乙酯的方向移动,提高乙酸乙酯的产率。
(3)用饱和Na2CO3溶液洗涤粗酯的目的是除去乙酸。如果用NaOH浓溶液代替Na2CO3,则会使乙酸乙酯发生水解而使实验失败。
(4)用饱和CaCl2溶液洗涤粗酯的目的是除去乙醇。
(5)让产生的乙酸乙酯及时蒸馏出来。
(6)粗酯里还有的杂质是水。
(7)让实验中产生的SO2等有毒气体排出室外,也有利于乙酸乙酯等液体流入锥形瓶,并使锥形瓶中的压强内外一致。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com