
1.下列词语中,各对加点字的读音都不相同的一项是
A.畸形/绮丽 后缀/补裰 玩弄/弄堂 咀嚼/咬文嚼字
B.烘焙/蓓蕾 坯子/胚胎 裨益/裨将 契机/提纲挈领
C.稽查/稽首 巷道/小巷 果脯/胸脯 笨拙/相形见绌
D.鞭笞/褫夺 麾下/春晖 不惮/澹然 攻讦/宵衣旰食
31、(10分)有氯化亚铁、氯化铜混合溶液400 mL,经测定其中Cl-浓度是a mol / L。投入过量的锌粉b g,充分反应后过滤,所得固体残渣洗涤干燥后,质量为c g。
(1) 求原混合溶液中Fe2+是____ _ ____ mol / L,Cu2+是_____ ___ _ mol / L。(以a、b、c表示)
(2) b的值应大于_______a g。
(3) c的数值越大,说明混合液中氯化铜含量___________(填“越大”或“越小”);
c的最大值(以a、b表示)应是__________g。
2008~2009学年度上学期期中考试
30、(7分)有未知浓度的盐酸25 mL,能跟20 mL某浓度的NaOH溶液完全反应。若先用0.1 g CaCO3与25 mL这种酸作用,剩余的酸需用上述NaOH溶液4 mL才能中和。求盐酸和NaOH溶液中溶质的物质的量浓度。(要求有计算过程)
29、(7分)某化学反应的反应物和产物如下:
KMnO4 + KI + H2SO4 → MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是 。
(2)如果该反应方程式中I2和KIO3的系数都是5
①KMnO4的系数是 。
②在下面的化学式上标出电子转移的方向和数目(单线桥)
KMnO4 + KI + H2SO4 →
(3)如果没有对该方程式中的某些系数作限定,可能的配平系数有许多组。原因是 。
28、(6分)4mL O2和3mL NxHy(y>x)混合气体在120℃,1.01×105Pa下点燃完全反应后,恢复到原温度和压强时,测得反应后N2、O2、H2O(气)混合气体密度减小3/10。
(1)NxHy的分子式为: 。
(2)反应的化学方程式为 。
27、(6分)有一包白色粉未状混和物,可能含有CaCO3、K2SO4、CaCl2、NaNO3和Na2CO3中的某几种,实验过程及现象如下图:
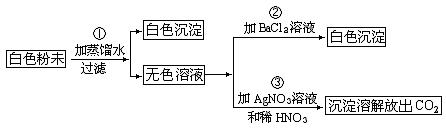 判断:混合物中一定含有
,肯定不含有
,
判断:混合物中一定含有
,肯定不含有
,
可能含有 。
26、(4分)将下列各分离物质方法的编号,填在各小题末的括号内:
A. 过滤法; B降温结晶法; C. 分液法; D. 萃取分液法; E. 蒸馏法; F. 层析法; G. 升华法
(1)除去食盐水中的泥沙( ) (2)除去植物油中的水( )
(3)将溶液中的硝酸钾与氯化钠分离( )(4)将天然水制为纯净水( )
25、已知硫酸铅难溶于水,也难溶于硝酸,但可溶于醋酸铵(NH4Ac)溶液形成无色溶液,其化学方程式为:PbSO4+2NH4Ac=Pb(Ac)2+(NH)2SO4。当在Pb(Ac)2溶液中通入H2S时,有黑色PbS生成。表示这个反应的有关离子反应方程式正确的是
A Pb(Ac)2+H2S=PbS↓+2HAc
B Pb2++H2S=PbS↓+2H+
C Pb2++2Ac-+H2S=PbS↓+2HAc
D Pb2++2Ac-+2H++S2-=PbS↓+2HAc
第Ⅱ卷(共40分)
24、在标准状况下,烧瓶内充满HCl气体,将此烧瓶倒扣在盛水的水槽内,当液面上升到烧瓶容积的 时,此时烧瓶内溶液的物质的量浓度为
时,此时烧瓶内溶液的物质的量浓度为
A 0.74 mol / L B 0.045 mol / L C 0.037 mol / L D 0.025 mol / L
23、已知:①2BrO3-+Cl2=Br2+2ClO3- ②5Cl2+I2+6H2O=2HIO3+10HCl
③ClO-3+5Cl-+6H+=3Cl2+3H2O 下列粒子氧化性强弱顺序正确的是
A ClO3->BrO3->IO3->Cl2 B IO3-<ClO3-<BrO3-<Cl2
C IO3-<BrO3-<Cl2<ClO3- D BrO3->ClO3->Cl2>IO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com