
4. 如图所示,电梯内的地板上竖直放置一根轻质弹簧,弹簧上方有一质量
如图所示,电梯内的地板上竖直放置一根轻质弹簧,弹簧上方有一质量
为m的物体。当电梯静止时弹簧被压缩了x1,当电梯运动时弹簧被压
缩了x2,且有x2> x1,试判断电梯运动的可能情况是 ( )
A.匀加速上升
B.匀加速下降
C.匀减速上升
D.匀减速下降
3.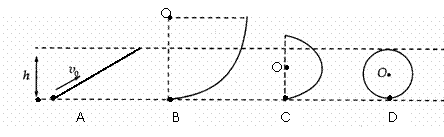 如图所示,小球以初速度v0竖直上抛,它能到达的最大高度为h,下图中A是光滑斜面、B是轨道半径大于h的光滑圆轨道、C是轨道半径小于h的光滑圆轨道、D是轨道直径等于h光滑圆轨道。小球在底端时的初速度都为v0,则小球在上述四种情况中能到达高度h的有 ( )
如图所示,小球以初速度v0竖直上抛,它能到达的最大高度为h,下图中A是光滑斜面、B是轨道半径大于h的光滑圆轨道、C是轨道半径小于h的光滑圆轨道、D是轨道直径等于h光滑圆轨道。小球在底端时的初速度都为v0,则小球在上述四种情况中能到达高度h的有 ( )
2.中央电视台《今日说法》栏目最近报道了一起发生在湖南长沙某
区湘府路上的离奇交通事故。家住公路转弯处的张先生和李先
生家在三个月内连续遭遇了七次大卡车侧翻在自家门口的场面,
第八次有辆卡车冲撞进李先生家,造成三死一伤和房屋严重损
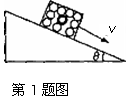
毁的血腥惨案。经公安部门和交通部门协力调查,画出的现场
示意图如图所示。下列分析中,你认为正确的是 ( )
A.由图可知汽车在转弯时发生侧翻是因为车作离心运动
B.由图可知汽车在转弯时发生侧翻是因为车作向心运动
C.为了减少事故的发生,公路转弯处应该设计为内侧高外侧低
D.为了减少事故的发生,公路转弯处应该设计为外侧高内侧低
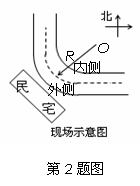
1. 如图所示,一箱苹果沿着倾角为θ的斜面,以速度v匀速下滑。
如图所示,一箱苹果沿着倾角为θ的斜面,以速度v匀速下滑。
在箱子的中央有一只质量为m的苹果,它受到周围苹果对它
作用力的方向 ( )
A.沿斜面向上 B.沿斜面向下
 C.竖直向上 D.垂直斜面向上
C.竖直向上 D.垂直斜面向上
2.0mol·L-1NaOH溶液中,充分反应。NaOH
溶液的体积V≥
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将 (填“偏高”或“偏低”)
[探究二] 实验方案:铝镁合金 测定生成气体的体积
测定生成气体的体积
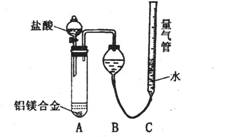
实验装置如右图,问题讨论:
(3)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置。你的意见是: (填“需要”或“不需要”)。
(4)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
①
②
29.(13分)铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
[探究一] 实验方案:铝镁合金  测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是
 实验步骤:
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL
28.(11分)有一澄清透明的溶液,可能有NH4+、Fe3+、H+、Mg2+、Al3+、I-、CO32-等离子,现分别取溶液进行下列实验:
(1)加入浓溴水,溶液变为褐色;
(2)加入淀粉,未见蓝色;
(3)在逐滴加入1mol·L-1NaOH溶液的过程中,
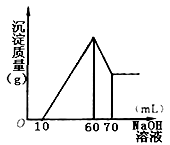 未闻到刺激性气体,随NaOH溶液的滴入,
未闻到刺激性气体,随NaOH溶液的滴入,
产生沉淀的量如图所示,试确定:
①溶液中一定存在的离子有 ;
②写出加入NaOH溶液过程中发生的反应的离子方程式
③其中阳离子物质的量分别为
27.(11分)某化学兴趣小组为探索工业废料的再利用,在实验室中用含有铝、铁、铜的合金制取氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体。其实验方案如下:
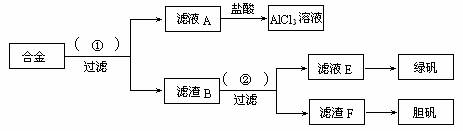
(1)所加试剂①、②分别是 。
(2)从滤液E中得到绿矾晶体的实验操作是:在隔绝空气的条件下, ;从滤渣F制取胆矾的第一步操作最好采用 。
(3)上述实验方案中,有一步设计明显不合理,请你予以指出,并说明理由 。
你认为正确的设计方案是
。
26.(15分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W是金属元素,X是地壳中含量最多的金属元素,且w、x的最高价氧化物的水化物相互反应生成盐和水;Y、Z是非金属元素,Y与W可形成离子化合物W2Y;G在Y的前一周期,其原子最外层比Y原子最外层少一个电子。
(1)X的原子结构示意图为 。
(2)W、X的最高价氧化物的水化物相互反应的离子方程式为 。
(3)工业上制取X单质的化学方程式为 。
(4)G的气态氢化物与Y的最高价氧化物的水化物恰好反应生成的正盐的化学方程式为 。在催化剂作用下,汽车尾气中G的氧化物GO与一氧化碳两种气体能相互反应转化为无污染、能参与大气循环的两种气体,写出有关反应的化学方程式 ;若有33.6 L(已换算成标准状况)一氧化碳参加反应,转移的电子数为 。
(5)298K时,Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到Z的最高价氧化物的水化物的稀溶液,并放出a kJ的热量。该反应的热化学方程式为
(6)说出Z单质的一种用途______ ___
25. 设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,
设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,
不能达到预期目的的是 ( )
A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,
比较生成气体的快慢 B.分别向等量的白色粉末中加等体积适量的水,比较固体
溶解量的多少 C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成 D.分别将等量的白色粉末用右图装置进行实验,比较澄清石灰水是否变混浊
第Ⅱ卷(非选择题,共50分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com