
9.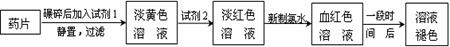 铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
⑴ 试剂1是 ,试剂2是 ,加入新制氯水后溶液中发生的离子反应方程式是
,
⑵ 加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为
写出+2价Fe在空气中转化为+3价Fe的化学方程式
;
⑶ 该同学猜想血红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗? 。
若你认为合理,请说明理由(若你认为不合理,该空不要作答)
若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不要作答) 。
8.设计一个用BaCl2溶液及试管鉴别Na2SO3溶液和稀H2SO4的实验,简要写出鉴别过程和实验结论。
7.如何用最简便的实验方法,只用酚酞试液就能鉴别出浓度均为0.1mol·L-1的食盐,盐酸和NaOH溶液,简述其实验方法和步骤。
6.蛇纹石由MgO、A12O3、Si02、Fe203组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是
A.沉淀X的成分是Si02
B.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3,
C.在溶液Y中加入过量的NaOH溶液,过滤,得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
D.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
5.下列有关实验所选用的试剂能达到目的的是 ( )
A.证明NaHCO3溶液中混有苏打用澄清石灰水 B.证明SO2中混有CO2用澄清石灰水 C.证明AgNO3溶液中混有Al(NO3)3用氨水 D.除掉C2H6中的C2H4用酸性KMnO4溶液
4.下列各组物质,不能用一种试剂区别开的是 ( )
A.二氧化锰、氧化铜、铁粉、炭粉 B.硫酸铵、氯化铵、氯化钠、硫酸钠
C.乙醇、四氯化碳、苯、已烯 D.苯、水、甲苯、二甲苯
3.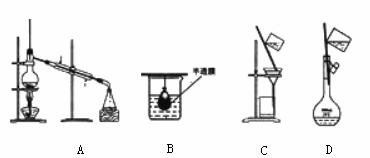 以下实验装置一般不用于分离物质的是
( )
以下实验装置一般不用于分离物质的是
( )
2.下列实验能达到预期目的的是 ( )
.... ①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
.... ②将Cl2的制备和性质实验联合进行以减少实验中的空气污染
.... ③用食醋和澄清石灰水验证蛋壳中含有碳酸盐
.... ④用硝酸钡溶液鉴别硫酸根离子与亚硫酸根离子
.... ⑤用溴水检验汽油中是否含有不饱和脂肪烃
A.①②③ B.①③④ C.②③⑤ D. ②④⑤
1.下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是( )
A.Ba(OH) 3 KSCN NaCl Mg(NO3) (FeCl3溶液)
B.NaNO3 NaHCO3 (NH4) 2SO3 Na2SiO3 (H2SO4溶液)
C.NH4Br K2CO3 NaI CaCl2 (AgNO3溶液)
D.(NH4) 3PO4 NaBr CuSO4 AlCl3 (KOH溶液)
例1 如何鉴别下列几组物质 (1)(NH4)2SO4、NaCl、CH3COONa三种溶液;
(2)Al2(SO4)3、MgSO4、(NH4)2SO4、CuSO4四种溶液;
(3) Na2SiO3、Na2CO3、Na2S2O3、NaCl、NaAlO2五种溶液
(4)NaOH、NaCl、NH4NO3三种固体
例2 欲检验(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵晶体)中含有NH4+、Fe2+、SO42-和H2O,设计如下实验步骤:①取少量晶体放在试管内,用酒精灯加热,试管口有液体,说明晶体中含有H2O;②将加热后剩余的晶体溶解于水,加入硝酸酸化的BaCl2溶液,有白色沉淀生成,说明晶体中含有SO42-;③滤去白色沉淀,向滤液中加入过量浓NaOH溶液,加热,有能使红色石蕊试纸变蓝的气体产生,说明晶体中含有NH4+;④向步骤③的剩余液体中加入KSCN溶液,无明显变化,再加入少量氯水,溶液变成血红色,说明晶体中含有Fe2+。其中不能达到实验目的的是 ( )
A.①③④ B.①④ C.③④ D.只有④
例3 我们知道铜放于冷的浓硫酸中无明显现象,甲同学认为在室温下Cu与浓H2SO4不反应,而乙同学认为铜也可能发生了钝化,表面生成了红色的Cu2O,经查资料知Cu2O在稀硫酸中发生反应:
Cu2O+2H+=Cu2++Cu+H2O。请你设计一实验以证明乙的说法是否正确?
_________________________________________________________________
例4某教科书对“铝热反应”实验的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”,“纸漏斗的下部被烧穿,有熔融物落入沙中”。已知:Al、Fe的熔点、沸点数据如下:
|
物质 |
Al |
Fe |
|
熔点(℃) |
660 |
1535 |
|
沸点(℃) |
2467 |
2750 |
(1)某同学猜测,铝热反应所得到的熔融物是铁铝合金。理由是:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理? (填“合理”或“不合理”)。
(2)根据已有知识找出一种验证产物中有Fe的最简单方法:
(3)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝。请填写下列表格:
|
所用试剂 |
|
|
实验操作及现象 |
|
|
有关反应的化学方程式 |
|
例5已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
(1)甲同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:____________ (填粒子的化学式,下同);
乙同学认为这是发生化学反应所致,则使溶液呈黄色的微粒是_________。
(2)你认为哪位同学的观点是正确的?______________(填“甲”或“乙”),为了验证你的判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂:
A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液 E.硝酸银溶液 F.碘化钾淀粉溶液
|
实验方案 |
所选用试剂(填代号) |
实验现象 |
|
方案一 |
|
|
|
方案二 |
|
|
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,则首先被氧化的离子是______ :若选用淀粉碘化钾溶液来判断哪位同学的推断是正确的,你认为是否可行?______ ,
理由是:__________________________________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com