
4、等价转化法:通过“化复杂为简单、化陌生为熟悉”将问题等价转化成便于解决的问题,从而得到正确的结果。
例11、不等式 的解集为
的解集为 ,则
,则 _______,
_______,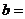 ________。
________。
解:设 ,则原不等式可转化为:
,则原不等式可转化为: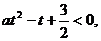 ∴a > 0,且2与
∴a > 0,且2与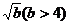 是方程
是方程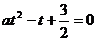 的两根,由此可得:
的两根,由此可得: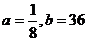 。
。
例12、不论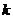 为何实数,直线
为何实数,直线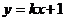 与圆
与圆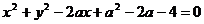 恒有交点,则实数
恒有交点,则实数 的取值范围是 。
的取值范围是 。
解:题设条件等价于点(0,1)在圆内或圆上,或等价于点(0,1)到圆 ,∴
,∴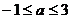 。
。
3、数形结合法:对于一些含有几何背景的填空题,若能根据题目条件的特点,作出符合题意的图形,做到数中思形,以形助数,并通过对图形的直观分析、判断,则往往可以简捷地得出正确的结果。
例8、已知向量 =
=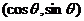 ,向量
,向量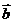 =
= ,则|2
,则|2 -
-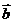 |的最大值是
|的最大值是
解:因 ,故向量2
,故向量2 和
和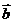 所对应的点A、B都在以原点为圆心,2为半径的圆上,从而|2
所对应的点A、B都在以原点为圆心,2为半径的圆上,从而|2 -
-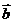 |的几何意义即表示弦AB的长,故|2
|的几何意义即表示弦AB的长,故|2 -
-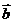 |的最大值为4。
|的最大值为4。
例9、如果不等式 的解集为A,且
的解集为A,且 ,那么实数
,那么实数 的取值范围是
。
的取值范围是
。
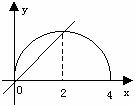 解:根据不等式解集的几何意义,作函数
解:根据不等式解集的几何意义,作函数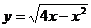 和
和
函数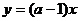 的图象(如图),从图上容易得出实数
的图象(如图),从图上容易得出实数 的取
的取
值范围是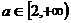 。
。
例10、设函数 f(x)=x3+ax2+2bx+c.若当 x∈(0,1)时,f(x)取得极大值;x∈(1,2)时,f(x)取得极小值,则 的取值范围是 .
 解:f´(x)= x2+ax+2b,令f´(x)=0,由条件知,上述方程应满足:一根在(0,1)之间,另一根在(1,2)之间,∴ ,得 ,在aob坐标系中,作出上述区域如图所示,而 的几何意义是过两点P(a,b)与A(1,2)的直线斜率,而P(a,b)在区域内,由图易知kPA∈(,1).
解:f´(x)= x2+ax+2b,令f´(x)=0,由条件知,上述方程应满足:一根在(0,1)之间,另一根在(1,2)之间,∴ ,得 ,在aob坐标系中,作出上述区域如图所示,而 的几何意义是过两点P(a,b)与A(1,2)的直线斜率,而P(a,b)在区域内,由图易知kPA∈(,1).
2、特殊化法:当填空题已知条件中含有某些不确定的量,但填空题的结论唯一或题设条件中提供的信息暗示答案是一个定值时,可以将题中变化的不定量选取一些符合条件的恰当特殊值(或特殊函数,或特殊角,特殊数列,图形特殊位置,特殊点,特殊方程,特殊模型等)进行处理,从而得出探求的结论。这样可大大地简化推理、论证的过程。
例4、在 ABC中,角A、B、C所对的边分别为a、b、c,如果a、b、c成等差数列,则
ABC中,角A、B、C所对的边分别为a、b、c,如果a、b、c成等差数列,则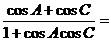
解法一:取特殊值a=3, b=4, c=5 ,则cosA= cosC=0,
cosC=0, 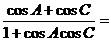
 。
。
解法二:取特殊角A=B=C=600 cosA=cosC=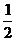 ,
,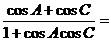
 。
。
例5、如果函数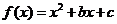 对任意实数
对任意实数 都有
都有 ,那么
,那么 的大小关系是 。
的大小关系是 。
解:由于 ,故知
,故知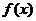 的对称轴是
的对称轴是 。可取特殊函数
。可取特殊函数 ,即可求得
,即可求得 。∴
。∴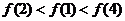 。
。
例6、已知SA,SB,SC两两所成角均为60°,则平面SAB与平面SAC所成的二面角为 。
解:取SA=SB=SC,则在正四面体S-ABC中,易得平面SAB与平面SAC所成的二面角为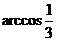 。
。
 例7、已知
例7、已知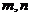 是直线,
是直线,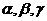 是平面,给出下列命题:①若
是平面,给出下列命题:①若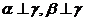 ,则
,则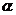 ∥
∥ ;②若
;②若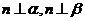 ,则
,则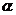 ∥
∥ ;③若
;③若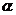 内不共线的三点到
内不共线的三点到 的距离都相等,则
的距离都相等,则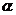 ∥
∥ ;④若
;④若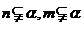 ,且
,且 ∥
∥ ,
, ∥
∥ ,则
,则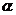 ∥
∥ ;⑤若
;⑤若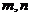 为异面直线,
为异面直线,
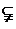
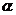 ,
, ∥
∥ ,
,
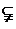
 ,
, ∥
∥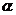 ,则
,则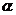 ∥
∥ 。则其中正确的命题是 。(把你认为正确的命题序号都填上)
。则其中正确的命题是 。(把你认为正确的命题序号都填上)
解:依题意可取特殊模型正方体AC1(如图),在正方体AC1中逐一判断各命题,易得正确的命题是②⑤。
1、直接法:直接从题设条件出发,利用定义、性质、定理、公式等,经过变形、推理、计算、判断得到结论的,称为直接法。它是解填空题的最基本、最常用的方法。使用直接法解填空题,要善于通过现象看本质,自觉地、有意识地采取灵活、简捷的解法。
例1、乒乓球队的10名队员中有3名主力队员,派5名参加比赛。3名主力队员要安排在第一、三、五位置,其余7名队员选2名安排在第二、四位置,那么不同的出场安排共有_________种(用数字作答)。
解:三名主力队员的排法有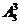 种,其余7名队员选2名安排在第二、四位置上有
种,其余7名队员选2名安排在第二、四位置上有 种排法,故共有排法数
种排法,故共有排法数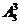
 =252种。
=252种。
例2、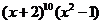 的展开式中
的展开式中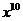 的系数为
。
的系数为
。
解:
得展开式中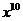 的系数为
的系数为
 =179。
=179。
例3、已知函数 在区间
在区间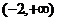 上为增函数,则实数
上为增函数,则实数 的取值范围是 。
的取值范围是 。
解: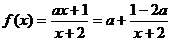 ,由复合函数的增减性可知,
,由复合函数的增减性可知, 在
在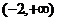 上为增函数,∴
上为增函数,∴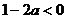 ,∴
,∴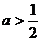 。
。
20.(5分)研究表明,在一定温度和压强条件下,2 mol H2(g) 和1 mol O2(g) 完全化合生成2 mol H2O(g) 所放出的热量;①与在相同条件下2 mol H2O(g) 完全分解为2 mol H2(g) 和1 mol O2(g) 所吸收的热量在数值上相等; ②是相同条件下1 mol H2(g) 和0.5 mol O2(g) 完全化合生成1 mol H2O(g)所放出热量的2倍;③比在相同条件下2 mol H2(g) 和1 mol O2(g) 完全化合生成2 mol H2O(l) 所放出的热量少。
由此,你可得出哪些结论?
19.某学校化学兴趣小组同学在两支小试管中分别加入浓度为4mol/L稀盐酸3mL,将分别装有0.3gNaHCO3和0.3gNa2CO3粉末的小气球分别套在两支试管口。将气球内的NaHCO3和Na2CO3同时倒人试管中,观察到的现象及分析如下:
(1)比较两支试管中的现象: 。
(2)若两气球内的压强相同.两试管大小相同,则大小气球体积之比约为 (填最简整数比)
(3)甲同学用手触摸试管,发现盛NaHCO3粉末的试管变冷,而盛Na2CO3的试管温度升高。由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应。甲同学写出了下列热化学方程式(其中“aq”代表水合或无限稀释的含义):
HCO3-(aq)+H+(aq)=H2O(1)+CO2(g);△H>O;
CO32-(aq)+2H+(aq)=H2O(1)+CO2(g);△H<O;
甲分析结论的方法是否科学? 。(填“是”或“否”)
(4)为研究反应是吸热还是放热,乙同学继续进行下列实验。(每个实验平行做三次,取平均值)
|
序 号 |
试剂l |
试剂2 |
混合前温度 |
混合后最高或最低温度 |
|
1 |
35mL水 |
2.5gNaHCO3固体 |
20℃ |
18.5℃ |
|
2 |
35mL水 |
3.2gNa2CO3固体 |
20℃ |
24.3℃ |
|
3 |
35mL稀盐酸 |
含2.5g NaHCO3 的饱和溶液32.5ml |
20℃ |
19℃ |
|
4 |
35mL稀盐酸 |
含3.2g Na2CO3的饱和溶23.1mL+10mL水 |
20℃ |
24.2℃ |
|
5 |
35mL稀盐酸 |
2.5g NaHCO3固体 |
20℃ |
16.2℃ |
|
6 |
35mL稀盐酸 |
3.2gNa2CO3固体 |
20℃ |
25.1℃ |
请你帮助填写相关内容:
①该研究报告的题目是《 》
②通过上述实验可得出五条结论:
a.NaHCO3的溶解是 (“吸热”或“放热”)过程;
b.Na2CO3的溶解是 (“吸热”或“放热”)过程;
c.NaHCO3的饱和溶液和盐酸的反应是 (”吸热”或“放热”)反应;
d.Na2CO3的饱和溶液和盐酸的反应是 (“吸热”或“放热”)反应;
e.NaHCO3固体与稀盐酸反应的反应热是 (填a→d的字母)的热效应之和。
18.用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
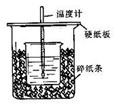
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
17.在一个小烧杯里,加入20gBa(OH)2.H2O粉末,将小烧杯放在事先已滴有3~4滴水的玻璃片上。然后加入10gNH4Cl晶体,并立即用玻璃棒搅拌。
(1)试验中玻璃棒的作用是 。
(2)写出有关反应的方程式 ,该反应属于 反应。
(3)实验中观察到的现象有 , 和反应混合物成糊状。反应混合物呈糊状的原因是 。
(4)通过 现象,说明该反应为 热反应,这是由于反应物的总能量
生成物的总能量。
16.(6分)热值指在一定条件下每克物质完全燃烧所放出的热量,(燃烧产物在该条件下是一种较为稳定的状态),下表是几种物质在常温常压下的热值数据。
|
物质 |
H2 |
CO |
CH4 |
|
热值/kJ·g–1 |
143 |
10 |
56 |
(1)根据以上热值数据,最理想的燃料是 。
(2)根据以上热值数据,写出在该状态下氢气燃烧的热化学方程式 。
(3)若管道煤气(含体积比为1:1的H2和CO)价格为1.00元/m3,天然气的价格为2.50元/m3,使用哪种气体在经济上更为合算? 理由是 。(无需写出计算过程)
15.煅烧石灰石制生石灰,设用焦炭为燃料,热化学方程式为:
CaCO3(s) CaO(s)+CO2(g);△H= +159KJ/mol
CaO(s)+CO2(g);△H= +159KJ/mol
C(s)+O2(g) CO2(g);△H= -393.5KJ/mol
CO2(g);△H= -393.5KJ/mol
设 热能的利用率为70%,计算煅烧1t石灰石需含碳90%的焦炭多少吨?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com