
¿˝6.(09ƒÍ∏£Ω®æÌ) ƒÐ µœ÷œ¬¡–ŒÔ÷ º‰÷±Ω”◊™ªØµƒ‘™Àÿ «
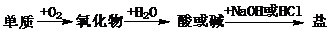
A. πË°°°°°°°°°°°°°° B. ¡Ú°°°°°°°°°°°°°° C. Õ≠°°°°°°°°°°°° °°°°°°D. Ã˙
[Ω‚Œˆ]S”ÎO2…˙≥…SO2£¨‘Ÿ”ÎH2O…˙≥…H2SO3£¨ø…“‘”ÎNaOH…˙≥…Na2SO3£¨BœÓ’˝»∑°£AœÓ£¨SiO2≤ª”ÎÀÆ∑¥”¶£¨¥Ì£ªCœÓ÷–CuO£¨DœÓ÷–Fe3O4æ˘≤ª”ÎH2O∑¥”¶£¨π ¥Ì°£
[¥∞∏]B
¿˝7.(09ƒÍπ„∂´æÌ) ≥£Œ¬œ¬£¨Õ˘H2O2»Ð“∫÷–µŒº”…Ÿ¡øFeSO4»Ð“∫£¨ø…∑¢…˙»Áœ¬¡Ω∏ˆ∑¥”¶£∫2Fe2++H2O2+2H+£Ω2Fe3++2H2O°°°° 2Fe3++H2O2£Ω2Fe2++O2°¸+2H+œ¬¡–Àµ∑®’˝»∑µƒ «
A£ÆH2O2µƒ—ıªØ–‘±»Fe3+«ø£¨∆‰ªπ‘≠–‘±»Fe2+»ı
B£Æ‘⁄H2O2∑÷Ω‚π˝≥Ã÷–£¨»Ð“∫µƒpH÷Ω•œ¬Ωµ
C£Æ‘⁄H2O2∑÷Ω‚π˝≥Ã÷–£¨ Fe2+∫ÕFe3+µƒ◊Сø±£≥÷≤ª±‰
D£ÆH2O2…˙≤˙π˝≥Ó™—œ∏Ò±Ð√‚ªÏ»ÎFe2+
[Ω‚Œˆ]Ω·∫œA°¢B¡Ω∏ˆ∑Ω≥à Ω∏˘æð —ıªØ–‘°¢ªπ‘≠–‘«ø»ı±»Ωœπʬ…£∫µ√ H2O2µƒ—ıªØ–‘>Fe3+µƒ—ıªØ–‘£¨ H2O2µƒªπ‘≠–‘>Fe2+µƒªπ‘≠–‘£¨A¥Ì£ª2H2O2£Ω2H2O+O2°¸£¨∑÷Ω‚π˝≥Ã÷–£¨Fe2+◊˜¥þªØº¡£¨»Ð“∫pH÷µ≤ª±‰£¨B¥Ì£¨H2O2∑÷Ω‚Fe3+ªÚFe2+◊˜¥þªØº¡£¨À˘“‘◊Сø≤ª±‰°£“ÚŒ™Fe2+ø…µº÷¬H2O2∑÷Ω‚£¨À˘“‘H2O2…˙≤˙π˝≥Ó™±Ð√‚ªÏ»ÎFe2+£¨D’˝»∑°£
[¥∞∏]CD
¿˝3.(2009ΩÏ¡˙—““ª÷–µ⁄“ª—ß∂Œøº ‘)œ¬¡– µ—Èœ÷œÛ£¨”Ζ¬÷∆¬»ÀÆ÷–µƒƒ≥–©≥…∑÷(¿®∫≈ƒ⁄ŒÔ÷ )√ª”–πÿœµµƒ°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
A£ÆΩ´NaHCO3πÃú”»Î–¬÷∆¬»ÀÆ£¨”–ŒÞ…´∆¯≈ð(H+)
B£Æ π∫Ï…´≤ºÃıÕ …´(HCl)
C£ÆœÚFeCl2»Ð“∫÷–µŒº”¬»ÀÆ£¨‘ŸµŒº”KSCN»Ð“∫£¨∑¢œ÷≥ —™∫Ï…´(Cl2)
D£ÆµŒº”AgNO3»Ð“∫…˙≥…∞◊…´≥¡µÌ(Cl-)
[Ω‚Œˆ]¬»ÀÆ÷–¥Ê‘⁄H+£¨”ÎNaHCO3∑¥”¶≤˙…˙CO2£¨”ÎH+œýπÿ£ª¬»ÀÆ π∫Ï…´≤ºÃıÕ …´ «“ÚŒ™¬»ÀÆ÷–¥Ê‘⁄HClO£¨∂¯≤ª «“ÚŒ™¬»ÀÆ÷–¥Ê‘⁄HCl£ª¬»ÀÆ÷–¥Ê‘⁄Cl2ƒÐ—ıªØFe2+°˙Fe3+£¨π µŒº”KSCN»Ð“∫£¨»Ð“∫≥ —™∫Ï…´£ª¬»ÀÆ÷–¥Ê‘⁄Cl-ƒÐ”ÎAgNO3»Ð“∫…˙≥…∞◊…´≥¡µÌ°£
[¥∞∏]B
¿˝4.œ¬¡–”–πÿ¬»µƒ– ˆ÷–’˝»∑µƒ «°°
A£Æ“∫¬»∫Õ¬»ÀÆ «Õ¨“ªŒÔ÷ °°
°° B£Æ∫Ï¡◊‘⁄¬»∆¯÷–»º…’≤˙…˙∞◊…´—ÃŒÌ
C£Æ¬»∆¯”ÎÀƵƒ∑¥”¶÷–¬» «—ıªØº¡£¨ÀÆ «ªπ‘≠º¡
D£Æ”√¬»÷∆∆Ø∞◊∑€ «Œ™¡Àµ√µΩ“◊÷¸¥Êµƒ∆Ø∞◊º¡
[Ω‚Œˆ]“∫¬»°¢¬»ÀÆ∂º «“∫㨵´«∞’þ «¥ø¬»£¨∫Û’þ «¬»”ÎÀƵƒªÏ∫œŒÔ£¨ ±º‰—”≥§¬»ÀÆ÷–ªπ÷Ω•…˙≥…—ŒÀ·∫Õ¥Œ¬»À·£¨¬»∑÷◊”Ω•…Ÿ£¨¬»¿Î◊”Ω•∂ý°£»Áπ˚‘Ÿ”–π‚’’£¨ “Ú∑÷Ω‚“≤‘⁄Ω•…Ÿ£¨≥ˆœ÷—ı∆¯∫Õ∏¸∂ý—ŒÀ·°£¬»”ÎÀƵƒ∑¥”¶ «¬»∑÷◊”÷–¬»‘≠◊”º‰∑¢…˙µƒ◊‘…Ì—ıªØªπ‘≠£¨º¥∆ÁªØ∑¥”¶, ÀÆÀ‰»ª «∑¥”¶ŒÔ£¨»¥Œ¥≤Œº”—ıªØªπ‘≠°£A°¢C≤ª’˝»∑°£
—à «∑÷…¢‘⁄∆¯ÃÂ÷–µƒπÃÖ°ø≈¡££¨ŒÌ «∑÷…¢‘⁄∆¯Ã¿Եƒ“∫Ö°÷ȵŒ°£¡◊‘⁄¬»∆¯¿Ô»º…’µƒ≤˙ŒÔ»˝¬»ªØ¡◊ «ŒÞ…´“∫ã¨ø…∑¢ŒÌ£ªŒÂ¬»ªØ¡◊ ««≥ª∆…´πÃ㨃ЖŒ≥…—ð£∆Ø∞◊∑€∫Õ¬»∂ºø…“‘◊˜Œ™∆Ø∞◊º¡°¢œ˚∂溡£¨«“¬»∏¸”––ß°£µ´¬»∆¯ƒ—÷¸¥Ê£¨”÷”–æÁ∂棨“ª∞„“Ω”√°¢º“”√µƒ∆Ø∞◊º¡∫Õ
œ˚∂溡 π¬»∆¯ «≤ª∫œ“Àµƒ£¨À˘“‘÷∆≥…∆Ø∞◊∑€±„”⁄÷¸¥Ê∫Õ π”√°£∆Ø∞◊∑€±£¥Êµ√µ±£¨»Á√б’£¨“‘∑¿÷πŒ¸ÀÆ∫Õ ∂¯±‰÷ £¨ø…“‘¥Ê∑≈Ωœ≥§ ±º‰°£B°¢D’˝»∑°£
[¥∞∏]B°¢D°£
¿˝5. ∂ý‘≠◊”∑÷◊”«Ë(CN)2°¢¡Ú«Ë(SCN)2∫Õ(OCN)2µƒ–‘÷ ”ά±Àÿµ•÷ œýÀ∆£¨π ≥∆À¸√«Œ™ƒ‚¬±Àÿ°£À¸√«ø…“‘…˙≥…À·∫Õ—Œ(º˚œ¬±Ì£¨±Ì÷–X¥˙±ÌF°¢Cl°¢BrªÚI)°£
|
°° |
¬±Àÿ |
«Ë |
¡Ú«Ë |
¢Ÿ |
|
°∞µ•÷ °± |
X2 |
(CN)2 |
(SCN)2 |
(OCN)2 |
|
À· |
HX |
HCN |
¢⁄ |
HOCN |
|
—Œ |
KX |
KCN |
KSCN |
¢€ |
(1)‘⁄±Ì÷–¢Ÿ¢⁄¢€ø’∏Ò¥¶”¶∑÷±ÃÓ–¥_______°¢_______°¢_______°£
(2)ÕÍ≥…œ¬¡–∑¥”¶µƒªØ—ß∑Ω≥Ã ΩªÚ¿Î◊”∑Ω≥Ã Ω°£
¢Ÿ(CN)2∫ÕKOH»Ð“∫∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫______________°£
¢⁄“—÷™“ı¿Î◊”µƒªπ‘≠–‘«ø»ıŒ™£∫Cl£≠£ºBr£≠£ºCN£≠£ºSCN£≠£ºI£≠°£ ‘–¥≥ˆ‘⁄NaBr∫ÕKSCNµƒªÏ∫œ»Ð“∫÷–º”»Î(CN)2∑¥”¶µƒ¿Î◊”∑Ω≥Ã Ω£∫____________________________________°£
[Ω‚Œˆ]¥ÀÂ÷˜“™øº≤È°∞‘À”√“——ß÷™ ∂Ω¯––¿ýÕ∆ÀºŒ¨µƒƒÐ¡¶°±°£Ω‚ ±ø…”√ Ï÷™µƒCl2°¢HCl°¢KClµ»ŒÔ÷ ◊˜≤Œ’’ŒÔ°£”…ªπ‘≠–‘Br-<CN-<SCN-£¨ø…Õ∆÷™—ıªØ–‘Br2>(CN)2>(SCN)2£¨“Ú∂¯ø…≈–∂œ(CN)2÷ªƒÐ”ÎKSCN∑¥”¶£¨≤ªƒÐ”ÎNaBr∑¥”¶£¨“ýº¥”…ŒÔ÷ µƒ—ıªØ–‘∫Õªπ‘≠–‘µƒ«ø»ı£¨ø…“‘≈–∂œ—ıªØªπ‘≠∑¥”¶ƒÐ∑Ò∑¢…˙°£
[¥∞∏]
(1)—ı«Ë°° HSCN°° KOCN
(2)¢Ÿ(CN)2+2KOH====KCN+KOCN+H2O
¢⁄(CN)2+2SCN£≠====2CN£≠+(SCN)2
¿˝1.(09ƒÍ»´π˙1æÌ)“—÷™÷Ð∆⁄±Ì÷–£¨‘™ÀÿQ°¢R°¢W°¢Y”Α™ÀÿXœý¡⁄°£Yµƒ◊Ó∏þªØ∫œº€—ıªØŒÔµƒÀÆªØŒÔ ««øÀ·°£ªÿ¥œ¬¡–Œ £∫
(1)W”ÎQø…“‘–Œ≥…“ª÷÷∏þŒ¬Ω·ππÃ’¥…≤ƒ¡œ°£Wµƒ¬»ªØŒÔ∑÷◊”≥ ’˝Àƒ√ÊÃÂΩ·ππ£¨Wµƒ—ıªØŒÔµƒæßÿý–Õ « °°°°°°°°°°°°°°°°°°°°°°£ª
(2)Qµƒæþ”–œýÕ¨ªØ∫œº€«“ø…“‘œýª•◊™±‰µƒ—ıªØŒÔ «°°°°°°°°°°°°°°°°°° £ª
(3)R∫ÕY–Œ≥…µƒ∂˛‘™ªØ∫œŒÔ÷–£¨R≥ œ÷◊Ó∏þªØ∫œº€µƒªØ∫œŒÔµƒªØ—ß Ω «°°°°°°°°°°°° £ª
(4)’‚5∏ˆ‘™Àÿµƒ«‚ªØŒÔ∑÷◊”÷–£¨¢Ÿ¡¢ÃÂΩ·ππ¿ý–ÕœýÕ¨µƒ«‚ªØŒÔµƒ∑–µ„¥”∏þµΩµÕ≈≈¡–¥Œ–Ú «(Ãѧ Ω)°°°°°°°°°°°°°°°° £¨∆‰‘≠“Ú «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°£ª
¢⁄µÁ◊”◊Ð ˝œýÕ¨µƒ«‚ªØŒÔµƒªØ—ß Ω∫Õ¡¢ÃÂΩ·ππ∑÷± «°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° £ª
(5)W∫ÕQÀ˘–Œ≥…µƒΩ·ππÃ’¥…≤ƒ¡œµƒ“ª÷÷∫œ≥…∑Ω∑®»Áœ¬£∫Wµƒ¬»ªØŒÔ”ÎQµƒ«‚ªØŒÔº”»»∑¥”¶£¨…˙≥…ªØ∫œŒÔW(QH2)4∫ÕHCL∆¯Ã£ªW(QH2)4‘⁄∏þŒ¬œ¬∑÷Ω‚…˙≥…Qµƒ«‚ªØŒÔ∫Õ∏√Ã’¥…≤ƒ¡œ°£…œ ˆœýπÿ∑¥”¶µƒªØ—ß∑Ω≥à Ω(∏˜ŒÔ÷ ”√ªØ—ß Ω±Ì æ) «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
[Ω‚Œˆ]±æÂø…Ω·∫œŒ Â◊˜¥°£Wµƒ¬»ªØŒÔŒ™’˝ÀƒÃ–գ¨‘Ú”¶Œ™SiCl4ªÚCCl4£¨”÷W”ÎQ–Œ≥…∏þŒ¬Ã’¥…£¨π ø…Õ∆∂œWŒ™Si°£(1)SiO2Œ™‘≠◊”æßð£(2)∏þŒ¬Ã’¥…ø…¡™œÎµΩSi3N4,QŒ™N£¨‘Ú”–NO2”ÎN2O4÷ƺ‰µƒœýª•◊™ªØπÿœµ°£(3)Yµƒ◊Ó∏þº€—ıªØµƒµƒÀƪ،Ԍ™«øÀ·£¨«“”ÎSi°¢Nµ»œý¡⁄£¨‘Ú÷ªƒÐ «S°£RŒ™As£¨À˘“‘Rµƒ◊Ó∏þº€ªØ∫œŒÔ”¶Œ™As2S5°£(4)œ‘»ªxŒ™P‘™Àÿ°£¢Ÿ«‚ªØŒÔ∑–µ„À≥–ÚŒ™NH3> AsH3 > PH3,“ÚŒ™«∞’þ÷–∫¨”–«‚º¸∫Û¡Ω’þππ–ÕœýÕ¨£¨∑÷◊”º‰◊˜”√
¡¶≤ªÕ¨°£¢⁄SiH4°¢PH3∫ÕH2SµƒµÁ◊” ˝æ˘Œ™18°££¨Ω·ππ∑÷±Œ™’˝Àƒ√Ê㨻˝Ω«◊∂∫ÕV–Œ°£(5)”…Â÷–À˘∏¯≥ˆµƒ∫¨◊÷ƒ∏µƒªØ—ß Ωø…“‘–¥≥ˆæþõƒŒÔ÷ £¨»ª∫Û≈‰∆Ωº¥ø…
[¥∞∏](1)‘≠◊”æßð£(2)NO2∫ÕN2O4(3)As2S5°£(4)¢ŸNH3> AsH3 > PH3,“ÚŒ™«∞’þ÷–∫¨”–«‚º¸,∫Û¡Ω’þππ–ÕœýÕ¨£¨∑÷◊”º‰◊˜”√¡¶≤ªÕ¨£ª¢⁄µÁ◊” ˝œýÕ¨µƒ”–SiH4°¢PH3∫ÕH2SΩ·ππ∑÷±Œ™’˝Àƒ√Ê㨻˝Ω«◊∂∫ÕV–Œ°£(5)SiCl4 + 4NH3 = Si(NH2)4 + 4HCl£¨3Si(NH2)4 = 8NH3 + Si3N4
¿˝2.(1)«ËªØºÿ°¢«ËªØ«‚µƒ÷∆±∏∑¥”¶ ΩŒ™£∫
K2CO3+C+2NH3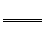 2KCN+3H2O£ª°˜H£Ω+276kJ£Ømol°° ¢Ÿ
2KCN+3H2O£ª°˜H£Ω+276kJ£Ømol°° ¢Ÿ
°°°°°°°° CO+NH3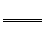 HCN+H2O£ª°˜H£Ω+46kJ£Ømol°° ¢⁄
HCN+H2O£ª°˜H£Ω+46kJ£Ømol°° ¢⁄
«Ë¿Î◊”Œ™∏∫“ªº€(CN-)£¨∆‰÷–úµ™‘™ÀÿµƒªØ∫œº€∑÷±Œ™________°£ “‘…œ¡Ω∏ˆ∑¥”¶ «∑Òæ˘Œ™—ıªØªπ‘≠∑¥”¶£ø
(2)÷∆±∏¥ø檌ÞÀÆHCN(∑–µ„299K)µƒ¡Ì“ª÷÷∑Ω∑® « £∫ªÏ∫œƒ•œ∏µƒKCN∫ÕKHS∑€ƒ© ∂»º”»»¢Ÿ ‘–¥≥ˆ’‚∏ˆ∑¥”¶ Ω°£¢⁄Œ™ ≤√¥“™ƒ•œ∏∫Õ”√∑€ƒ©£ø¢€Œ™ ≤√¥“™«øµ˜ ∂»º”»»£ø
[Ω‚Œˆ]æðπ≤º€º¸¿Ì¬€£¨“ª∞„µ±ÃºÕ¨∑«Ω Ù–‘±»À¸«øµƒ‘™ÀÿΩ·∫œ ±£¨Ãºœ‘’˝º€£¨µ™Œ™∏∫º€£¨Œ™-3º€£¨À˘“‘(CN-)÷–úŒ™+2º€£¨µ™Œ™-3º€°£π ¢ŸŒ™—ıªØªπ‘≠∑¥”¶£¨¢⁄Œ™∑«—ıªØ ªπ‘≠∑¥”¶°£µ⁄∂˛÷÷∑Ω∑®÷∆±∏HCN «πÃÔÎπÃÃÂ÷ƺ‰µƒ∑¥”¶£¨π ƒ•œ∏∫Õ”√∑€ƒ©µƒƒøµƒ «‘ˆ¥Û±Ì√ʪ˝£¨º”øÏ∑¥”¶ÀŸ¬ £¨æð“‚÷™£¨µ⁄∂˛÷÷∑Ω∑®÷∆±∏HCN»ÁŒ¬∂»Ã´µÕ£¨∑¥”¶ÀŸ¬ Ωœ–°£¨Œ¬∂»Ã´∏þ£¨‘ÚÀ· Ω—Œ“◊∑÷Ω‚∑¢…˙∏±∑¥”¶£∫2KHS
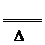 K2S+H2S°¸°£∏√∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™KCN+KHS
K2S+H2S°¸°£∏√∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™KCN+KHS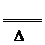 HCN°¸+K2S°£
HCN°¸+K2S°£
[¥∞∏]
(1)-3°¢¢ŸŒ™—ıªØªπ‘≠∑¥”¶£¨¢⁄Œ™∑«—ıªØªπ‘≠∑¥”¶°£
(2)KCN+KHS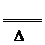 HCN°¸+K2S°£°° µ⁄∂˛÷÷∑Ω∑®÷∆±∏HCN «πÃÔÎπÃÃÂ÷ƺ‰µƒ∑¥”¶£¨π ƒ•œ∏∫Õ”√∑€ƒ©µƒƒøµƒ «‘ˆ¥Û±Ì√ʪ˝£¨º”øÏ∑¥”¶ÀŸ¬ .
HCN°¸+K2S°£°° µ⁄∂˛÷÷∑Ω∑®÷∆±∏HCN «πÃÔÎπÃÃÂ÷ƺ‰µƒ∑¥”¶£¨π ƒ•œ∏∫Õ”√∑€ƒ©µƒƒøµƒ «‘ˆ¥Û±Ì√ʪ˝£¨º”øÏ∑¥”¶ÀŸ¬ .
2°¢π˙Õ‚£∫—«÷Þ–Ì∂ýπ˙º“Ω” СÀ»Âº“ŒƒªØ£¨ø◊◊”‘⁄ ¿ΩÁ»À¿ý÷–”–…Óπ„”∞œÏ£¨”»∆‰∂‘∂´—«÷Óπ˙≤˙…˙π˝÷ÿ¥Û”∞œÏ°£
æð ∑ºÆ‘ÿ£¨‘Á‘⁄∫∫Ã∆÷Æ ±£¨»Âº“µ‰ºÆ±„¥´»Î≥Øœ °¢»’±æ°¢‘Ωƒœº∞∂´—«“ª–©π˙º“£¨≤¢”∞œÏ¡ÀÀ˚√«µƒ’˛÷Œ°¢ŒƒªØ°¢¬◊¿Ì∫Õ∑Áœ∞µ»…Áª·…˙ªÓµƒ∏˜∏ˆ∑Ω√Ê°£”––©—ß’þΩ´’‚“ª¿˙ ∑œ÷œÛ≥∆÷ÆŒ™°∞ø◊◊”ŒƒªØ»¶°±ªÚ°∞»ÂΩÃŒƒªØ»¶°±°£À˚√«∑«≥£÷ÿ ”»Âº“¬◊¿ÌÀºœÎ£¨…ı÷¡Ω´ƒ≥–©Ã∏¬€»Âº“¬◊¿ÌµƒŒƒ’¬—°Ω¯÷––°—ßøŒ±æ÷–£¨»Á–¬º”∆¬‘¯∞—°∞»Âº“¬◊¿Ì°±∂®Œ™÷–—ß…˙±ÿ∂¡øŒ°£≥Øœ °¢‘Ωƒœ°¢»’±æµ»π˙º“‘⁄∆‰¿˙ ∑∑¢’ππ˝≥Ã÷–£¨“—∞—»Âº“»⁄»Î±æ√Ò◊µƒ¥´Õ≥ŒƒªØ÷Æ÷–°£
¿ΩÁø¥ø◊◊”£∫
√¿π˙ŒƒªØ≤ø≥§Àµ£∫ø◊◊”µƒ»À∏Ò”ÎÀ˚µƒ“µº®£¨÷µµ√ еΩ÷–π˙∫Õ»´ ¿ΩÁ»À√Òµƒ◊Ó∏þ楓‚°£
°°°° ∑®π˙ŒƒªØ≤ø≥§Àµ£∫¥”æ√‘∂µƒƒÍ¥˙ø™ º£¨≈∑÷ÞæÕ≥–»œ¡Àø◊◊”’‚Œª÷–π˙∫Õ»´ ¿ΩÁ÷¯√˚µƒÀºœÎº“”ΒЗߺ“°£
¡™∫œπ˙ΩÃø∆Œƒ◊È÷Ø∞—ø◊◊”¡–Œ™”∞œÏ ¿ΩÁΩ¯≥õƒ Æ¥ÛŒƒªØ√˚»À÷Æ ◊£ª
°∞»À¿ý“™‘⁄21 ¿ºÕ…˙¥Êœ¬»•£¨±ÿ–ΪÿµΩ2500ƒÍ«∞£¨¥”ø◊◊”ƒ«¿Ô—∞’“÷«ª€°£°±-- ¿ΩÁ75Œª≈µ±¥∂˚Ω±ªÒµ√’þ∆¿º€ø◊◊”°£
ø◊◊”µƒÀºœÎ1993ƒÍ9‘¬±ª»´«Ú÷˜“™◊⁄Ωõƒ¥˙±Ì»À◊˜Œ™»À¿ý∫Õ∆Ωπ≤¥Êµƒª˘±æ‘≠‘Ú–¥»Î°∂◊þœÚ»´«Ú¬◊¿Ì–˚—‘°∑
ø◊◊”ÀºœÎ∂‘ ¿ΩÁ”∞œÏ…Ó‘∂
°°»Â—ß‘⁄»’±æ
°° Ð÷–ª™ŒƒªØ”∞œÏ◊Ó‘Áµƒ «»’±æ°£ø◊◊”‘⁄»’±æµƒ”∞œÏ≤ª—«”⁄‘⁄÷–π˙±æÕ¡°£°°¿˝»Á£¨»Âº“µƒ°∞√ұ氱ÀºœÎ≥…Œ™◊‘”…√Ò»®ÀºœÎº“◊þ…œ◊∑«Û√Ò÷˜÷Ƭ∑µƒ«≈¡∫£ª»Âº“µƒ°∞“¿˚÷Ʊʰ±≥…Œ™»’±æ◊ ±æ÷˜“–À∆∫Õ∑¢’𵃵¿µ¬÷ß÷˘£ª»Âº“µƒ°∞÷“–¢°±π€ƒÓŒ™Ω¸¥˙»’±æµƒπ˙º“∫Õ∆Û“µ∑˛ŒÒ£ª»Âº“µƒ°∞÷–”π°±∏≈ƒÓ”√¿¥–≠µ˜»’±æµƒœ÷¥˙’˛÷Œµ»µ»°£
∫´π˙◊»Â◊Ó…ı
°°ø◊◊”‘⁄∫´π˙±ª◊Œ™°∞¥Û≥…÷¡ •Œƒ–˚Õı°±°£«ß∞ŸƒÍ¿¥£¨∫´π˙√øƒÍ∂ºæŸ–– ¢¥Ûµƒ°∞ յϥۺ¿°±ºÕƒÓø◊◊”µÆ≥Ω°£»Â—ßÕ‚¥´µƒ“ª«ß∂ýƒÍ¿¥£¨∫´π˙ л—ߔ∞œÏ◊Ó…Ó°£°°
ø◊◊””⁄Ã∆ø™‘™∂˛ Æ∆þƒÍ(739)±ª◊∑⁄÷°∞Œƒ–˚Õı°±°£«ÂÀ≥÷Œ∂˛ƒÍ(1645)”˘∂®Œƒ√Ì⁄÷∫≈Œ™°∞¥Û≥…÷¡ •Œƒ–˚œ» ¶ø◊◊”°±£ª ÆÀƒƒÍ(1657)£¨∏ƒ≥∆°∞÷¡ •œ» ¶ø◊◊”°±°£
1°¢π˙ƒ⁄£∫
¢Ÿ¥¥∞ÏÀΩ—ß£∫ø◊◊”¥¥∞Ï¡ÀÀΩ—ß£¨¥Ú∆∆¡À“‘Õ˘πŸ∑Ω¬¢∂œ∞Ï—ßµƒ¥´Õ≥£¨ø™¥¥¡À°∞—ß‘⁄√Òº‰°±µƒ–¬ƒ£ Ω£¨∂‘÷–ª™√Ò◊ÂŒƒªØµƒΩ®ππ”Î¥´≥–∆µΩ¡À÷ÿ“™◊˜”√°£
¢⁄÷˜’≈°∞ƒ⁄ •Õ‚Õı°±£∫ ø◊◊”÷˜’≈µƒ°∞ƒ⁄ •Õ‚Õı°±£¨≥…Œ™÷–π˙π≈¥˙»À÷Œ…Áª·ø™√˜æ˝÷˜∫Õ’˛÷Œ»À≤≈µƒ¿ÌœÎ±Í◊º°£
¢€ø◊◊”À˘¥¥¡¢µƒ»Âº“ÀºœÎ∂‘÷–π˙…Áª·≤˙…˙¡À≥§æ√µƒ”∞œÏ£∫Œ˜∫∫°∞∞’˜Ì∞Ÿº“,∂¿◊»Â ı°±∫Û,»Âº“ÀºœÎΩ•≥…÷–π˙¥´Õ≥…Áª·µƒ÷˜¡˜ÀºœÎ,∂‘∫Û ¿≤˙…˙¡À…Ó‘∂”∞œÏ°£
4°¢ø◊◊”µƒΩÔ˝ÀºœÎ
¢Ÿ¥¥∞ÏÀΩ—ß£¨¥Ú∆∆πŸ∑Ω¬¢∂œ∞Ï—ßµƒ¥´Õ≥°£
¢⁄ΩÔ˝∂‘œÛ£∫ø◊◊”≥´µº°∞”–ΩÌ޿ý°±¿©¥Û¡ÀΩÔ˝∂‘œÛ°£¥”∂¯ πŒƒªØΩÔ˝œ¬“∆°£
¢€ΩÃ—ß µº˘£∫÷ÿ ”∆Ù∑¢—ß…˙µƒ◊‘æı–‘°¢÷˜∂Ø–‘°¢«øµ˜ µ ¬«Û «µƒ—ßœ∞è∂»°£°∞÷™÷Æ’þ≤ª»Á∫√÷Æ’þ£¨∫√÷Æ’þ≤ª»Á¿÷÷Æ’þ°±£¨°∞÷™÷ÆŒ™÷™÷Æ£¨≤ª÷™Œ™≤ª÷™£¨ «÷™“≤°±°£
¢ÐΩ×ß∑Ω∑®£∫…∆”⁄°∞“Ú≤ƒ ©Ωð±
¢ð—ßœ∞∑Ω∑®£∫«øµ˜—ß”ÎÀºµƒπÿœµ£¨—ßœ∞”Î∏¥œ∞µƒπÿœµ°£°∞—ß∂¯≤ªÀº‘ÚÿË£¨Àº∂¯≤ª—ß‘Ú¥˘°£°±
¢Þ≈ý—¯ƒø±Í£∫«øµ˜µÐ◊”“™”–≈®∫Òµƒ≤Œ’˛“‚ ∂°£°∞—ß∂¯”≈‘Ú À°±°£
◊ðπ€ø◊◊”µƒ“ª…˙£¨À˚∂‘À˚µƒ—ß…˙µƒ”∞œÏ£¨“ª≤ø∑÷ «Õ®π˝—‘¥´£¨Õ®π˝—ßœ∞π≈¥˙Œƒœ◊°¢¥´ ⁄∏˜÷÷ºº“’£¨∂¯∏¸∂ýµƒ°¢∏¸Œ™…Óøõƒ‘Ú «…ÌΩð£À˚µƒ«⁄∑Ð∫√—ߣ¨À˚∂‘’Ê¿Ì°¢∂‘¿ÌœÎ°¢∂‘ÕÍ√¿»À∏Òµƒ◊∑«Û£¨À˚µƒ’˝÷±°¢…∆¡º°¢«´–È°¢”–¿Ò£¨À˚∂‘π˙º“µƒ÷“≥œ”Î∂‘¿œ∞Ÿ–’µƒπÿ–ƒ£¨∂º…Ó…Óµÿ∏–»æ◊≈À˚µƒ—ß…˙”Î∫Û»À°£—œ∏Ò“™«Û◊‘º∫£¨“‘…Ì◊˜‘Ú£¨º» «ø◊◊”µƒ∏þ…– ¶µ¬£¨“≤ «ø◊◊”÷≥ˆµƒ“ªÃıΩÔ˝‘≠‘Ú°£ø◊◊”∞ÆΩÔ˝°¢∞Æ—ß…˙£¨ªÂ»À≤ªæΣ¨À˚ƒÐ∆Ωµ»∂‘¥˝—ß…˙£¨◊ˆµΩΩ×ߜý≥§£¨—œ∏Ò“™«Û◊‘º∫°¢“‘…Ì◊˜‘Ú°£ø◊◊” «æþ”–∏þ…– ¶µ¬µƒ“ª¥˙◊⁄ ¶°£°°
ø◊◊”µƒµÐ◊”÷–£¨”––©»Àº∏∫ı «÷’…˙≈„∞È◊≈ø◊◊”£¨∆‰«È∏–÷Æ…Ó£¨ §”⁄∏∏◊”–÷µÐ°£ø◊◊”À¿∫Û£¨±ª‘·”⁄«˙∏∑≥«±±µƒ„ÙÀÆ∞∂±þ£¨µÐ◊”√«“‘∂‘∏∏«◊÷Æ¿Ò“«∂‘¥˝ø◊◊”£¨Œ™∆‰∑˛…•3ƒÍ°£◊”π±‘⁄ø◊◊”µƒ∑ÿ«∞∏«¡À“ªº‰–°Œð£¨Œ™ø◊◊” ÿ∑ÿ6ƒÍ°£÷–π˙¿˙ ∑…œ¥¥∞ÏÀΩ—ßµƒœ»––’þ£¨µ⁄“ªŒª÷∞“µΩà ¶£¨µ√µΩ¡ÀµÐ◊”√«µƒ÷‘–ƒ◊楰£
ø◊◊”±ª∫Û ¿◊Œ™°∞ÕÚ ¿ ¶±Ì°±£¨≥…Œ™◊Ó∏∫ ¢√˚µƒŒ∞¥ÛΩÔ˝º“°£
3°¢∫À–ƒƒ⁄»ð£∫¿Ò∫Õ» µƒÀºœÎ
(1)°∞¿Ò°±µƒÀºœÎ
¢Ÿ∫¨“£∫°∞÷пҰ±(÷∏Œ˜÷ÐΩ®¡¢µƒ“‘∑÷∑‚÷∆∫Õ◊⁄∑®÷∆Œ™∫À–ƒµƒµ»º∂√˚∑÷÷∆∂».)
¢⁄¿Òµƒ µº˘∑Ω∑®£∫°∞øÀº∫∏¥¿Ò°±£¨°∞’˝√˚°±
(’˝√˚£∫÷∏∞¥’’÷пҵƒ÷∆∂»∞—µ± ±“—æ≠ªÏœ˝¡Àµƒ…Áª·µ»º∂÷»–ÚΩ√’˝π˝¿¥£¨¥ÔµΩ√˚’˝—‘À≥)
¢€°∞¿Ò°±µƒ÷˜“™ƒ⁄»ð£∫◊◊”Ϋ◊«◊
a°¢”⁄…Áª·£∫Ω®¡¢æ˝æ˝°¢≥º≥º°¢∏∏∏∏°¢◊”◊”µƒ…Áª·÷»–Ú
°°b°¢”⁄∏ˆ»À£∫∑«¿ÒŒ ”°¢∑«¿ÒŒÃ˝°¢∑«¿ÒŒ—‘°¢∑«¿ÒŒ∂Ø
(2)°∞» °±µƒÀºœÎ
¢Ÿ∫¨“£∫°∞∞Æ»À°±[»˝≤„ƒ⁄»ð:1°¢∞Æ◊‘º∫µƒ«◊»À;2°¢∞ÆÀ˚»À;3°¢Õ≥÷Œ µ––» ’˛]
¢⁄∑Ω∑®£∫°∞÷“À° °±÷Ƶ¿
(°∂¬€”Ô Æ‘Ú°∑◊”π±Œ ‘ª£∫°∞”–“ª—‘ø…“‘÷’…Ì––÷Æ’þ∫ı£ø°±◊”‘ª£∫°∞∆‰À°∫ı£°º∫À˘≤ª”˚£¨Œ ©”⁄»À°£°±(°∞≈≠°±)°° °∞º∫”˚¡¢∂¯¡¢»À£¨º∫”˚¥Ô∂¯¥Ô»À°£°±(°∞÷“°±)
¢€±Ìœ÷£∫∂‘”⁄Õ≥÷ŒΩ◊º∂£∫°∞Œ™’˛“‘µ¬°± --√Ò±æÀºœÎ
∂‘”⁄∆’Õ®»À£∫–¢æ¥∏∏ƒ∏£¨◊楖÷≥§
(∑¥”≥»Âº“◊¢÷ÿº“Õ•¬◊¿Ìπÿœµµƒ∫Õ–≥£¨≤¢÷˜’≈Ω´∫Õ–≥µƒº“Õ•µƒ¬◊¿Ì¿©’πµΩ…Áª·…œ£¨¥”∂¯¿¥Œ»∂®…Áª·÷»–Ú°£)
°° (3)» ∫Õ¿Òµƒπÿœµ£∫œý∏®œý≥…°¢≤ªø…∑÷∏Ó£¨°∞øÀº∫∏¥¿ÒŒ™» °±°∞»À∂¯≤ª» £¨»Á¿Ò∫Œ£ø°±
2°¢ƒøµƒ£∫Õ®π˝ª÷∏¥÷пң¨≥–µ£¥´≥–ŒƒªØ∫Õ∏ƒ…∆»Àº πÿœµµƒ…Áª·µ¿“°£
1°¢Ãıº˛
(1) ±¥˙“ÚÀÿ£∫¥∫«Ô…Áª·¥Û±‰∏Ô ±¥˙°£°∞¿Ò±¿¿÷ªµ°±
¢Ÿæ≠º√£∫ÀΩ”–Õ¡µÿ≥ˆœ÷£¨æÆÃÔ÷∆ÕþΩ‚°£
¢⁄’˛÷Œ£∫Õı “À•Œ¢£¨÷Ó∫Ó’˘∞‘£¨∑÷∑‚÷∆◊þœÚ±¿¿£°£
¢€ŒƒªØ£∫ÀΩ—ß–À∆£¨ŒƒªØœ¬“∆£¨–Œ≥…°∞ ø°±Ω◊≤„°£
ÀÊ◊≈Œ˜÷ÐÕ≥÷Œµƒ±¿¿££¨÷Ð∆ΩÕı∂´«®£¨…Áª·–Œ ∆ªÏ¬“£¨Õı “’∆πÐ¥´Õ≥ŒƒªØ—ß ıµƒπŸ¿Ù¡˜…¢µΩ÷бþ∏˜π˙£¨À˚√«À˘’∆Œ’µƒ—ß ı∫Õƒ≥–©µ‰ºÆ“≤¡˜…¢µΩ∏˜π˙°£¥∫«Ô∫Û∆⁄£¨“ª–©ŒƒªØ÷∞ ¬»À‘±“—≤ªƒÐ±£≥÷ ¿œÆæÙ¬ª£¨”⁄ «Õ—¿ÎπŸ∏Æ£¨…¢¬‰√Òº‰£¨“‘∆‰’∆Œ’µƒŒƒªØ°¢—ß ı÷™ ∂ƒ±…˙£¨≥…Œ™ øΩ◊≤„°£À˚√«¥¥∞ÏÀΩ—ß£¨π„ ’√≈ÕΩ£¨¥´≤•≤ªÕ¨µƒ÷™ ∂£¨–˚—Ô◊‘º∫µƒπ€µ„£¨÷Ω•–Œ≥…¡À∞Ÿº“’˘√˘µƒæ÷√Ê£¨’‚ «÷–π˙ŒƒªØÀºœÎµƒª‘ªÕ ±¥˙°£
¬≥π˙Œ™÷Ðπ´µ©÷Æ◊”≤Æ«ð∑‚µÿ£¨∂‘÷Ð¥˙ŒƒŒÔµ‰ºÆ±£¥ÊÕÍ∫√£¨Àÿ”–°∞¿Ò¿÷÷Æ∞Ó°±÷Æ≥∆°£¬≥œÂπ´∂˛ Ææ≈ƒÍ(«∞544ƒÍ)Œ‚π´◊”ºæ‘˝π€¿÷”⁄¬≥£¨Ã挙π€÷𰣬≥’—π´∂˛ƒÍ(«∞540ƒÍ)Ω˙¥Û∑Ú∫´–˚◊”∑√¬≥£¨π€ È∫Û‘ÞÃæ°∞÷пÒæ°‘⁄¬≥“”£°°±¬≥π˙ŒƒªØ¥´Õ≥”ε± ±—ß ıœ¬“∆µƒ–Œ ∆∂‘ø◊◊”ÀºœÎµƒ–Œ≥…”–∫Ð¥Û”∞œÏ°£ °°
(2)¿˙ ∑¥´Õ≥£∫ °∞»Â°±µÿŒªµƒ±‰ªØ
¥∫«Ô“‘«∞£¨»Â «÷˜≥÷¿Ò“«µƒŒ◊°¢ ∑°¢◊£°¢≤∑“ª¿ýµƒŒƒªØ»À£ª¥∫«Ô ±∆⁄£¨»Â“‘œý¿ÒŒ™“µ£¨ªÚŒ™»À ¶°£
(3)∏ˆ»À◊˜”√£∫≥Á∞ð÷Ðπ´£¨æ´Õ®¿Ò¿÷£¨≥‰¬˙∫Ηԥ´Õ≥ŒƒªØ°¢∏¥–À÷пҵƒ π√¸∏–
À˚ø™√≈ ⁄ÕΩ£¨œý¥´”–µÐ◊”3000»À£¨∆‰÷–”–72œÕ»À£¨Ω´∆‰—ßÀµ∫ÕÀºœÎºÃ≥–”Î∑¢—Ô£¨–Œ≥…¡À“ª∏ˆ“‘ø◊◊”Œ™÷––ƒµƒÀºœÎ¡˜≈…--»Âº“°£
5°¢Õ̃͜◊…ÌŒƒΩã∫’˚¿Ìµ‰ºÆ°¢œ◊…ÌΩÔ˝ ¬“µ
”…”⁄’˛÷Œ¿ÌœÎ∆∆√£¨ø◊◊”‘¯’˚¿Ì≥ˆ°∂ ´°∑°∂ È°∑°∂¿Ò°∑°∂“◊°∑°∂¿÷°∑°∂¥∫«Ô°∑µ»µ‰ºÆ°£∂‘÷–ª™ŒƒªØµƒ¥´≥–◊ˆ≥ˆ¡ÀæÞ¥Ûµƒπ±œ◊°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com