
3£®Ī÷ŗŗĪäµŪŹ±ĘŚ£¬Ä³ČĖøøĒ×ÓėĖūČĖ¶·Å¹£¬Ęä×Ó°ļƦÓĆľ¹÷Č„“ņĖūČĖ£¬²»ĮĻČ“ĪóÉĖĘäøø”£°“ÕÕµ±Ź±·ØĀÉ£¬Å¹ÉĖøøĒ׏ĒÓ¦“¦čɏ׵ÄĖĄ×ļ”£Ķ¢Ī¾ÕÅĢĄĒė½Ģ¶ÖŁŹęÓ¦ČēŗĪ“¦Ąķ”£¶ÖŁŹęČĻĪŖ£ŗøø×ÓŹĒ×īĒ×½üµÄ£¬ĢżĖµøøĒ×ÓėČĖ¶·Å¹£¬¶ł×Ó×ŌČ»½ōÕÅ£¬ŅŖÄĆľ¹÷Č„¾Č»¤øøĒ×£¬ÖĮÓŚĪóÖŠøøĒײ¢·Ē±¾Ņā£¬Ó¦øĆĪŽ×ļŹĶ·Å”£øƶĪ²ÄĮĻ·“Ó³ĮĖĪ÷ŗŗ”””””””””””””””””” (”””” )
”””” A£®ŅŃ¾·Ļ³żĮĖŃĻŠĢ¾ž·Ø”””””””””””””””””” ”” ””””””””””””
”””” B£®Čå¼ŅĀץķĖ¼ĻėÉųĶøµ½·ØĀÉÖ®ÖŠ
”””” C£®æŖŹ¼ĶĘŠŠÅŠĄżÉóÅŠÖĘ”””””””””””””” ””””””””””””””””””
”””” D£®·Ļ³żĮĖŌŹ¼Éē»įĶ¬Ģ¬ø“³šŌŌņ
2£®ĒŲŹ±ŹµŠŠæ¤ĻŲĮ½¼¶ŠŠÕžÖʶȔ£ø£½ØµŲÓņÉĻÖ÷ŅŖÓŠĆö֊椣¬µ±Ź±ø£ÖŻŹōĆö֊椹ÜĻ½£¬øł¾ŻĖłŃ§ÖŖŹ¶ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” (”””” )
”””” ¢Łµ±Ź±æ¤ŹŲµÄÖ°Ī»ÓÉÖŠŃėČĪĆü£¬²»æÉŅŌŹĄĻ®””
”””” ¢Śæ¤ŹŲŹĒĆöÖŠæ¤×īøߵĊŠÕž³¤¹Ł
”””” ¢ŪĆöÖŠæ¤ÓŠČØČĪĆāĻ½ĒųÄŚµÄĻŲĮī””
”””” ¢Üø£ÖŻŹĒĆöÖŠæ¤æ¤ŹŲµÄ·āµŲ
”””” A£®¢Ł¢Ś¢Ū¢Ü”””” ”””””””””” B£®¢Ś¢Ū¢Ü”””””””””””” C£®¢Ł¢Ś”””””””””””””””””””””””” D£®¢Ł¢Ü
1£®×Ś·ØÖʵĆŅŌĪ¬ĻµµÄÖŲŅŖŅņĖŲŹĒŃŖŌµ¹ŲĻµ”£ŅŌĻĀ×īÄÜÖ¤Ć÷ÕāŅ»¹ŪµćµÄ²ÄĮĻŹĒ ”””””””” (”””” )
”” A£®æ××ÓĖµ£ŗ”°ÖÜŅņÓŚŅóĄń£¬ĖłĖšŅę£¬æÉÖŖŅ²”””±
”” B£®ĖµĪĽā×Ö”·ŌŲ£ŗ”°×Ś£¬×š×ęĆķŅ²”””±””
”” C£®×ó“«”·ŌŲ£ŗ”°Ģģ×ӽعś£¬ÖīŗīĮ¢¼Ņ”””±
”” D£®×ó“«”·ŌŲ£ŗ”°¹ŹĶõ³¼¹«£¬¹«³¼“ó·ņ”””±
2.0mol”¤L£1NaOHČÜŅŗÖŠ£¬³ä·Ö·“Ó¦”£NaOH
ČÜŅŗµÄĢå»żV”Ż””””””””””””””
””
”” (2)¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘĮæ¹ĢĢ唣øĆ²½ÖčÖŠČōĪ“Ļ“µÓ¹ĢĢ壬²āµĆĆ¾µÄÖŹĮæ·ÖŹż½« ””””””(Ģī”°Ę«øß”±»ņ”°Ę«µĶ”±)
[Ģ½¾æ¶ž] ŹµŃé·½°ø£ŗĀĮĆ¾ŗĻ½š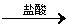 ²ā¶ØÉś³ÉĘųĢåµÄĢå»ż
²ā¶ØÉś³ÉĘųĢåµÄĢå»ż
ŹµŃé×°ÖĆČēÓŅĶ¼£¬ĪŹĢāĢÖĀŪ£ŗ””””
”” (3)ijĶ¬Ń§Ģį³öøĆŹµŃé×°ÖĆ²»¹»ĶźÉĘ£¬Ó¦ŌŚA”¢BÖ®¼äĢķ¼ÓŅ»øöøÉŌļ”¢³żĖįĪķµÄ×°ÖĆ”£ÄćµÄŅā¼ūŹĒ£ŗ”””””””””” (Ģī”°ŠčŅŖ”±»ņ”°²»ŠčŅŖ”±)”£
”” (4)ĪŖŹ¹²ā¶Ø½į¹ū¾”æÉÄܾ«Č·£¬ŹµŃé֊ӦעŅāµÄĪŹĢāŹĒ(Š“³öĮ½µć)£ŗ
¢Ł”””””””””””””””””” ””””””””””””””””””””””””””””””””
¢Ś”””””””””” ””””””””””””””””””””””””””””””””””””””””””
29£®(13·Ö)ĀĮĆ¾ŗĻ½šŅŃ³ÉĪŖĀÖ“¬ÖĘŌģ”¢»Æ¹¤Éś²śµČŠŠŅµµÄÖŲŅŖ²ÄĮĻ”£ŃŠ¾æŠŌѧĻ°Š”×éµÄČżĪ»Ķ¬Ń§£¬ĪŖ²ā¶Øijŗ¬Ć¾3%-5%µÄĀĮĆ¾ŗĻ½š(²»ŗ¬ĘäĖüŌŖĖŲ)ÖŠĆ¾µÄÖŹĮæ·ÖŹż£¬Éč¼ĘĻĀĮŠČżÖÖ²»Ķ¬ŹµŃé·½°ø½ųŠŠĢ½¾æ”£ĢīŠ“ĻĀĮŠæÕ°×”£
[Ģ½¾æŅ»]”” ŹµŃé·½°ø£ŗĀĮĆ¾ŗĻ½š 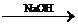 ””²ā¶ØŹ£Óą¹ĢĢåÖŹĮæ
””²ā¶ØŹ£Óą¹ĢĢåÖŹĮæ
ŹµŃéÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ””””””””””””””””””””””””””””””””””””””””
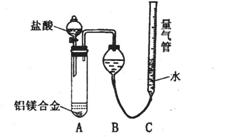 ŹµŃé²½Öč£ŗ
ŹµŃé²½Öč£ŗ
”” (1)³ĘČ”5£®4gĀĮĆ¾ŗĻ½š·Ūĩѳʷ£¬Ķ¶ČėVmL
28£®(11·Ö)ÓŠŅ»³ĪĒåĶøĆ÷µÄČÜŅŗ£¬æÉÄÜÓŠNH4+”¢Fe3+”¢H+”¢Mg2+”¢Al3+”¢I-”¢CO32-µČĄė×Ó£¬ĻÖ·Ö±šČ”ČÜŅŗ½ųŠŠĻĀĮŠŹµŃé£ŗ
”” (1)¼ÓČėÅØäåĖ®£¬ČÜŅŗ±äĪŖŗÖÉ«£»
”” (2)¼ÓČėµķ·Ū£¬Ī“¼ūĄ¶É«£»
”” (3)ŌŚÖšµĪ¼ÓČė1mol”¤L-1NaOHČÜŅŗµÄ¹ż³ĢÖŠ£¬
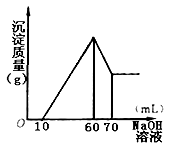 Ī“Īŵ½“Ģ¼¤ŠŌĘųĢ壬ĖęNaOHČÜŅŗµÄµĪČė£¬
Ī“Īŵ½“Ģ¼¤ŠŌĘųĢ壬ĖęNaOHČÜŅŗµÄµĪČė£¬
²śÉś³ĮµķµÄĮæČēĶ¼ĖłŹ¾£¬ŹŌČ·¶Ø£ŗ
¢ŁČÜŅŗÖŠŅ»¶Ø“ęŌŚµÄĄė×ÓÓŠ”””””””””””” ””””£»
¢ŚŠ“³ö¼ÓČėNaOHČÜŅŗ¹ż³ĢÖŠ·¢ÉśµÄ·“Ó¦µÄĄė×Ó·½³ĢŹ½
””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
¢ŪĘäÖŠŃōĄė×ÓĪļÖŹµÄĮæ·Ö±šĪŖ”””””””” ””””””””””””””””””””””””””””””
27£®(11·Ö)ij»ÆѧŠĖȤŠ”×éĪŖĢ½Ė÷¹¤Ņµ·ĻĮĻµÄŌŁĄūÓĆ£¬ŌŚŹµŃéŹŅÖŠÓĆŗ¬ÓŠĀĮ”¢Ģś”¢ĶµÄŗĻ½šÖĘČ”ĀČ»ÆĀĮČÜŅŗ”¢ĀĢ·Æ¾§Ģå(FeSO4”¤7H2O)ŗĶµØ·Æ¾§Ģ唣Ę䏵Ńé·½°øČēĻĀ£ŗ
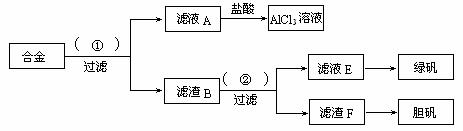
”” (1)Ėł¼ÓŹŌ¼Į¢Ł”¢¢Ś·Ö±šŹĒ”””””””””””””””””””””””””””””””””””””””””” ”£
”” (2)“ÓĀĖŅŗEÖŠµĆµ½ĀĢ·Æ¾§ĢåµÄŹµŃé²Ł×÷ŹĒ£ŗŌŚøō¾ųæÕĘųµÄĢõ¼žĻĀ£¬”””””””””””””” £»“ÓĀĖŌüFÖĘČ”µØ·ÆµÄµŚŅ»²½²Ł×÷×īŗĆ²ÉÓĆ”””””””””””””””””””””””””””””” ”£
”” (3)ÉĻŹöŹµŃé·½°øÖŠ£¬ÓŠŅ»²½Éč¼ĘĆ÷ĻŌ²»ŗĻĄķ£¬ĒėÄćÓčŅŌÖø³ö£¬²¢ĖµĆ÷ĄķÓÉ”””””””””””” ”£
ÄćČĻĪŖÕżČ·µÄÉč¼Ę·½°øŹĒ””””””””””””””””””””””””””””””””””””””””””””””””””””””””
”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
26£®(15·Ö)W”¢X”¢Y”¢ZŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄĶ¬Ņ»¶ĢÖÜĘŚŌŖĖŲ£¬WŹĒ½šŹōŌŖĖŲ£¬XŹĒµŲæĒÖŠŗ¬Įæ×ī¶ąµÄ½šŹōŌŖĖŲ£¬ĒŅw”¢xµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĻą»„·“Ӧɜ³ÉŃĪŗĶĖ®£»Y”¢ZŹĒ·Ē½šŹōŌŖĖŲ£¬YÓėWæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļW2Y£»GŌŚYµÄĒ°Ņ»ÖÜĘŚ£¬ĘäŌ×Ó×īĶā²ć±ČYŌ×Ó×īĶā²ćÉŁŅ»øöµē×Ó”£””
”” (1)XµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ”””””””””””””” ”£
”” (2)W”¢XµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĻą»„·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ”””””””””””””””””””””” ”£
”” (3)¹¤ŅµÉĻÖĘČ”Xµ„ÖŹµÄ»Æѧ·½³ĢŹ½ĪŖ”””””””””””””””” ”£
”” (4)GµÄĘųĢ¬Ēā»ÆĪļÓėYµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļĒ”ŗĆ·“Ӧɜ³ÉµÄÕżŃĪµÄ»Æѧ·½³ĢŹ½ĪŖ”””””””””””””””””” ”””£ŌŚ“߻ƼĮ×÷ÓĆĻĀ£¬Ęū³µĪ²ĘųÖŠGµÄŃõ»ÆĪļGOÓėŅ»Ńõ»ÆĢ¼Į½ÖÖĘųĢåÄÜĻą»„·“Ó¦×Ŗ»ÆĪŖĪŽĪŪČ¾”¢ÄܲĪÓė“óĘųŃ»·µÄĮ½ÖÖĘųĢ壬Š“³öÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½”””””””” £»ČōÓŠ33.6 L(ŅŃ»»Ėć³É±ź×¼×“æö)Ņ»Ńõ»ÆĢ¼²Ī¼Ó·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ”””” ”””””””””£
”” (5)298KŹ±£¬ZµÄ×īøß¼ŪŃõ»ÆĪļĪŖĪŽÉ«ŅŗĢ壬0.25 moløĆĪļÖŹÓėŅ»¶ØĮæĖ®»ģŗĻµĆµ½ZµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĻ”ČÜŅŗ£¬²¢·Å³öa kJµÄČČĮ攣øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ
”””””””” ””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
”” (6)Ėµ³öZµ„ÖŹµÄŅ»ÖÖÓĆĶ¾______”””””””””””””””””” ___
25£® Éč¼ĘĻĀĮŠŹµŃé·½°ø¼ų±šNa2CO3ŗĶNaHCO3Į½ÖÖ°×É«·ŪÄ©£¬
Éč¼ĘĻĀĮŠŹµŃé·½°ø¼ų±šNa2CO3ŗĶNaHCO3Į½ÖÖ°×É«·ŪÄ©£¬
²»ÄÜ“ļµ½Ō¤ĘŚÄæµÄµÄŹĒ”””””””””””””””””””””” (”””” )
”””””””” A£®·Ö±šĻņµČĮæµÄ°×É«·ŪÄ©ÖŠ¼ÓµČĢå»ż”¢µČÅØ¶ČµÄĻ”ŃĪĖį£¬
±Č½ĻÉś³ÉĘųĢåµÄæģĀż ”””” B£®·Ö±šĻņµČĮæµÄ°×É«·ŪÄ©ÖŠ¼ÓµČĢå»żŹŹĮæµÄĖ®£¬±Č½Ļ¹ĢĢå
ČܽāĮæµÄ¶ąÉŁ ”””” C£®·Ö±š½«µČĮæµÄ°×É«·ŪÄ©Åä³ÉČÜŅŗ£¬Č»ŗó¼ÓČė³ĪĒåŹÆ»ŅĖ®£¬±Č½ĻŹĒ·ńÓŠ³ĮµķÉś³É ”””” D£®·Ö±š½«µČĮæµÄ°×É«·ŪÄ©ÓĆÓŅĶ¼×°ÖĆ½ųŠŠŹµŃ飬±Č½Ļ³ĪĒåŹÆ»ŅĖ®ŹĒ·ń±ä»ģ×Ē
µŚ¢ņ¾ķ(·ĒŃ”ŌńĢā£¬¹²50·Ö)
24£®Ļņŗ¬ÓŠ0£®078molFeCl2µÄČÜŅŗÖŠĶØČė0£®009molCl2£¬ŌŁĻņĘäÖŠ¼ÓČėŗ¬0£®01molX2O72-µÄĖįŠŌČÜŅŗ£¬Ź¹ČÜŅŗÖŠµÄFe2+Ē”ŗĆĶźČ«±»Ńõ»Æ£¬ĒŅX2O72-±»»¹ŌĪŖXn+£¬ŌņnÖµĪŖ(”””” )
A£®2”””””””””” ”””””” B£®3 ”””””””””””””” C£®4”””””””””””” ”””””” D£®5
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com