
22.(8分)
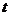 ℃时,将2 mol A气体和l mol B气体充人体积为2 L的恒温恒容密闭容器中,发生如下反应:
℃时,将2 mol A气体和l mol B气体充人体积为2 L的恒温恒容密闭容器中,发生如下反应: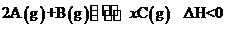 ,在2 min时反应达到平衡状态,此时容器中剩余0.6 mol B,并测得C的浓度为0.6 mol·L-1。计算:
,在2 min时反应达到平衡状态,此时容器中剩余0.6 mol B,并测得C的浓度为0.6 mol·L-1。计算:
(1)从反应开始至平衡时,A的平均反应速率。
(2)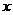 的值及
的值及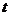 ℃时,上述反应的平衡常数K。
℃时,上述反应的平衡常数K。

21.(9分)
2009年“六·五”世界环境日,中国主题是“减少污染--行动起来”,这向世界传达了建设环境友好型社会的理念。
已知反应:
①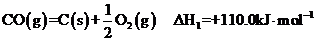
②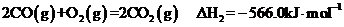
请回答下列问题:
(1)反应①的熵变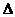 S
(填“>”或“<”)0。
S
(填“>”或“<”)0。
(2)有人建议,汽车尾气中的CO可用催化加热分解的方法来消除(反应①),这一方案在理论上是否可行? (填“可行”或“不可行”)。
(3)反应②中的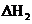 是不是CO的燃烧热?
(填“是”或“不是”)。
是不是CO的燃烧热?
(填“是”或“不是”)。
(4)煤炭的充分燃烧也是建设环境友好型社会的一个重要方面,12 g C(s)完全燃烧生成CO2(g)时,放出的热量为 kJ(依据反应①、②计算)。
20.(8分)
今有下列四种碱溶液:①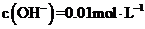 的KOH溶液;②
的KOH溶液;②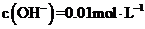 的Ba(OH)2溶液;③
的Ba(OH)2溶液;③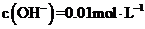 的氨水;④
的氨水;④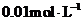 的氨水。
的氨水。
(1)溶质物质的量浓度最大的是 (填序号,下同)。
(2)溶液pH最小的是 。
(3)等体积的四种溶液分别加入盐酸,当恰好中和时,消耗盐酸的物质的量的关系是
(用“>”、“<”或“=”把①、②、③、④连接,下同),等体积的四种溶液中阴、阳离子总的物质的量的关系是 。
19.(9分)
 一定条件下,在l L密闭容器中C12(g)、S(g)发生反应(产物只有一种),三种物质的物质的量随时间变化的曲线如图所示,请回答下列问题:
一定条件下,在l L密闭容器中C12(g)、S(g)发生反应(产物只有一种),三种物质的物质的量随时间变化的曲线如图所示,请回答下列问题:
(1)生成物的化学式为 。
(2)反应进行2 min时达到平衡,此时Cl2的平均反应速率v(Cl2)= 。
(3)反应达到平衡时,S(g)的转化率为 。
18.(10分)
为了测定食醋(含3%-5%的CH3COOH,其他有机酸忽略不计)中醋酸的浓度,某校化学兴趣小组的同学设计了如下实验:
(1)实验步骤
①配制0.10 mol·L-1的NaOH溶液1 L;
②取5 mL食醋稀释至50 mL;
③取稀释后的食醋10 mL放入锥形瓶中,滴入2-3滴酚酞指示剂;
④用NaOH标准溶液进行滴定;
⑤再重复滴定两次,数据记录如下表:
|
滴定次数 实验数据 |
1 |
2 |
3 |
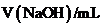 (起始读数) (起始读数) |
0.10 |
0.40 |
0 |
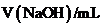 (终点读数) (终点读数) |
7.62 |
7.90 |
7.48 |
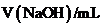 (消耗 (消耗 |
7.52 |
7.50 |
7.48 |

(2)实验分析
请你参与上述实验,并回答下列问题:
①如图,NaOH标准溶液不能盛放在 (填“A”或“B”)中,其原因是
(用离子方程式表示)。
②当滴入最后一滴NaOH溶液时,锥形瓶内溶液的颜色由 色变
为 色,且半分钟内不褪色,说明已达到滴定终点。
③根据步骤⑤中的数据,可求得食醋中醋酸的物质的量浓度为 mol·L-1.
④如果锥形瓶用水洗净后,再用待测液润洗,则所测食醋的浓度将 (填“偏高”、“偏低”或“无影响”)。
(3)问题探究
如果用同样的方法测定红醋中醋酸的浓度,为便于观察,首先得对红醋进行脱色处理,你认为应选用下列物质中的 (填字母)。
A.SO2 B.Cl2 C.活性炭 D.KMnO4
17.(8分)
某化学兴趣小组对镁与盐酸的反应进行实验探究,实验数据如下:
|
实验编号 |
镁的质量 |
镁的规格 |
盐酸的体积 |
盐酸的浓度 |
 |
|
① |
24g |
镁条 |
500mL |
6mol·L-1 |
|
|
② |
24g |
24g镁条 剪成100段 |
500mL |
6mol·L-1 |
|
|
③ |
24g |
镁粉 |
500mL |
6mol·L-1 |
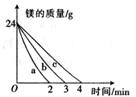
(1)该实验中影响镁与盐酸反应速率的因素是 。
(2)曲线c是由实验 (填序号)得到的数据。
(3)反应进行1 min时,生成氢气最多的是实验 (填序号)。
(4)若要求实验①的反应速率与实验②的反应速率相同(使用的药品不变),可采取的措施是
。
16.已知:①
②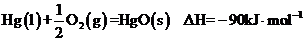
则反应: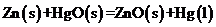 的
的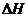 等于
等于
A.-260 kJ B.-440 kJ·mol-1
C.-440 kJ D.-260 kJ·mol-1
第Ⅱ卷 (非选择题 共52分)
15.一定条件下,某金属M与CO2发生反应:
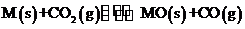 .该反应在不
.该反应在不
|
温度 |
700℃ |
900℃ |
|
K |
1 |
2 |
同温度下的平衡常数K见右表,下列叙述中正确的是
A.该反应是放热反应
B.增大压强可以提高M的转化率
C.通入足量的CO2,M可以完全转化为MO
D.700℃时,平衡体系中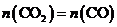
14.在密闭容器中进行如下反应: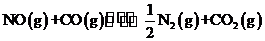 ,在不同温度下反应达到平衡时,NO的转化率如图所示,下列说法中正确的是
,在不同温度下反应达到平衡时,NO的转化率如图所示,下列说法中正确的是
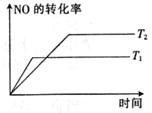 A.T1>T2,正反应是放热反应
A.T1>T2,正反应是放热反应
B.T1>T2,正反应是吸热反应
C.T1<T2,正反应是放热反应
D.T1<T2,正反应是吸热反应
13.在2 L恒容密闭容器中发生反应:2A(g)+B(g) 2C(g),若最初加入的A和B都是
2C(g),若最初加入的A和B都是
4 mol,10 s后反应达到平衡,此时间段A的平均反应速率是0.12 mol·L-1·s-1,则平衡后,容器中B的物质的量浓度为
A.2.8 mol·L-1 B.1.4 mol·L-1
C.3.2 mol·L-1 D.3.6 mol·L-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com