
1.[2008珠海一模]已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:1。
请回答:
(1) 组成A分子的原子的核外电子排布式是 ;
(2) B和C的分子式分别是 和 ;C分子的立体结构呈 形,该分子属于 分子(填“极性”或“非极性”);
(3) 向D的稀溶液中加入少量氯化铁溶液现象是 ,该反应的化学方程式为
(4) 若将1molE在氧气中完全燃烧,只生成1molCO2和2molH2O,则E的分子式是 。
|
(3)有无色气体产生 2H2O2===2H2O+O2↑ (4)CH4O。
2 [2008茂名一模]Al和Si、Ge和As在元素周期表金属和非金属过渡位置上,在其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。请回答下列问题:
(1) As 的价层电子构型为
(2) AlCl3是化工生产中的常用催化剂,熔点为192.6℃,熔融状态以二聚体A12C16形式存在,其中铝原子与氯原子的成键类型是
(3)超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,AlN晶体与金刚石类似,每个Al原子与个N原子相连,与同一个Al原子相连的N原子构成的空间构型为。在四大晶体类型中,AlN属于 晶体。
(4)Si和C 同主族,Si、C和0成键情况如下:
在C和0之间可以形成双键形成CO2分子,而Si和O则不能和碳那样形成有限分子原因是
(5)SiCl4(l)常用作烟雾剂,原因Si存在3d轨道,能同H20 (l)配位而剧烈水解,在潮湿的空气中发烟,试用化学方程式表示其原理
(l) 4s24p3( l 分) (2)共价键(或σ键) (l分)
(3) 4 (l分)正四面体(l分)原子(2分) (4) Si一0大于C一0的键,C=0的键能大于Si=O的键能,所以Si和O成单键,而C和O以双键形成稳定分子( 2 分)
(5)SiCl4(l) + 3H2O (l) = H2Si03 (s) + 4HCl(aq) ( 2 分)
选修有机化学5
3.元素电离能和元素电负性
第一电离能:气态电中性基态原子失去1个电子,转化为气态基态正离子所需要的能量叫做第一电离能。常用符号I1表示,单位为kJ/mol。
(1).原子核外电子排布的周期性.
随着原子序数的增加,元素原子的外围电子排布呈现周期性的变化:每隔一定数目的元素,元素原子的外围电子排布重复出现从ns1到ns2np6的周期性变化.
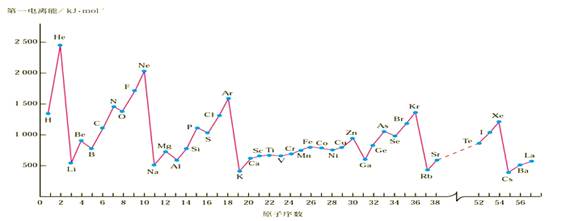
(2).元素第一电离能的周期性变化.
随着原子序数的递增,元素的第一电离能呈周期性变化:
★同周期从左到右,第一电离能有逐渐增大的趋势,稀有气体的第一电离能最大,碱金属的第一电离能最小;
★同主族从上到下,第一电离能有逐渐减小的趋势.
说明:
①同周期元素,从左往右第一电离能呈增大趋势。电子亚层结构为全满、半满时较相邻元素要大即第 ⅡA 族、第 ⅤA 族元素的第一电离能分别大于同周期相邻元素。Be、N、Mg、P
②.元素第一电离能的运用:
a.电离能是原子核外电子分层排布的实验验证.
b.用来比较元素的金属性的强弱. I1越小,金属性越强,表征原子失电子能力强弱.
(3).元素电负性的周期性变化.
元素的电负性:元素的原子在分子中吸引电子对的能力叫做该元素的电负性。
随着原子序数的递增,元素的电负性呈周期性变化:同周期从左到右,主族元素电负性逐渐增大;同一主族从上到下,元素电负性呈现减小的趋势.
电负性的运用:
a.确定元素类型(一般>1.8,非金属元素;<1.8,金属元素).
b.确定化学键类型(两元素电负性差值>1.7,离子键;<1.7,共价键).
c.判断元素价态正负(电负性大的为负价,小的为正价).
d.电负性是判断金属性和非金属性强弱的重要参数(表征原子得电子能力强弱).
例8.下列各组元素,按原子半径依次减小,元素第一电离能逐渐升高的顺序排列的是
A.K、Na、Li B.N、O、C C.Cl、S、P D.Al、Mg、Na
例9.已知X、Y元素同周期,且电负性X>Y,下列说法错误的是
A.X与Y形成化合物时,X显负价,Y显正价
B.第一电离能可能Y小于X
C.最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性
D.气态氢化物的稳定性:HmY小于HmX
例10.气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
|
元素 |
I1/eV |
I2/eV |
I3/eV |
|
甲 |
5.7 |
47.4 |
71.8 |
|
乙 |
7.7 |
15.1 |
80.3 |
|
丙 |
13.0 |
23.9 |
40.0 |
|
丁 |
15.7 |
27.6 |
40.7 |
下列说法正确的是
A.甲的金属性比乙强 B.乙的化合价为+1价
C.丙一定为非金属元素 D.丁一定是金属元素
例11.在下面的电子结构中,第一电离能最小的原子可能是
A.ns2np3 B.ns2np5 C.ns2np4 D.ns2np6
例12.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.下图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
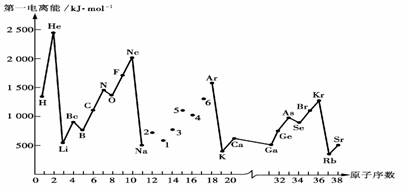
请回答以下问题:
(1).认真分析上图中同周期元素第一电离能的变化规律,将Na--Ar之间六种元素用短线连接起来,构成完整的图像.
(2).从上图分析可知,同一主族元素原子的第一电离能I1变化规律是______________;
(3).上图中5号元素在周期表中的位置是________________________________________;
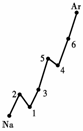 (4).上图中4、5、6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是:__________________________________.
(4).上图中4、5、6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是:__________________________________.
例12.(1).见上图(右) (2).从上到下依次减小
(3).第三周期,ⅤA族
(4).因同主族上一周期的元素的氢化物分子间存在氢键
例13.1932年美国化学家鲍林首先提出了电负性的概念.电负性(用X表示)也是元素的一种重要性质,若 x 越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的 x 值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x 值 |
0.98 |
1.57 |
2.04 |
2.55 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
⑴.通过分析 x 值变化规律,确定N、Mg的 x 值范围:
<x (N)< , <x (Mg)< .
⑵.推测x值与原子半径的关系是 ;根据短周期元素的x值变化特点,体现了元素性质的 变化规律.
⑶.某有机化合物结构中含S-N键,其共用电子对偏向 (写原子名称).
⑷.经验规律告诉我们:当成键的两原子相应元素的 x 差值△x>1.7时,一般为离子键,当△ x<1.7时,一般为共价键.试推断AlBr3中化学键类型是 .
⑸.预测周期表中, x 值最小的元素位于 周期 族.(放射性元素除外)
例13.(1).2.55 3.44 0.93 1.57
(2).电负性随原子半径减小而增大,周期性
(3).氮 (4).共价键 (5).6,IA
『综合模拟训练』
2.(构造原理)
了解多电子原子中核外电子分层排布遵循的原理,能用电子排布式表示1-36号元素原子核外电子的排布.
(1).原子核外电子的运动特征可以用电子层、原子轨道(亚层)和自旋方向来进行描述.在含有多个核外电子的原子中,不存在运动状态完全相同的两个电子.
(2).原子核外电子排布原理.
①.能量最低原理:电子先占据能量低的轨道,再依次进入能量高的轨道.
②.泡利不相容原理:每个轨道最多容纳两个自旋状态不同的电子.
③.洪特规则:在能量相同的轨道上排布时,电子尽可能分占不同的轨道,且自旋状态相同.
洪特规则的特例:在等价轨道的全充满(p6、d10、f14)、半充满(p3、d5、f7)、全空时(p0、d0、f0)的状态,具有较低的能量和较大的稳定性.如24Cr [Ar]3d54s1、29Cu [Ar]3d104s1.
(3).掌握能级交错图和1-36号元素的核外电子排布式.
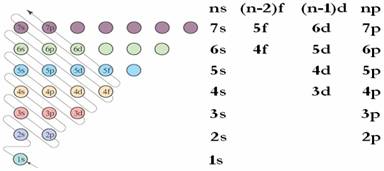
①根据构造原理,基态原子核外电子的排布遵循图⑴箭头所示的顺序。
②根据构造原理,可以将各能级按能量的差异分成能级组如图⑵所示,由下而上表示七个能级组,其能量依次升高;在同一能级组内,从左到右能量依次升高。基态原子核外电子的排布按能量由低到高的顺序依次排布。
例3.表示一个原子在第三电子层上有10个电子可以写成
A.310 B.3d10 C.3s23p63d2 D. 3s23p64s2
例4.下列电子排布中,原子处于激发状态的是
A.1s22s22p5 B. 1s22s22p43s2
C. 1s22s22p63s23p63d44s2 D. 1s22s22p63s23p63d34s2
例5.下列关于价电子构型为3s23p4的粒子描述正确的是
A.它的元素符号为O
B.它的核外电子排布式为1s22s22p63s23p4
C.它可与H2生成液态化合物
 D.其电子排布图为:
D.其电子排布图为:
1s 2s 2p 3s 3p
例6.按所示格式填写下表有序号的表格:
|
原子序数 |
电子排布式 |
价层电子排布 |
周期 |
族 |
|
17 |
① |
② |
③ |
④ |
|
⑤ |
1s22s22p6 |
⑥ |
⑦ |
⑧ |
|
⑨ |
⑩ |
3d54s1 |
⑾ |
ⅥB |
例6.①.1s22s22p63s23p5 ②.3s23p5 ③.3 ④.ⅦA ⑤.10 ⑥.2s22p6
⑦.2 ⑧.0 ⑨.24 ⑩.1s22s22p63s23p63d54s1 ⑾.4
例7.(1).砷原子的最外层电子排布式是4s24p3,在元素周期表中,砷元素位于__________
周期 族;最高价氧化物的化学式为 ,砷酸钠的化学式是 .
(2).已知下列元素在周期表中的位置,写出它们最外层电子构型和元素符号:
①.第4周期ⅣB族 ;
②.第5周期ⅦA族 .
例7.(1).4 ⅤA As2O5 Na3AsO4
(2).①.3d24s2 Ti ②.5S25p5 I
1.电子云:用小黑点的疏密来描述电子在原子核外空间出现的机会大小所得的图形叫电子云图.离核越近,电子出现的机会大,电子云密度越大;离核越远,电子出现的机会小,电子云密度越小.
电子层(能层):根据电子的能量差异和主要运动区域的不同,核外电子分别处于不同的电子层.原子由里向外对应的电子层符号分别为K、L、M、N、O、P、Q.
原子轨道(能级即亚层):处于同一电子层的原子核外电子,也可以在不同类型的原子轨道上运动,分别用s、p、d、f表示不同形状的轨道,s轨道呈球形、p轨道呈纺锤形,d轨道和f轨道较复杂.各轨道的伸展方向个数依次为1、3、5、7.
例1.下列关于氢原子电子云图的说法正确的是
A.通常用小黑点来表示电子的多少,黑点密度大,电子数目大
B.黑点密度大,单位体积内电子出现的机会大
C.通常用小黑点来表示电子绕核作高速圆周运动
D.电子云图是对运动无规律性的描述
例2.下列有关认识正确的是
A.各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7
B.各能层的能级都是从s能级开始至f能级结束
C.各能层含有的能级数为n -1
D.各能层含有的电子数为2n2
2.0mol·L-1NaOH溶液中,充分反应。NaOH
溶液的体积V≥
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将 (填“偏高”或“偏低”)
[探究二] 实验方案:铝镁合金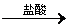 测定生成气体的体积
测定生成气体的体积
实验装置如右图,问题讨论:
(3)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥、除酸雾的装置。你的意见是: (填“需要”或“不需要”)。
(4)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
①
②
29.(13分)铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
[探究一] 实验方案:铝镁合金  测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是
 实验步骤:
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL
28.(11分)有一澄清透明的溶液,可能有NH4+、Fe3+、H+、Mg2+、Al3+、I-、CO32-等离子,现分别取溶液进行下列实验:
(1)加入浓溴水,溶液变为褐色;
(2)加入淀粉,未见蓝色;
(3)在逐滴加入1mol·L-1NaOH溶液的过程中,
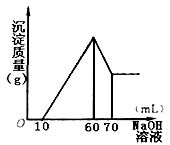 未闻到刺激性气体,随NaOH溶液的滴入,
未闻到刺激性气体,随NaOH溶液的滴入,
产生沉淀的量如图所示,试确定:
①溶液中一定存在的离子有 ;
②写出加入NaOH溶液过程中发生的反应的离子方程式
③其中阳离子物质的量分别为
27.(11分)某化学兴趣小组为探索工业废料的再利用,在实验室中用含有铝、铁、铜的合金制取氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体。其实验方案如下:

(1)所加试剂①、②分别是 。
(2)从滤液E中得到绿矾晶体的实验操作是:在隔绝空气的条件下, ;从滤渣F制取胆矾的第一步操作最好采用 。
(3)上述实验方案中,有一步设计明显不合理,请你予以指出,并说明理由 。
你认为正确的设计方案是
。
26.(15分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W是金属元素,X是地壳中含量最多的金属元素,且w、x的最高价氧化物的水化物相互反应生成盐和水;Y、Z是非金属元素,Y与W可形成离子化合物W2Y;G在Y的前一周期,其原子最外层比Y原子最外层少一个电子。
(1)X的原子结构示意图为 。
(2)W、X的最高价氧化物的水化物相互反应的离子方程式为 。
(3)工业上制取X单质的化学方程式为 。
(4)G的气态氢化物与Y的最高价氧化物的水化物恰好反应生成的正盐的化学方程式为 。在催化剂作用下,汽车尾气中G的氧化物GO与一氧化碳两种气体能相互反应转化为无污染、能参与大气循环的两种气体,写出有关反应的化学方程式 ;若有33.6 L(已换算成标准状况)一氧化碳参加反应,转移的电子数为 。
(5)298K时,Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到Z的最高价氧化物的水化物的稀溶液,并放出a kJ的热量。该反应的热化学方程式为
(6)说出Z单质的一种用途______ ___
25. 设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,
设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,
不能达到预期目的的是 ( )
A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,
比较生成气体的快慢 B.分别向等量的白色粉末中加等体积适量的水,比较固体
溶解量的多少 C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成 D.分别将等量的白色粉末用右图装置进行实验,比较澄清石灰水是否变混浊
第Ⅱ卷(非选择题,共50分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com