
25. -Hello, Grand Hotel.
-I’d like a room with a bath. How much do you______?
A. ask B. charge C. afford D. pay
24. It is the hotel _______is located in the downtown _______he applied to for a job.
A. that ; where B. which ; that C. / ; that D. what ; that
23. To the great _______of the citizens, no one else was infected with H1N1 except the 12 confirmed cases at that time.
A. relaxation B. disappointment C. relief D. surprise
22. The speech which he made ______ the project bothered me greatly.
A. being concerned B. be concerned C. concerned D. concerning
第一节:单项填空(共15小题,每小题1分,满分15分)
21. It’s really _______type I’ve been after, but I’d like to give it _______second thought.
A. a; 不填 B. a; the C. the; a D. the; the
34.将N2和H2按一定比例混合,其密度是相同状况下H2的3.6倍,取出0.5mol该混合气体充入密闭容器里,发生反应N2(g)+3H2(g) 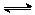 2NH3(g)
△H<0,在一定条件下达到平衡。已知反应达到平衡后容器内压强是相同条件下反应前的0.8倍。试求:
2NH3(g)
△H<0,在一定条件下达到平衡。已知反应达到平衡后容器内压强是相同条件下反应前的0.8倍。试求:
(1)写出此反应的化学平衡常数表达式;
(2)达到平衡时混合气体中氨的物质的量;
(3)平衡时N2的转化率。
2009-2010年度哈师大附中高三第三次月考
33.有A、B、C、D、E、F六种短周期元素,原子序数依次增大,其中A、D元素的原子最外层电子均只有一个电子,且A和D可形成离子化合物;C、F同主族,B元素位于元素周期表中第二周期,且原子最外层电子数占核外电子总数的3/4;F元素原子最外电子层比同周期的E元素原子的最外层多4个电子,请回答:
(1)写出A、D两种元素组成的化合物的电子式 ;
(2)写出B、D、E三种元素组成的常见化合物的名称 ;
(3)工业生产E的化学方程式为 ;
(4)元素F位于元素周期表第 周期,第 族。
(5)D、F两元素最高价氧化物的水化物之间发生的反应的化学方程式
(6)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为
。
32.在一定条件下,在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
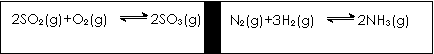
(1)若起始时两边分别投入2 mol SO2、1 mol O2;1 mol N2、3 mol H2,达到平衡后,隔板是否能处于中央 (填“能”或“否”)。
(2)若起始时投入2 mol SO2、1 mol O2;1 mol N2、2 mol H2,达到平衡后,隔板仍处于中央,则SO2的转化率和N2的转化率之比为 (填数字);
(3)若起始时投入2 mol SO2、1 mol O2;1 mol N2、a mol H2、0.1 mol NH3,起始时右侧体积小于左侧体积,当a值在一定范围内变化时,均可通过调节反应器温度,使左右两侧反应都达到平衡,且平衡时隔板处于中央,此时SO2的转化率与N2的转化率之比为5:1,求a的取值范围 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com