
9.下列离子方程式正确的是
A.100mL0.1mol·L-1的Na2CO3溶液中逐滴加入含0.01molCH3COOH醋酸溶液:
CO32-+ 2CH3COOH ====CO2↑+ 2CH3COO-+ H2O
B.硫酸氢铵溶液加入足量氢氧化钡溶液:
2NH4++Ba2++SO42-+2OH-====BaSO4↓+2 NH3·H2O
C.150mL 0.1mol·L-1 NaOH缓慢通入标准状况下的CO2气体224 mL:
3OH-+2CO2====HCO3-+CO32-+H2O
D.FeSO4酸性溶液中加入H2O2: Fe2++H2O2+2H+====Fe3++2H2O
8.在常温下四个容积相同的抽空的密闭容器内,分别注入下列各组气体(先注入一种,再注入另一种),全部气体注入完毕后,容器中的压强从大到小的顺序是
①2mol二氧化硫和1mol氧气 ②2mol硫化氢和1mol二氧化硫
③2mol硫化氢和1mol氯气 ④2mol氨和lmol氯化氢
A.③>④>①>② B.①>②=③>④
C.①=③>④>② D.①=②=③>④
7.甲、乙两烧杯分别盛有等体积、等物质的量浓度的稀盐酸、稀氢氧化钠,分别在甲、乙两烧杯中各加入等质量的金属钠和铝,充分反应后下列情况不可能出现的是
A.甲、乙两烧杯中产生的氢气的质量比为23:9
B.若反应后甲、乙两烧杯中皆无金属剩余,甲、乙两烧杯产生的氢气的质量相等
C.若反应后有一个烧杯中有金属剩余,甲、乙两烧杯产生的氢气的乙的多
D.若反应后有一个烧杯中有金属剩余,甲、乙两烧杯产生的氢气的质量相等
6.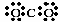 下列各项中表达正确的是
下列各项中表达正确的是
 A.次氯酸的结构式:H—Cl—O
B.二氧化碳的电子式:
A.次氯酸的结构式:H—Cl—O
B.二氧化碳的电子式:
C.8个中子的碳原子的核素符号:12C D.K原子的结构示意图为:
5.化学与生产、生活、社会密切相关,下列说法正确的是
A.氯气可用作消毒剂和漂白剂,是因为氯气具有强氧化性
B.工业上用石灰石、纯碱和石英在高温条件下制得玻璃的原理与碳酸、硅酸的酸性强弱有关
C.神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料。
D.硫酸工业中,应把从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中
4.设阿伏加德常数为NA,下列叙述正确的是
A.过量的锌粒与一定量的浓硫酸反应,若浓硫酸的还原产物仅为SO2,则每生成1mol气体,电子转移数一定是2NA
B.标准状况下,22.4 L氦气含有原子数为2NA
C.由H2O、D2O混合组成的物质0.1mol 中含有电子数不是NA
D.常温下,28.6gNa2CO3·10H2O在晶体或在溶液中,含有的CO32-数均小于0.1NA
3.符合下列条件且一定能大量共存的离子组是
A.由水电离出的c(H+)×c(OH-)=10-24溶液中,CH3COO-、NO3-、Na+、Ca2+
B.能使PH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.能使溴水褪色,加入NH4HCO3固体产生刺激性气味气体:S2-、ClO-、OH-、K+
D.加入过量NaOH或过量稀H2SO4时都能产生白色沉淀:Ba2+、Mg2+、Cl-、HCO3-
2.下列叙述正确的是
A.氯化钠熔融电离成钠离子和氯离子这一过程是化学变化
B.含有离子的晶体不一定是离子晶体
C.正四面体结构的物质其化学键的夹角均为109°28′
D.只含一种元素的物质是单质
1.治理太湖蓝藻污染是我国目前重要的环保工程,据测算,每年流入太湖的磷约为400吨,下列措施中不能有效缓解此类水体污染的是
A.减少生活污水和工业废水的排放
B.利用污水中几乎所有的无机磷都以磷酸盐存在,可投加石灰或铝盐、铁盐形成难溶性的磷酸盐沉淀治理
C.投放大量喜欢吃蓝藻的鱼类
D.减少氟利昂的使用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com