
28.101kPa时,1mol纯物质完全燃烧生成 时所放出的热量,叫做该物质的燃烧热,单位 。
27. 盖斯定律:化学反应的反应热只与反应体系的 和 有关,而与反应的途径无关。
26. 在与外界隔离的体系中,自发过程将导致体系的熵 ,(填“增大”、“减小”、“不变”),这个原理也叫做 原理。对于同一种物质, 时熵值最大。
25. 已知反应2SO2(g)+O2(g)
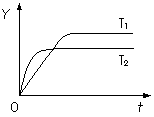
已知反应2SO2(g)+O2(g)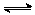 2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是
2SO3(g);ΔH<0,向某体积恒定的密闭容器中按体积比2∶1充入SO2和O2,在一定条件下发生反应。下图是某物理量(Y)随时间(t)变化的示意图(图中T表示温度),Y可以是
A.SO2的转化率
B.混合气体的密度
C.密闭容器内的压强
D.O2的体积分数
24. 可确认化学平衡发生移动的是
A.化学反应速率发生了改变
B.有气体物质参加的可逆反应达到平衡后,改变了压强
C.由于某一条件的改变,平衡混合物各组分的百分含量发生了改变
D.可逆反应达到平衡后,使用了催化剂
23.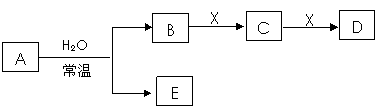 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是
A.若A是单质,B和D的反应是OH―+HCO3― = H2O+CO32―,则E一定能还原Fe2O3
B.若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
C.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
D.若D为CO,C能和E反应,则A一定是Na2O2www.
22. 在密闭容器中发生下列反应aA(g) 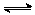 cC(g)+dD(g),反应达到平衡后,将容器体积压缩到原来的一半,再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将容器体积压缩到原来的一半,再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A.A的转化率变小
B.平衡向正反应方向移动
C.D的体积分数变大
D.a > c+d
21. “类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是A.IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;
则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3
B.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;
则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3
C.晶体中有阴离子,必有阳离子;则晶体中有阳离子,必有阴离子
D.干冰(CO2)是分子晶体,则SiO2也是分子晶体
20. 可逆反应A(g)+3B(g) 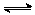 2C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是
2C(g)+2D(g)在不同条件下的反应速率如下,其中反应速率最快的是
A.v(A)=0.4mol/(L·s)
B.v(B)=0.6mol/(L·s)
C.v(C)=0.4mol/(L·s)
D.v(D)=0.45mol/(L·s)
19. 在原子的第n电子层中,当n为最外层时,最多容纳的电子数与(n-1)层相同;当n为次外层时,其最多容纳的电子数比(n-1)层最多容纳的电子数多10,则n层是
A.N层
B.M层
C.L层
D.K层
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com