
2.“先王之法,立天子不使诸侯疑焉,立诸侯不使大夫疑焉,立嫡子不使庶孽疑焉。疑生争,争生乱,是故诸侯失位则天下乱,大夫无等则朝堂乱。”这种继承制度在政治上给西周带来的最不利影响是
A.权力世袭制度渐渐消亡 B.使世卿世禄的贵族特权自行消灭
C.贵族普遍地转化成庶人 D.中央和地方的政治隶属关系失控
1.一人多姓。史书上说:“秦封(鞅)于商,故号商君。卫之诸庶孽公子也,人称卫鞅,姓公孙氏,其祖本姬姓也”。其中,商姓来源于
A.自然的崇拜 B.所在地方的地名
C.母亲的族姓 D.因功而得到的封地
16.下列物质能使干燥的蓝色石蕊试纸先变红又褪色的是( )
①氯气 ②液氯 ③新制氯水 ④氯气溶于无水酒精所形成的溶液 ⑤盐酸
⑥盐酸酸化的漂白粉溶液
A.③⑥ B.①②③⑥ C.①②③ D.③④⑥
第Ⅱ卷(共52分)
17(7分).据报道,某些花岗岩会产生氡(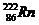 ),从而对人体产生伤害。请回答:[:]
),从而对人体产生伤害。请回答:[:]
(1)该原子的质量数是 ,质子数是 ,中子数是 。
(2)研究发现,镭能蜕变为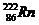 ,故称
,故称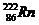 为镭射气;钍能蜕变为
为镭射气;钍能蜕变为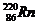 ,故将
,故将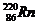 称为钍射气;锕能蜕变为
称为钍射气;锕能蜕变为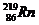 ,故将
,故将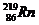 称为锕射气。
称为锕射气。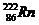 、
、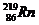 是( )
是( )
A.同种元素 B.同位素 C.同种核素 D.同种原子
由此可见, 决定元素种类,质子数和 决定核素种类。
 18(6分).(1)溴:通常状态下,溴是
色,密度比水(填“大”或“小”) ,溶于苯中呈 色。
18(6分).(1)溴:通常状态下,溴是
色,密度比水(填“大”或“小”) ,溶于苯中呈 色。
(2)碘:碘是
色的固体,
,即被加热时不经熔化就直接变成紫色蒸气,蒸气遇冷又重新 凝聚成固体。碘溶于四氯化碳中呈 色。
凝聚成固体。碘溶于四氯化碳中呈 色。
19(8分).某宇航员从太空某星球外层空间取回的气体样品分析如下:
①将样品溶于水,发现其主要成分气体A极易溶于水。
②将A的浓溶液与软锰矿(主要成分是MnO2)共热可产生一种黄绿色气体单质B,将B通入NaOH溶液中可生成两种盐。
③A的稀溶液与锌粒反应生成气体C,C与B的混合气体经光照发生爆炸又生成气体A,实验测得反应前后气体体积不变。
④将B通入KI溶液中,溶液变成棕黄色。
据此回答下列问题 :(1)气体B溶于NaOH溶液反应的化学方程式
:(1)气体B溶于NaOH溶液反应的化学方程式
(2)A的稀溶液与锌粒反应生成气体C的化学方程式
(3)C与B的混合气体经光照发生爆炸生成气体A的化学方程式
(4)B通入KI溶液中反应的化学方程式
 20(6分).如图为实验室用自来水制取蒸馏水的装置示意图,根据图示回答下列问题。
20(6分).如图为实验室用自来水制取蒸馏水的装置示意图,根据图示回答下列问题。
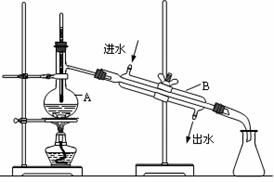
 ⑴图中的两处明显的错误是
⑴图中的两处明显的错误是
 __________________________
__________________________ _______
_______
 _____________________________。[:]
_____________________________。[:]
 ⑵ A仪器的名称是____________,
⑵ A仪器的名称是____________,
B仪器的名称是_______________。
 ⑶实验时A中除加入少量自来水外,还需
⑶实验时A中除加入少量自来水外,还需
加入少量__________________,其作用是
______________________________。

21(5分).下面是四种盐在不同温度下的溶解 度(g/100g H2O)
度(g/100g H2O)
|
温度 |
NaNO3 |
KNO3 |
NaCl |
KCl |
10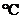 |
80.5 |
20.9[:ZXXK] |
35.7 |
31.0 |
100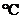 |
175 |
246 |
39.1 |
56.6 |
(假设:(1)盐类共存时不影响各自的溶解度。(2)分离晶体时,溶剂的损耗忽略不计。)
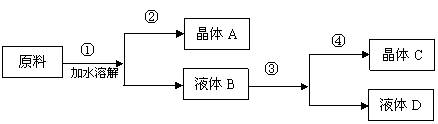 某同学设计用物质的量比为1:1的硝酸钠和氯化钾为原料,加入一定量的水制取硝酸钾晶体的实验,其流程如图:
某同学设计用物质的量比为1:1的硝酸钠和氯化钾为原料,加入一定量的水制取硝酸钾晶体的实验,其流程如图:
[:]
(1)在①和③的实验过程中,关键的实验条件是 。
(2)分离出晶体的②和④的操 作
作 是
(填“蒸发”、“结晶”、“过滤”中的某种操作)。硝酸钾晶体是
(填“A”或“C”)。
是
(填“蒸发”、“结晶”、“过滤”中的某种操作)。硝酸钾晶体是
(填“A”或“C”)。
(3)欲将粗产品提纯,可采取的方法是 。
 22(9分).实验室用氯化钠固体配制100mL 1.0 mol·L-1 的NaCl溶液,有如下操作步骤:
22(9分).实验室用氯化钠固体配制100mL 1.0 mol·L-1 的NaCl溶液,有如下操作步骤:
①用托盘天平称量____________g NaCl晶体放入小烧杯中,加适量蒸馏水溶解 ;
;
②继续向容量瓶中加蒸馏水至液面距刻度线1-2cm处,改用_____________小心滴加蒸馏水至溶液凹液面的最低处与刻度线相切;
③把①中所得溶液小心地转入______________中;
④将容量瓶塞紧,充分摇匀;
⑤用少量蒸馏水洗涤烧杯与玻璃棒2-3次,洗涤液一并转移到容量瓶中。
(1)将上述步骤的空白处填空;
(2)本实验操作步骤的正确顺序是(填序号,不能重复) ;
(3)试分析下列操作对所配得溶液的浓度有何影响(填:“偏高”、“偏低”、或“无影响”)
①容量瓶用蒸馏水洗净后没有干燥就直接用来配溶液,所配得溶液的浓度 ;
②定容时,俯视刻度线,所配得溶液的浓度 ;
③定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。所配得溶液的浓度 。
23(11分).实验室中所用少量氯气是用下列方法制取的,
试回答下列问题: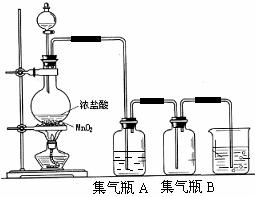
(1)该实验中制取氯气的反应是氧化还原反应吗?(填“是”或“否”) ,如果是氧化还原反应,请指出 是氧化剂, 是还原剂,并用双线桥标出电子转移的方向和数目:
(2)集气瓶A中盛装的是饱和食盐水(注:氯气在饱和食盐水中溶解度很小,而氯化氢在饱和食盐水中的溶解度则很大),其作用是 。
(3)氯气溶入水显酸性,且氯气有毒,并有剧烈的刺激性,若吸入大量氯气,可中毒死亡,所以氯气尾气直接排入大气中,会污染环境。实验室中可采用 溶液来吸收有毒的氯气。
(4)一次实验中,用浓盐酸80mL,其密度为1.19g·cm-3、HCl的质量分数为36.5%,跟MnO2恰好完全反应,产生了5.6L(标准状况下)的氯气。据此计算浓盐酸的物质的量浓度=
mol·L-1 , 被氧化的HCl的物质的量= mol
[:ZXXK]
南安一中2009-2010学年度第一学期期中考试
15.下列数量的物质中含原子个数最多的是( )
A.0.4摩尔O2 B.3.01×1022CO2分子
C.4℃时(水的密度为1g/mL)5.4毫升水 D.10g氖
14.在4℃时(水的密度为1g/mL)向100mL水中溶解了22.4L HCl气体(标准状态下测得)后形成的溶液。下 列说法中正确的是
( )
列说法中正确的是
( )
A.该溶液物质的量浓度因溶液的密度未知而无法求得
B.该溶液物质的量浓度为10mol·L-1
C.该溶液中溶质的质量分数因溶液的密度未知而无法求得
D.所得溶液的体积为22.5L
13. 4 ℃时(水的密度为1g/mL),若20滴水恰好为1 mL,那么1滴水中所含的水分子数约为(NA表示阿伏加德罗常数的值) ( )
A.20NA B.NA/360 C.9 NA/10 D.360/NA
12.将百分比浓度为a%,物质的量浓度为c1 mol·L-1的稀H2SO4 蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是( )C
蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是( )C
A.c2=c1 B.c2<c1 C.c2>2c1 D.无法确定
11.鉴别NaCl、NaBr 、NaI三种无色溶液,可选用的试剂是( )
①AgNO3 溶液、稀HNO3 ②淀粉KI溶液 ③碘水、淀粉溶液 ④氯水、CCl4
A.①③ B.①② C.①②③ D.①④
10.浓盐酸和Ca(ClO)2能发生如下反应:
Ca(ClO)2+4HCl(浓)== CaCl2+2Cl2↑+2H2O
用贮存很久的漂白粉与浓盐酸反应制得的Cl2中,可能含有的杂质气体是( )[:]
①CO2 ②HCl ③H2O(气) ④O2
A.①②③ B.②③④ C.②③ D.①④[:ZXXK]
9.方志敏烈士生前在狱中曾用米汤(内含淀粉)给鲁迅先生写信,鲁迅先生收到信后,为了看清信中的内容,可选用的化学试剂是( )
A.碘化钾 B碘酒 C溴水 D碘化钾淀粉溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com