
1、过氧化氢的沸点比水高,但受热易分解。某试剂厂先制得7%-8%得过氧化氢溶液,再蒸馏浓缩成3%溶液时,可采用的适宜方法是( )(只有一个正确选项)
A、常压蒸馏 B、减压蒸馏 C、加生石灰常压蒸馏 D、加压蒸馏
解析:本题考查学生对几种蒸馏原理的应用。生石灰的作用是吸收水。题目要求浓缩过氧化氢溶液且过氧化氢的沸点比水高,应通过蒸发水达浓缩之目的。故首先将C选项排除。比较余下的A、B、D三个选顼,不同之处只在于压强。由题目右知H2O2受热易分解,故必蒸馏时温度不要太高为好。减压蒸馏可在较低温度上蒸发去水分,故选B顼。
1、已知下列两个热化学 方程式:
方程式:
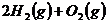 =
=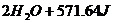
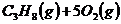 =
=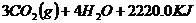
实验测得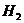 与
与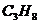 得混和气体共5摩,完全燃烧时放热3847KJ,则混和气体中
得混和气体共5摩,完全燃烧时放热3847KJ,则混和气体中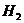 与
与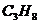 得体积比是( )
得体积比是( )
A、1:3 B、3:1 C、1:4 D、1:1
解析:因为3847<2* 2220.0,所以混和气体中
2220.0,所以混和气体中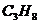 不可能超过2/5,这样A、C、D三个选项都可以排除,正确选项为B。通过简单计算,迅速排除不合理选项,正确选项轻易可得。
不可能超过2/5,这样A、C、D三个选项都可以排除,正确选项为B。通过简单计算,迅速排除不合理选项,正确选项轻易可得。
5、下列各组离子:⑴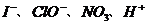 ⑵
⑵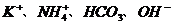 ⑶
⑶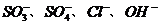 ⑷
⑷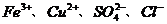 ⑸
⑸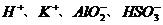 ⑹
⑹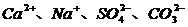 在水溶液中能大量共存的是( )
在水溶液中能大量共存的是( )
A、⑴和⑹ B、⑶和⑷ C、⑵和⑸ D、⑴和⑷
解析:判断离子是否共存,应从以下六个方面来进行分析:
看离子间是否生成难溶的物质。
看离子间是否生成气体或挥发性物质。
看离子间是否生成难电离的物质。(弱酸、弱碱、水)
看离子间是否发生氧化-还原反应(强氧化性的离子与较强还原性的离子不能共存)
看离子间在水溶液中能否发生双水解反应。如果有弱酸的阴离子和弱碱的阳离子,便不能大量共存。
看离子间能否发生络合反应,如果能生成复杂难电离的络劳资,便不能大量共存。
(1)中I- 、NO3- H+
 三者相遇会发生氧化-还原反应,生成I2,NO或NO2故不能共存,含(1)的选项都应排
三者相遇会发生氧化-还原反应,生成I2,NO或NO2故不能共存,含(1)的选项都应排 除,即排除A、D选项。再看(2)其中HCO3-、OH-不能共存,故含有(2)选项C也应排
除,即排除A、D选项。再看(2)其中HCO3-、OH-不能共存,故含有(2)选项C也应排 除,则B为正确答案。
除,则B为正确答案。
4.N2H4是一种高效清洁的火箭燃料。0.25mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5KJ热量。则下列热化学方程式中正确的是 ( )
A、1/2 N2H4(g)+1/2O2 (g) ===1/2 N2(g)+H2O(g);△H=+267KJ.mol_
B、N2H4(g)+O2 (g) === N2(g)+2H2O(l); △H=-133.5KJ.mol_
C、N2H4(g)+O2 (g) === N2(g)+2H2O(g); △H=+534KJ.mol_
D、N2H4(g)+O2 (g) === N2(g)+2H2O(g); △H=-534KJ.mol_
解析:因为放热反应,所以排除A、C;产物是气态水,所以排除B,只剩下D,因此D为正确答案。
3.在PH=1的溶液中,一定可以大量共存的离子组是( C )
A、Cl-、ALO2-、Na+ 、K+ B、SO42-、NO3-、Fe2+、Mg2+
C、 Na+、Fe3+、SO42-、Cl-
 D、NH4+、Ba2+、Cl-、HCO3-
D、NH4+、Ba2+、Cl-、HCO3-
解析:解题的关键是在每组中要多加一种H+进去考虑。排除ABD
2.下列除去杂质的方法正确的是 ( )
乙烷气体中混有少量乙烯:通入氢气,使乙烯发生加成反应
二氧化碳气体中混有少量二氧化硫:通入酸性高锰酸钾溶液后,收集气体
乙醇中混有少量乙酸:加入氢氧化钠溶液后,分液
氯化钠溶液中混有少量硫酸钠:加适量硝酸钡溶液,过滤。
解析:根据“除杂不加杂”的原则,在除杂质过程中,要尽量避免加入新的杂质。A引入了氢气,排除;C引入了乙酸钠和氢氧化钠,排除;D引入了硝酸根,排除;只剩下B为正确。
1、为了除去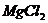 酸性溶液中的
酸性溶液中的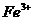 ,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸。这种试剂是( )
,可在加热搅拌的条件下加入一种试剂,过滤后再加入适量盐酸。这种试剂是( )
A、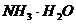 B、
B、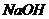 C、
C、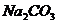 D、
D、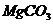
解析:根据“除杂不加杂”的原则,在除杂质过程中,要尽量避免加入新的杂质。A引入了NH4+排除;B引入了Na+排除;C引入了Na+排除;只剩下D。
13.(14分)如图所示,质量为M、倾角为θ的斜面体置于光滑的水平地面上,要使原来与斜面接触的质量为m的小球做自由落体运动,则向右拉斜面体的水平力F至少为多大?
解析:设小球距水平地面的高度为h,则距斜面下端的水平距离s=hcot θ
小球从h高处自由下落到水平地面所需的时间为:
 t=
t=
故斜面体从静止开始向右匀加速运动s位移所需的时间应为:
t′==≤t
即a≥gcot θ
又因为a=
可得:F≥Mgcot θ
即向右拉斜面体的水平力至少为Mgcot θ.
答案:Mgcot θ
12.(13分)如图所示,直升机沿水平方向匀速飞往水源取水灭火,悬挂着质量m=500 kg空箱的悬索与竖直方向的夹角θ1=45°.直升机取水后飞往火场,加速度沿水平方向,大小稳定在a=1.5 m/s2时,悬索与竖直方向的夹角θ2=14°.如果空气阻力大小不变,且忽略悬索的质量,试求水箱中水的质量M.(取g=10 m/s2,sin 14°≈0.242,cos 14°≈0.970)
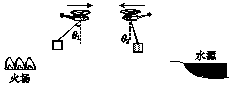 [2007年高考·江苏物理卷]
[2007年高考·江苏物理卷]
解析:直升机取水,水箱受力平衡,得:
水平方向:FT1sin θ1-Ff=0
竖直方向:FT1cos θ1-mg=0
可解得:Ff=mgtan θ1
直升机返回,由牛顿第二定律得:
水平方向:FT2sin θ2-Ff=(m+M)a
竖直方向:FT2cos θ2-(m+M)g=0
解得:水箱中水的质量M=4.5×103 kg.
答案:4.5×103 kg
11.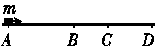 (13分)如图所示,质量为m的带电小物体以某一初速度从A点出发,在绝缘水平面上沿直线ABCD运动.已知A、B间的距离为l1,B、C间的距离为l2,AC段的动摩擦因数为μ(μ<1),CD段是光滑的,小物体在BC段上运动时还受到竖直向下的电场力F的作用,其大小为mg.
(13分)如图所示,质量为m的带电小物体以某一初速度从A点出发,在绝缘水平面上沿直线ABCD运动.已知A、B间的距离为l1,B、C间的距离为l2,AC段的动摩擦因数为μ(μ<1),CD段是光滑的,小物体在BC段上运动时还受到竖直向下的电场力F的作用,其大小为mg.
(1)当小物体的初速度为多大时可以到达CD区域?
(2)若小物体到达C点刚好停止,求小物体从B点运动到C点所需的时间t.
解析:(1)在AB段,小物体与水平面之间的弹力大小为mg
在BC段,小物体与水平面之间的弹力大小为mg
设当初速度为v0时,小物体恰好能滑到C点停止,由动能定理,有:
μmgl1+μ·mg·l2=mv
解得:v0=
即小物体的初速度v0≥时,可以到达CD区域.
(2)由牛顿第二定律知,小物体在BC段做减速运动的加速度为:a==μg,故有at2=l2
解得:t=2.
答案:(1)v0≥ (2)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com